
研究物质性质的基本程序是一个系统过程,其基本程序一般分为四个过程。下列是研究物质性质基本程序的第一步的是
A.预测物质的性质 B.观察物质的外观性质
C.进行实验和观察 D.作出相关的解释和结论
科目:高中化学 来源: 题型:
下列各组离子,在强酸性溶液中可以大量共存的是:( )
A.K+ 、Fe2+、NO3- 、Cl- B.Al3+、Na+ 、CO32- 、NO3-
C.NH4+、K+、NO3-、Cl- D.Na+ 、Ba2+、Cl- 、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:
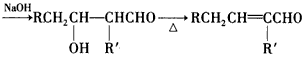 ①双键在链端的烯烃发生硼氢化一氧化反应,生成的醇羟基在链端:
①双键在链端的烯烃发生硼氢化一氧化反应,生成的醇羟基在链端:
R-CH=CH2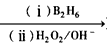 R-CH2CH2OH
R-CH2CH2OH
②RCH2CHO +R'CH2CHO
化合物M是一种香料,可用如下路线合成
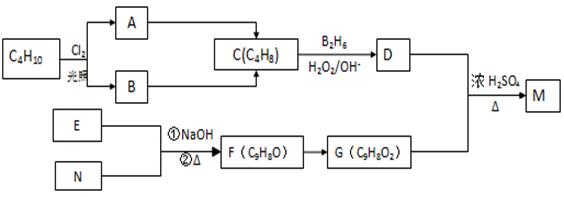
已知:核磁共振氢谱显示E分子中有两种氢原子,F为芳香化合物。请回答下列问题:
(1) 写出反应A→C的反应条件:___________ __________。
(2). 原料C4H10的名称是_________ _____(系统命名)。
(3) 写出M的结构简式:________ ___。
(4) 写出E和N生成F的化学方程式:_____________________ _____。
(5) 写出D和G生成M的化学方程式:_______ ______________ ____。
(6)写出与G具有相同官能团的G的所有芳香类同分异构体的结构简式:_________________ ___ __。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验操作说法中,正确的是
①用pH试纸测得氯水的pH为2
②用量筒、试管胶头滴管、玻璃棒、蒸馏水和pH试纸,可鉴别pH相等的硫酸和醋酸
③在进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
④用碱式滴定管量取25.00mL溴水
⑤可用渗析的方法除去淀粉中混有的少量NaCl杂质
⑥在进行过滤操作时,为了加快速率,可用玻璃棒不断搅拌过滤器中液体
A.①③⑤ B.②③⑤ C.③④⑤ D.①③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
含铬废水、铬渣对环境的污染问题备受关注,通过化学原理对废物进行有效处理变废为宝是目前的一个重要研究课题。
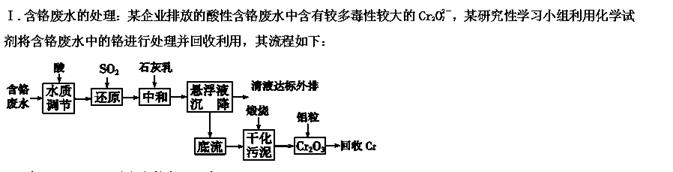 (1)请写出通入SO2时发生的离子反应:______________________________________。
(1)请写出通入SO2时发生的离子反应:______________________________________。
(2)该流程中干化污泥的主要成分为 (填化学式),写出加入铝粒时发生反应的化学方程式____________________________________。
(3)还原Cr2O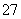 也可以使用其他还原剂,如电解还原法就是使用Fe电极电解酸性含铬废水,电解时产生的Fe2+作还原剂还原Cr2O
也可以使用其他还原剂,如电解还原法就是使用Fe电极电解酸性含铬废水,电解时产生的Fe2+作还原剂还原Cr2O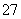 变为Cr3+,该反应的离子方程式为 。
变为Cr3+,该反应的离子方程式为 。
Ⅱ.含铬废渣的处理
铬渣烧结炼铁法:铬渣中约含有55%的氧化钙和氧化镁,此外还含有15%左右的氧化铁,这些都是炼铁所需的成分。少量的铬渣代替消石灰同铁矿粉、煤粉混合,经烧结后送入高炉冶炼,六价铬还原为三价铬或金属铬,金属铬熔入铁水,而其他成分熔入熔渣。炼铁可使铬渣彻底解毒并充分利用,是铬渣治理的良好方法之一。
(4)铬渣烧结炼铁法中煤粉的作用是 。(写两点)
(5)碱性溶液还原法:直接在碱性铬渣溶液中加入硫化钠等进行六价铬的还原反应,形成Cr(OH)3沉淀后,过滤回收铬污泥。请配平碱性溶液还原法中发生的离子反应:
 Cr2O
Cr2O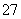 +
+ S2-+
S2-+ H2O===
H2O=== Cr(OH)3↓+
Cr(OH)3↓+ S2O
S2O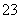 +
+ OH-
OH-
(6)若用碱性溶液还原法处理1L PH=9的含铬废水,处理后溶液的PH变为10,则理论上在此过程中处理掉的Cr2O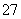 的物质的量约为 mol。
的物质的量约为 mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关0.2 mol·L-1 BaCl2溶液的说法中,不正确的是
A.500 mL溶液中Cl-浓度为0.2 mol·L-1
B.500 mL溶液中Ba2+浓度为0.2 mol·L-1
C.500 mL溶液中Cl-总数为0.2 NA
D.500 mL溶液中Ba2+和Cl-总数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
制备金属氯化物,常用两种方法:①用金属与氯气直接化合得到;②用金属与盐酸反应制得。下列氯化物中既能由金属和氯气直接反应制得,又能由金属和盐酸反应制得的是
A.CuCl2 B.FeCl3 C.AlCl3 D.FeCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
在蒸馏实验中,下列叙述不正确的是 ( )
A.在蒸馏烧瓶中放入几粒碎瓷片,防止液体暴沸
B.将温度计水银球放在蒸馏烧瓶支管口附近
C.冷水从冷凝管下口入,上口出
D.蒸馏烧瓶不用垫石棉网,可直接加热
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:

(1)W位于元素周期表第 周期第 族;W的原子半径比X的 (填“大”或“小”)。
(2)Z的第一电离能比W的 (填“大”或“小”); 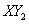 油固态变为气态所需克服的微粒间作用力是 ;氢元素、
油固态变为气态所需克服的微粒间作用力是 ;氢元素、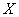 、
、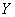 的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称 。
的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称 。
(3)震荡下,向Z单质与盐酸反应后的无色溶液中滴加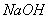 溶液直至过量,能观察到的现象是;
溶液直至过量,能观察到的现象是;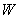 的单质与氢氟酸反应生成两种无色气体,该反应的化学方程式是 。
的单质与氢氟酸反应生成两种无色气体,该反应的化学方程式是 。
(4)在25°、101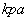 下,已知13.5g的
下,已知13.5g的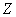 固体单质在
固体单质在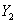 气体中完全燃烧后恢复至原状态,放热419
气体中完全燃烧后恢复至原状态,放热419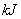 ,该反应的热化学方程式是 。
,该反应的热化学方程式是 。
25
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com