
【题目】在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+ O2 (g) ![]() 2SO3(g) △H< 0。查阅资料知:SO3熔点16.83℃,沸点44.8℃。
2SO3(g) △H< 0。查阅资料知:SO3熔点16.83℃,沸点44.8℃。
(1)600℃时,在一容积为2 L的密闭容器中,将二氧化硫和氧气混合,反应过程中SO2,O2,SO3物质的量变化如图。
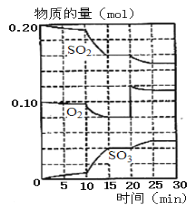
①据图判断,该反应处于平衡状态的时间是_______。
②计算600℃下,该反应的化学平衡常数 K=_______。
③据图判断,反应进行至20 min时,曲线发生变化的原因是________________(用文字表达)。
(2)某化学研究学习小组用下图的装置组装设计了一个实验,以测定SO2转化为SO3的转化率,仪器的连接顺序是a→h→i→b→c→f→g→d→e。
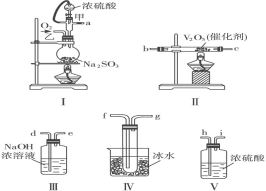
①为提高SO2的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序是____。
②在Ⅰ处用大火加热烧瓶时SO2的转化率会_______。(选填“增大”“不变”或“减小”)
③用n mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ处增重 m g,则本实验中SO2的转化率为_____________。
【答案】15~20 min、 25~30min 1.56 增大氧气的浓度(或物质的量) 先加热Ⅱ处催化剂 减小 ![]() ×100%
×100%
【解析】
(1)①根据化学平衡状态的特征分析;
②根据K的表达式和平衡时各物质的浓度计算;
③在SO2、O2、SO3物质的量的变化图中,20min时n(O2)突然增大,而此时SO2、SO3的物质的量不变,随后平衡正向移动,所以此时改变的条件应为增大O2的物质的量。
(2)I中制备SO2和O2的混合气,V装置干燥混合气,II装置实现二氧化硫的催化氧化,IV装置冷凝SO3,III装置吸收未反应的二氧化硫,据此分析结合反应特点解答。
(1)①据图判断,该反应处于平衡状态的时间是15~20min、25~30min;
答案为:15~20min、25~30min;
②600℃下,从图中可以看出,20min达平衡时,n(SO2)=0.16mol,n(O2)=0.08mol,n(SO3)=0.04mol,则浓度为c(SO2)=0.08mol/L,c(O2)=0.04mol/L,c(SO3)=0.02mol/L,
该反应的化学平衡常数 K=![]() ;
;
答案为:1.56;
③据图判断,反应进行至20 min时,曲线发生变化的原因是增大氧气的浓度(或物质的量);
答案为:增大氧气的浓度(或物质的量)。
(2)① 为提高SO2的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序是先加热Ⅱ处催化剂;
答案为:先加热Ⅱ处催化剂;
② 在Ⅰ处用大火加热烧瓶时,升高温度平衡逆向移动,导致SO2的转化率会减小;
答案为:减小;
③ n mol Na2SO3粉末与足量浓硫酸反应,理论上生成SO2 n mol;Ⅲ处增重 m g,说明未反应的SO2为mg,参加反应的SO2的质量为(64n-m)g,实验中SO2的转化率为![]() ;
;
答案为:![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】草酸二甲酯可用作制备维生素B13的中间体,也可用作增塑剂。实验室以草酸![]() 和甲醇为原料制备草酸二甲酯的一种方法如下:
和甲醇为原料制备草酸二甲酯的一种方法如下:![]()
![]()
![]() 。
。
相关物质的有关数据如下表所示:
物质 | 苯 | 甲醇 | 草酸二甲酯 |
熔点/℃ | 5.5 | -97 | 54 |
沸点/℃ | 80.1 | 64.3 | 163.5 |
相对分子质量 | 78 | 32 | 118 |
水溶性 | 不溶 | 互溶 | 不溶 |
实验过程:向如图反应装置中加入27g草酸、40g无水甲醇、100ml苯、5ml浓硫酸,搅拌下加热回流;待反应完全后,分离出甲醇和苯,所得反应液经水洗,有机层再用10%的碳酸钠溶液洗涤,然后用蒸馏水洗涤,加无水氯化钙固体干燥;过滤,滤液冷却后析出晶体,干燥,得草酸二甲酯30.1g。
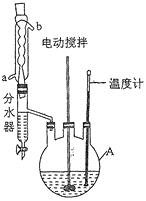
回答下列问题:
(1)仪器A的名称为____________,反应过程中冷却水应从________(填“a”或“b”)口进入。
(2)分离出甲醇和苯的操作名称为______________________________。
(3)用10%的碳酸钠溶液洗涤的目的是____________________________________。
(4)甲醇过量的目的是________________________________________________,浓硫酸的作用是_____________________________________________。
(5)分水器的优点是__________________________________________(任写一点)。
(6)本实验的产率是___________(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2018年8月31日,华为公司发布AI芯片麒麟980,标志着我国高科技企业的芯片制造技术迈入国际领先水平。组成芯片的核心物质是高纯度硅。下图是以石英砂为原料同时制备硅和金属锂的流程。![]() 石英砂的主要成分为
石英砂的主要成分为![]() ,含有少量
,含有少量![]() 、
、![]() 、
、![]()
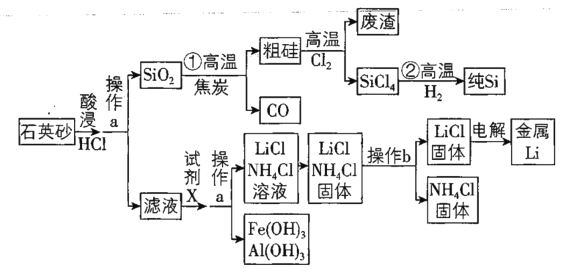
已知:LiCl的熔点是![]() 、沸点是
、沸点是![]() ;
;![]() 在
在![]() 分解完全。常温下,
分解完全。常温下,![]() ,
,![]() 。
。
(1)粗硅中常含有副产物SiC,请写出![]() 中生成SiC的反应方程式__________。
中生成SiC的反应方程式__________。
(2)操作a为___________;试剂X是___________。
(3)已知操作b为加热,可选择的适宜温度是______
![]()
![]()
![]()
![]()
(4)本生产工艺要求,要控制LiCl和![]() 溶液中的杂质离子浓度在
溶液中的杂质离子浓度在![]() 以下,应控制溶液的pH为_____,此时溶液中
以下,应控制溶液的pH为_____,此时溶液中![]() 的浓度为___________ 。
的浓度为___________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二苯基乙二酮常用作医药中间体及紫外线固化剂,可由二苯基羟乙酮氧化制得,相关物质的物理参数、化学方程式及装置图(加热和夹持装置已略去)如下:
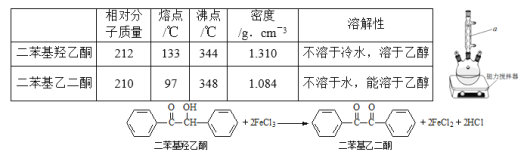
在反应装置中,加入10ml冰醋酸、5.50gFeCl3固体、10ml水及少量碎瓷片,加热至沸腾,停止加热,待沸腾平息后加入2.12g二苯基羟乙酮,继续加热回流至二苯基羟乙酮完全反应。反应结束后加水煮沸,冷却后即有二苯基乙二酮粗产品析出,用70%乙醇水溶液重结晶提纯,得到1.80g产品。
重结晶过程如下:
加热溶解→活性炭脱色→趁热过滤 →冷却结晶→抽滤→洗涤→干燥
请回答以下问题:
(1)装置图中仪器a的名称是_______________,其作用是______________。
(2)加入碎瓷片的作用是________。若加热后发现未加碎瓷片,应采取的正确方法是____________________________________________________。
(3)实验中可采用薄层色谱跟踪反应进程,其原理和操作与纸上层析类同,通过观察薄层色谱展开后的斑点(在实验条件下,只有二苯基羟乙酮和二苯基乙二酮能够产生斑点)判断样品中的成分。下图分别为加入二苯基羟乙酮后反应开始、回流15min、30min、45min和60min时,用毛细管取样、点样,薄层色谱展开后的斑点:
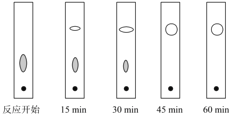
该实验条件下加热________后可认为反应结束。
A.15min B.30min C.45min D.60min
(4)上述重结晶过程中,____________(填步骤名称)操作除去了不溶性杂质。
(5)在重结晶过程中,不可选用明火直接加热,原因是_________________________。
(6)不选择蒸馏的方法提纯二苯基乙二酮粗产品的原因是______________________。
(7)本实验的产率是_________%。(保留3位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的是( )
A. 用 所示装置分离CCl4和I2的混合物
所示装置分离CCl4和I2的混合物
B. 用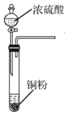 所示装置获取少量SO2气体
所示装置获取少量SO2气体
C. 用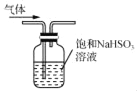 所示装置除去CO2气体中的少量SO2
所示装置除去CO2气体中的少量SO2
D. 用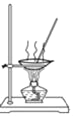 所示装置蒸发NaCl溶液获得NaCl晶体
所示装置蒸发NaCl溶液获得NaCl晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酰氯(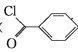 )是制备染料,香料药品和树脂的重要中间体,以光气法制备苯甲酰氯的原理如下(该反应为放热反应):
)是制备染料,香料药品和树脂的重要中间体,以光气法制备苯甲酰氯的原理如下(该反应为放热反应):
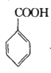 +COCl2
+COCl2![]()
![]() +CO2+HCl
+CO2+HCl
已知物质性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 溶解性 |
苯甲酸 | 122.1 | 249 | 微溶于水,易溶于乙醇、乙醚等有机溶剂 |
碳酰氯(COCl2) | -188 | 8.2 | 较易溶于苯、甲苯等。遇水迅速水解,生成氯化氢,与氨很快反应,主要生成尿素[CO(NH2)2]和氯化铵等无毒物质 |
苯甲酰氯 | -1 | 197 | 溶于乙醚、氯仿和苯。遇水或乙醇逐渐分解,生成苯甲酸或苯甲酸乙酯和氯化氢 |
三氯甲烷(CHCl3) | -63.5 | 63.1 | 不溶于水,溶于醇、苯。极易挥发,稳定性差,450℃以上发生热分解 |
I.制备碳酰氯
反应原理:2 CHCl3+O2![]() 2HCl+COCl2
2HCl+COCl2
甲. 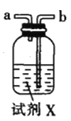 乙.
乙. 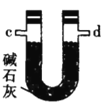 丙.
丙. 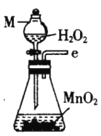 丁.
丁.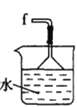 戊.
戊. 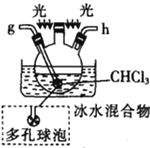
(1)仪器M的名称是____________
(2)按气流由左至右的顺序为___________→c→d→_________→_________→_________→_________→_________.
(3)试剂X是_______________(填名称)。
(4)装置乙中碱石灰的作用是____________。
(5)装置戊中冰水混合物的作用是____________;多孔球泡的作用是________________。
Ⅱ.制备苯甲酰氯(部分夹持装置省略)
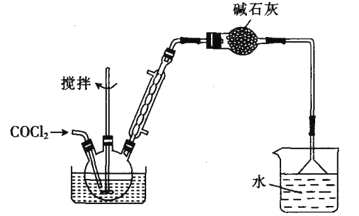
(6)碳酰氯也可以用浓氨水吸收,写出该反应的化学方程式:______________。
若向三颈烧瓶中加入610g苯甲酸,先加热至140~150℃,再通入COCl2,充分反应后,最后产品经减压蒸馏得到562g苯甲酰氯,则苯甲酸的转化率为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用呋喃甲醛为原料制备呋喃甲醇与呋喃甲酸。
Ⅰ、制备原理:
2![]() +NaOH
+NaOH![]() +
+![]()
![]() +HCl
+HCl![]() +NaCl
+NaCl
Ⅱ、实验步骤
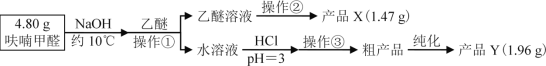
Ⅲ、相关信息
呋喃甲醛 | 呋喃甲醇 | 呋喃甲酸 | 乙醚 | |
熔点/℃ | -36.5 | -29 | 133 | -116.3 |
沸点/℃ | 161.7 | 170 | 231 | 34.5 |
水溶性 | 微溶 | 微溶 | 可溶 | 不溶 |
相对分子质量 | 96 | 98 | 112 | 74 |
Ⅳ、实验装置
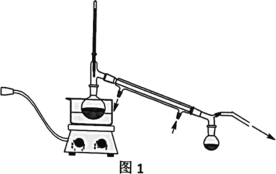
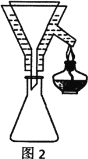
V、分析与思考,回答下列问题:
(1)操作①名称___
(2)操作②的装置如图1所示,收集产品X时温度计的读数应控制在90℃左右,其原因是___。
(3)操作①所得水溶液,加盐酸须控制pH为2~3,pH<3的理由是___;控制溶液pH时,应选择的指示剂是__。
(4)粗产品Y纯化过程用图2装置进行热过滤,具体操作:向铜漏斗中加热水→___→拆装置。涉及操作顺序最合理的选项。
A.加热漏斗支管→放入短颈漏斗→放入滤纸→放接液烧杯→倒入热的待滤液
B.放入短颈漏斗→放接液烧杯→加热漏斗支管→放入滤纸→倒入热的待滤液
C.放入短颈漏斗→放入滤纸→加热漏斗支管→放接液烧杯→倒入热的待滤液
D.放入短颈漏斗→放入滤纸→放接液烧杯→倒入热的待滤液→加热漏斗支管
(5)共消耗30mL萃取剂乙醚,从萃取效果角度思考,下列4种萃取方式最合理的是__。
A.30mL、0mL、0mL B.10mL、10mL、10mL
C.15mL、10mL、5 mL D.5mL、10mL、15mL
(6)计算产品Y的产率ω(Y)=___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某NaOH溶液中通入CO2气体后得到溶液M,因CO2通入的量的不同,溶液M的组成也不同,若向M中加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示,则下列分析与判断不正确的是(不计CO2的溶解)
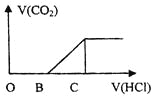
A.若OB=0,则形成溶液M所发生的离子方程式为OH-+CO2=![]()
B.若OB=BC,则溶液M为![]() 溶液
溶液
C.若OB>BC,则溶液M中大量存在的阴离子为![]() 和
和![]()
D.若3OB=BC,则溶液M中![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于溶液的酸碱性说法正确的是
A.含OH-的溶液一定呈碱性B.在100°C时,纯水的pH<7,因此显酸性
C.c(H+)=c(OH-)的溶液一定呈中性D.pH=14的溶液碱性最强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com