

���� ��1����2NaNO2+4HI=2NO+I2+2NaI+2H2O��֪��HI��IԪ�صĻ��ϼ۲������ߣ����ֲ��䣬�����Σ�NaI������HI�������Ժͻ�ԭ�ԣ�NԪ�صĻ��ϼ���+3����Ϊ+2��IԪ�صĻ��ϼ���-1����Ϊ0���Դ������
��2��ѡ���Լ�ʱҪ���ǣ�����ʹNaNO2ת����������Ⱦ��
��3��˫��ˮ����������˵��˫��ˮ��Ԫ�ػ��ϼ����ߣ����ֻ�ԭ��˵��˫��ˮ��Ԫ�ػ��ϼ۽��ͣ�
��4���������������ԣ���������������ԣ���ԭ���������ԣ�
��5���ٸ���������ԭ��Ӧ���������ͻ�ԭ�����ص��������Ѱ�ҷ�Ӧ��������Ȼ���ϻ��ϼ����������ƽ��
�ڸ����������ķ�Ӧ���������ϼ۵ı仯����������õ�ת�Ƶ��ӵ���Ŀ��
��� �⣺��1��NԪ�صĻ��ϼ���+3����Ϊ+2��IԪ�صĻ��ϼ���-1����Ϊ0����˫���ű�ʾ����ת�Ƶķ������ĿΪ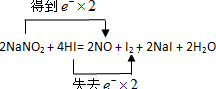 ��
��
�ʴ�Ϊ�� ��
��
��2��NaNO2��N2�DZ���ԭ������ӻ�ԭ����NԪ������������O��ClԪ�أ���ֻ�ܼ�NH4Cl����ԭ��������ʽΪNaNO2+NH4Cl�TNaCl+N2��+2H2O�����������е��õ�3����ָ�����еĵ����Ȼ���е�ʧȥ3����ָ�����еĵ���
�ʴ�Ϊ��B��
��3��A����Ԫ�صĻ��ϼ۱仯��B��AgԪ�صĻ��ϼ۽��͡�˫��ˮ��OԪ�صĻ��ϼ����ߣ�B�й���������л�ԭ�ԣ�C��˫��ˮ����Ԫ�ػ��ϼ�����Ҳ���ͣ����ֻ�ԭ�Ժ������ԣ�ֻ��D��˫��ˮ����Ԫ�ػ��ϼ۽��ͣ�˵��˫��ˮ���������������������ԣ��ʴ�Ϊ��D��
��4����ӦAg2O+H2O2=2Ag+O2��+H2O�У�����������������˫��ˮ����ԭ������������Ag2O��H2O2����Ӧ3H2O2+Cr2��SO4��3+10KOH=2K2CrO4+3K2SO4+8H2O�У�˫��ˮ��������������������������������H2O2��K2CrO4����������˳��ΪAg2O��H2O2��K2CrO4��
�ʴ�Ϊ��Ag2O��H2O2��K2CrO4��
��5���ٸ÷�Ӧ�����У���������������Ժ�˫��ˮ�Ļ�ԭ�Ե��¶��䷢��������ԭ��Ӧ�����������������Ԫ�ش�+7��Ϊ+2�ۣ����ϼ۽���5�ۣ�˫��ˮ����Ԫ�ػ��ϼ۴�-1�۱�Ϊ0�ۣ����ϼ���������2�ۣ������������ӵ�ϵ��Ϊ2��˫��ˮ��ϵ��Ϊ5��Ȼ�����������غ���ƽ�ɵø÷�Ӧ�����ӷ���ʽΪ��2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2����
�ʴ�Ϊ��2MnO4-+5H2O2��
��������Ӧ������5mol����ת�Ƶ���10mol������Ӧ����6.72L����״������0.3mol��������ʱ����ת�Ƶĵ���Ϊ��10mol��$\frac{0.3mol}{5}$=0.6mol��
�ʴ�Ϊ��0.6��
���� ���⿼����������ԭ��Ӧ����ƽ���ۺ�Ӧ�ã���Ŀ�Ѷ��еȣ�����֪ʶ��϶ࡢ�ۺ��Խ�ǿ����ֿ���ѧ���ķ������������������Ӧ��������ע������������ԭ��Ӧ����ƽ��������ȷ����������ԭ���ĸ���жϷ�����


 �Ƹ�С״Ԫ�������������ϵ�д�
�Ƹ�С״Ԫ�������������ϵ�д� ����һ������ܼƻ�ϵ�д�
����һ������ܼƻ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��5.85 g NaCl��������1 Lˮ�п����0.1mol/L��NaCl ��Һ | |
| B�� | 500 ml 0.5mol/L ��NaOH��Һ��NaOH����0.25 mol | |
| C�� | ��200mL 3mol/L��BaCl2��Һ��100mL 3mol/L��KCl��Һ��Ϻ���Һ�е�c��Cl-����Ȼ��3mol/L�����Ի�Ϻ�����仯�� | |
| D�� | ��100g 20%��NaCl��Һ��100g H2O��Ϻ�NaCl��Һ������������10% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷�Ӧ���û���Ӧ | B�� | �÷�Ӧ��FeCl3����ԭ�� | ||
| C�� | ��ԭ�ԣ�Cu��Fe2+ | D�� | �����ԣ�CuCl2��FeCl3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �轺����װʳƷ�ĸ����û�з�����ѧ�仯 | |
| B�� | ̼��ά��һ���¿����IJ��ϣ������ںϳ��л��߷��ӻ����� | |
| C�� | Al2O3�����ͻ���ϣ�Al��OH��3������ȼ�� | |
| D�� | С�մ�������θ������һ��ҩ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CuO��Cu��OH��2 | B�� | CaCO3��CaCl2 | C�� | Na2SO4��NaCl | D�� | Mg��NO3��2��KNO3 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com