
【题目】利用某冶金行业产生的废渣(主要含![]() ,还有少量
,还有少量![]() 、
、![]() 等杂质)可以制备
等杂质)可以制备![]() ,生产流程如下:
,生产流程如下:
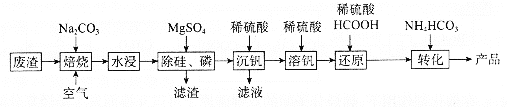
已知:![]() 微溶于水、溶于碱生成
微溶于水、溶于碱生成![]() (加热生成
(加热生成![]() ),具有强氧化性。向
),具有强氧化性。向![]() 溶液中加酸,不同
溶液中加酸,不同![]() 对应的主要存在形式如表:
对应的主要存在形式如表:
|
| 10.6~12 | 约8.4 | 3~8 | 约2 | <1 |
存在形式 |
|
|
|
|
|
|
回答下列问题:
(1)“焙烧”后V元素转化为![]() ,
,![]() 元素转化为________(写化学式)。
元素转化为________(写化学式)。
(2)欲除尽磷元素(即![]() ),最终溶液中
),最终溶液中![]() 的浓度至少为________
的浓度至少为________![]() (已知
(已知![]() )。
)。
(3)“沉钒”过程中,![]() 由8.5到5.0发生反应的离子方程式为________;最终需要控制
由8.5到5.0发生反应的离子方程式为________;最终需要控制![]() 约为________;“沉钒”最终得到的主要含钒物质是________(写化学式)。
约为________;“沉钒”最终得到的主要含钒物质是________(写化学式)。
(4)“还原”和“转化”过程中主要反应的离子方程式分为________、________。
【答案】![]()
![]()
![]() 2
2 ![]()
![]()
![]()
【解析】
结合题干信息,根据(NH4)5(VO)6(CO3)4(OH)9·10H2O的生产流程分析,废渣加入Na2CO3在空气中焙烧得到NaVO3和Na2SiO3,Na3PO4,水浸后加入MgSO4得到H2SiO3和Mg3(PO4)2的滤渣除去,滤液加入稀硫酸沉钒最终得到V2O5,过滤,再加入稀硫酸溶解得到VO2+,加入HCOOH还原得到VO2+,加入NH4HCO3转化得到产品,据此分析解答。
(1)由上述分析可知,废渣加入Na2CO3在空气中焙烧得到NaVO3和Na2SiO3,Na3PO4,故答案为:Na2SiO3;
(2)因为Ksp[Mg3(PO4)2]=c3(Mg2+)·c2(PO43-),已知Ksp[Mg3(PO4)2]=1.0×10-24,假设PO43-刚好完全除尽,即c(PO43-)=1.0×10-5mol·L-1,则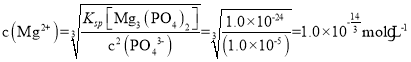 ,即溶液中Mg2+的浓度至少为
,即溶液中Mg2+的浓度至少为![]() ,故答案为:
,故答案为:![]() ;
;
(3)结合已知数据分析可知,“沉钒”过程中,pH由8.5到5.0主要发生的反应时V3O93-转化为V10O286-,反应的离子方程式为:10V3O93-+12H+===3V10O286-+6H2O,沉钒最终得到的物质时V2O5,所需要控制的pH约为2,故答案为:10V3O93-+12H+===3V10O286-+6H2O;2;V2O5;
(4)根据上述分析,“还原”过程中HCOOH将VO2+还原得到VO2+,自身被氧化为CO2,根据氧化还原反应的规律得到离子反应方程式为:2VO2++HCOOH+2H+===2VO2++CO2↑+2H2O,“转化”时,NH4HCO3与上一步还原得到VO2+反应得到产品,反应的离子反应方程式方程式为:5NH4++6VO2++17HCO3-+6H2O===(NH4)5(VO)6(CO3)4(OH)9·10H2O+13CO2↑,故答案为:2VO2++HCOOH+2H+===2VO2++CO2↑+2H2O;5NH4++6VO2++17HCO3-+6H2O===(NH4)5(VO)6(CO3)4(OH)9·10H2O+13CO2↑。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】毒奶粉中发现的化工原料三聚氰胺可以由下列反应合成:CaO+3C ![]() CaC2+CO↑,CaC2+N2
CaC2+CO↑,CaC2+N2 ![]() CaCN2+C,CaCN2+2H2O=NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
CaCN2+C,CaCN2+2H2O=NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
(1)写出与Ca在同一周期且未成对电子数最多的基态原子的电子排布式:___________;CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O,由此可以推知CN22-的空间构型为________。
(2)1mol尿素分子[CO(NH2)2]中含有的π键与σ键的数目之比为_______;
(3)三聚氰胺俗称“蛋白精”,其结构为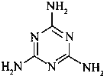 。其中氮原子的杂化方式有_____________。
。其中氮原子的杂化方式有_____________。
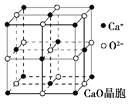
(4)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为______,Ca2+采取的堆积方式为____________,其中O2-处于Ca2+堆积形成的八面体空隙中;已知CaO晶体的密度为ρ,求晶胞中距离最近的两个钙离子之间的距离_____________(列出计算式);
(5)配位化合物K3[Fe(CN)n]遇亚铁离子会产生蓝色沉淀,因此可用于检验亚铁离子,已知铁原子的最外层电子数和配体提供电子数之和为14,求n=_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作或装置能达到目的的是( )
A | B | C | D |
|
|
|
|
混合浓硫酸和乙醇 | 配制一定浓度的溶液 | 收集 | 证明乙炔可使溴水褪色 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某恒容密闭容器中进行如下可逆反应:2M(g)+N(g)![]() W(?)+4Q(g)△H<0,起始投料只有M和N。下列示意图正确且能表示该可逆反应达到平衡状态的是
W(?)+4Q(g)△H<0,起始投料只有M和N。下列示意图正确且能表示该可逆反应达到平衡状态的是
A. B.
B.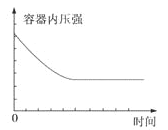
C.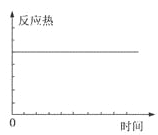 D.
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积和温度不变的密闭容器中充入amolX和足量Y,发生反应:2X(g)+Y(s)![]() Z(g)+W(g),建立平衡后,若再加入bmolX,下列判断不正确的是( )
Z(g)+W(g),建立平衡后,若再加入bmolX,下列判断不正确的是( )
A.平衡正向移动B.X的转化率不变
C.X的转化率减小D.Y的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不同条件下,用O2氧化一定浓度的FeCl2溶液过程中所测的实验数据如图所示。下列分析或推测不合理的是
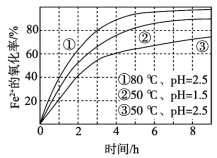
A. Fe2+的氧化率随时间延长而逐渐增大
B. 由②和③可知,pH越大,Fe2+氧化速率越快
C. 由①和③可知,温度越高,Fe2+氧化速率越快
D. 氧化过程的离子方程式为:4Fe2+ + O2 + 4H+ == 4Fe3+ + 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某硫酸厂以含有SO2的尾气、氨气等为原料,合成有重要应用价值的硫化钙、硫酸钾、亚硫酸铵等物质。合成路线如下:
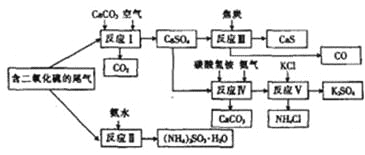
(1)写出反应Ⅲ的化学方程式:___________________________________________。
(2)下列有关说法正确的是_________(填字母)
A.反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙
B.反应Ⅱ和反应Ⅲ的基本反应类型相同
C.反应Ⅳ需控制在60~70℃,目的之一是减少碳酸氢铵的分解
D.反应Ⅴ中的副产物氯化铵可用作氮肥
(3)(NH4)2SO3可用于电厂等烟道气中脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,形成共生系统。写出二氧化氮与亚硫酸铵反应的化学方程式:___________。
(4)很多硫酸厂为回收利用SO2,直接用氨水吸收法处理尾气。
① 用15.0 mL 2.0 mol/L氨水吸收标准状况下448 mL SO2,吸收液中的溶质为_______。
② 某同学用酸性KMnO4溶液滴定上述吸收液,当达到滴定终点时,消耗KMnO4溶液25.00 mL,则酸性KMnO4溶液中c(KMnO4) =_________________。
(5)氨气用途广泛,可以直接用于燃料电池,下图是用氨水作原料的燃料电池的工作原理。
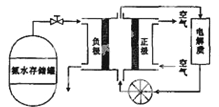
氨气燃料电池的电解质溶液最好选择________(填“酸性”、“碱性”或“中性”)溶液,氨气燃料电池的反应是氨气与氧气生成一种常见的无毒气体和水,该电池总反应的化学方程式是___________,负极的电极反应式是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用冬青的提取物合成出一种抗结肠炎药物.其结构简式如图所示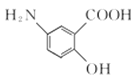 :下列叙述中不正确的是( )
:下列叙述中不正确的是( )
A. 该物质属于芳香族化合物,易溶于水
B. 该物质可以发生加成、氧化、取代等反应
C. 该物质能与强酸和强醎反应,也能与碳酸氢钠反应
D. 仅改变这三条侧链在苯环上的位置,还可得到10种同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下图所示转化关系(X代表卤素),说法不正确的是
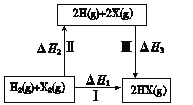
A.2H(g) +2X(g) = 2HX(g) ΔH3<0
B.途径Ⅰ生成HX的反应热与途径无关,所以ΔH1 = ΔH2 + ΔH3
C.途径Ⅰ生成HCl放出的热量比生成HBr的多,说明HCl比HBr稳定
D.Cl、Br、I的非金属性依次减弱,所以途径Ⅱ吸收的热量依次增多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com