
| A. | ①② | B. | ④⑥ | C. | ③⑤ | D. | ②④ |
分析 X、Y、Z三者均为短周期元素,已知X元素有一种同位素不含中子,则X为H;Y元素原子的最外层电子数是次外层电子数的2倍,则次外层为2,最外层电子数为4,可知Y为C;Z元素原子的最外层电子数是次外层电子数的3倍,则次外层为2,最外层电子数为6,可知Z为O,结合H为+1价、O为-2价及化合物中正负化合价代数和为0来解答.
解答 解:X、Y、Z三者均为短周期元素,已知X元素有一种同位素不含中子,则X为H;Y元素原子的最外层电子数是次外层电子数的2倍,则次外层为2,最外层电子数为4,可知Y为C;Z元素原子的最外层电子数是次外层电子数的3倍,则次外层为2,最外层电子数为6,可知Z为O,
①HCO3中C为+5价,不存在;
②H2CO2中C为+2价,不存在+2价含氧酸;
③H2CO3为碳酸,C元素为+4价,存在;
④H2C2O2中C为+1价,不存在;
⑤H2C2O4为草酸,C为+3价,存在;
⑥H4C2O2为乙酸,C元素的化合价为0,存在,
并非都存在的一组分子是④⑥,
故选B.
点评 本题考查原子结构及元素周期律,为高频考点,把握原子结构推断元素为解答的关键,侧重分析与应用能力的考查,注意碳元素形成的有机物,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题

| A. | 用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液 | |
| B. | 用装置①进行电镀,镀件接在b极上 | |
| C. | 装置①的a极为阴极 | |
| D. | 装置②的总反应是:Cu+2Fe3+═Cu2++2Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
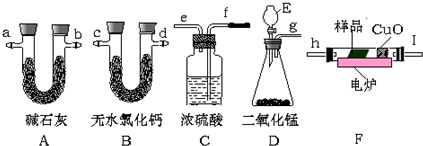
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-=Cl2↑ | |
| B. | 氢氧燃料电池的负极反应式:O2+2H2O+4e-=4OH- | |
| C. | 在铁的表面镀上一层锌,铁作阳极,电极反应式为:Zn2++2e-=Zn | |
| D. | 钢铁发生电化学腐蚀的正极反应式:Fe-2e-=Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
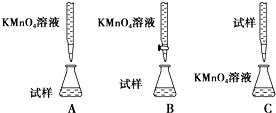
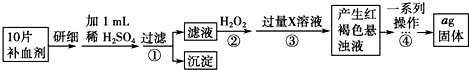
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al4C3晶体,熔点2200℃,熔融态不导电 | |
| B. | C3N4晶体具有比金刚石还大的硬度 | |
| C. | VF5晶体易溶于一些有机溶剂中 | |
| D. | BaCl2熔融状态下能够导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3•H2O+H2O | |
| B. | 澄清石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O | |
| C. | 钠与水反应:2Na+2H2O=2Na++2OH-+H2↑ | |
| D. | 碳酸钡中加入稀硫酸:BaCO3+2H+=Ba2++CO2↑+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com