
【题目】尼美舒利是一种非甾体抗炎药,它的一种的合成路线如下:

已知:![]() (易氧化)
(易氧化)
![]()
回答下列问题:
(1)B的结构简式为_______________________。
(2)由C生成D的化学方程式为_______________,其反应类型为___________。
(3)E中的官能团有___________、___________ (填官能团名称)。
(4)E的同分异构体中能同时满足下列条件的共有_______种(不含立体异构);
①含有两个苯环且两个苯环直接相连
②能与FeCl3溶液发生显色反应
③两个取代基不在同一苯环上
其中核磁共振氢谱为6组峰,峰面积比为2∶2∶2∶2∶2∶1的结构简式为_________。
(5)由甲苯为原料可经三步合成2,4,6-三氨基苯甲酸,合成路线如下:

反应①的试剂和条件为____________;中间体B的结构简式为________________;
【答案】![]()
![]() +
+![]() →
→ +NaBr取代反应醚键氨基9
+NaBr取代反应醚键氨基9![]() 浓硝酸/浓硫酸,加热
浓硝酸/浓硫酸,加热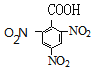
【解析】
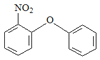
F和硝酸发生取代反应生成尼美舒利,根据尼美舒利的结构简式可以确定F为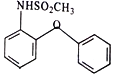 ,根据尼美舒利及流程图知,A为
,根据尼美舒利及流程图知,A为![]() ,A发生取代反应生成B,B为
,A发生取代反应生成B,B为![]() ,
,![]() 发生邻位取代反应生成C,C为
发生邻位取代反应生成C,C为![]() ,C和苯酚钠发生反应生成D,D为
,C和苯酚钠发生反应生成D,D为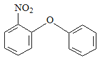 ,
, 发生还原反应生成E,E为
发生还原反应生成E,E为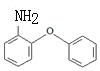 。
。
(1)通过以上分析知,B为![]() ,故答案为:
,故答案为:![]() ;
;
(2)C为![]() ,C和苯酚钠发生反应生成D为
,C和苯酚钠发生反应生成D为 ,反应方程式为
,反应方程式为![]() +
+![]() →
→ +NaBr,为取代反应,故答案为:
+NaBr,为取代反应,故答案为:![]() +
+![]() →
→ +NaBr;取代反应;
+NaBr;取代反应;
(3)E为 ,E中官能团为醚键和氨基,故答案为:醚键;氨基;
,E中官能团为醚键和氨基,故答案为:醚键;氨基;
(4)E为 ,E的同分异构体中能同时满足下列条件:①含有两个苯环且两个苯环直接相连;②能与FeCl3溶液发生显色反应,说明含有酚羟基,③两个取代基不在同一苯环上,另一个取代基为氨基,如果-OH位于苯基的邻位,则氨基有3种结构;如果-OH位于苯基间位,氨基有3种结构;如果-OH位于苯基对位,氨基有3种结构,所以符合条件的有9种;其中核磁共振氢谱为6组峰,峰面积比为2:2:2:2:2:1的结构简式为
,E的同分异构体中能同时满足下列条件:①含有两个苯环且两个苯环直接相连;②能与FeCl3溶液发生显色反应,说明含有酚羟基,③两个取代基不在同一苯环上,另一个取代基为氨基,如果-OH位于苯基的邻位,则氨基有3种结构;如果-OH位于苯基间位,氨基有3种结构;如果-OH位于苯基对位,氨基有3种结构,所以符合条件的有9种;其中核磁共振氢谱为6组峰,峰面积比为2:2:2:2:2:1的结构简式为![]() ,故答案为:9;
,故答案为:9;![]() ;
;
(5)由甲苯为原料可经三步合成2,4,6-三氨基苯甲酸,甲苯先和浓硝酸发生取代反应生成A为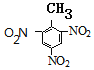 ,
, 被氧化生成
被氧化生成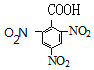 ,
, 被还原生成2,4,6-三氨基苯甲酸,反应①的试剂和条件为浓硝酸/浓硫酸,加热;中间体B的结构简式为
被还原生成2,4,6-三氨基苯甲酸,反应①的试剂和条件为浓硝酸/浓硫酸,加热;中间体B的结构简式为  ,故答案为:浓硝酸/浓硫酸,加热;
,故答案为:浓硝酸/浓硫酸,加热; 。
。


科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①-⑩在表中的位置,用化学用语回答下列问题:

(1)非金属性最强的是______(填元素符号),化学性质最不活泼的是_____(填元素符号)。
(2)由①、④、⑥、⑨中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
(3)②、③、⑨的最高价含氧酸的酸性由强到弱的顺序是_____________。(填化学式)
(4)表中能形成两性氢氧化物的元素是_________(填元素符号),分别写出该元素的氢氧化物与⑥、⑧最高价氧化物的水化物反应的离子方程式:___________________,_________________________。
(5)请设计一个实验方案,比较④、⑧单质氧化性的强弱,并描述现象和结论:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用0.100 mol·L-1盐酸分别滴定20.00 mL 0.100 mol·L-1的氨水和20.00 mL 0.100 mol·L-1NaOH溶液,两溶液的pH与所加盐酸体积(V)的关系如图所示。下列说法正确的是 ( )

A. Kb(NH3·H2O)的数量级为10—4
B. 10 < a < 20
C. P点溶液中:c(NH4+)>c(Cl一)
D. 水的电离程度:M > N > P
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加几滴石蕊溶液。下列实验现象描述正确的是

A. 逸出气体的体积,a电极的小于b电极的
B. 一电极逸出无味气体,另一电极逸出刺激性气体
C. a电极附近呈红色,b电极附近呈蓝色
D. a电极附近呈蓝色,b电极附近呈红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上采用接触法制硫酸,其中在接触室进行的反应是( )
A. S+O2![]() SO2B. 4FeS2+11O2
SO2B. 4FeS2+11O2![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
C. 2SO2+O2![]() 2SO3D. SO3 + H2O=H2SO4
2SO3D. SO3 + H2O=H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下五种有色溶液与SO2作用,能褪色且其实质相同的是( )
①滴有石蕊的NaOH溶液 ②氯水 ③酸性KMnO4溶液 ④品红溶液 ⑤碘和淀粉的混合物
A.①④B.①②③C.②③④D.②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取少量NaHSO3的实验装置如图所示:

请回答:
(1)实验中取一定量Cu片和一定量浓H2SO4放在圆底烧瓶中共热,至反应结束后,发现烧瓶中还有少量Cu剩余,则H2SO4是否剩余?______,原因是_____________。
①下列药品中,能够证明反应后烧瓶中有硫酸剩余的是_______。
A.Fe粉 B.BaCl2溶液 C.Ag D.饱和NaHSO3溶液
②当向甲中反应后的溶液中通入氧气,发现铜片全部溶解,且仅生成硫酸铜溶液,则该反应的离子方程式为__________。
(2)装置乙的作用是______________。
(3)请写出铜与浓硫酸反应的化学方程式:______。
(4)下列说法正确的是_____(填序号)。
a.甲装置使用的玻璃仪器有:酒精灯、玻璃管、长颈漏斗、圆底烧瓶
b.酸性KMnO4溶液用于尾气处理
c.当把品红溶液滴入锥形瓶中,若品红不褪色,说明无NaHSO3产生
d.当把品红溶液滴入锥形瓶中,若品红褪色,说明NaOH已完全转化为NaHSO3
e.若把品红溶液换成酸性高锰酸钾溶液,并滴入锥形瓶中,不显紫红色,说明NaOH已完全转化为NaHSO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)写出表示含有8个质子、10个中子的原子的化学符号:________;
(2)32号元素在元素周期表中的位置___________________;
(3)在N2、H2S、NaCl、NH4Cl、Na2O2、H2O2中,既含有离子键又含有极性键的是________________ ,既含有离子键又含有非极性键的是______________;
(4) A、B、C为短周期元素,在周期表中所处的位置如图所示,A、C两种元素的原子核外电子数之和等于B原子的质子数,请回答下列问题:
![]()
写出A、B、C三种元素的符号:A_______,B________,C________;B在周期表中位置是 __________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com