
【题目】硫酸亚铁是一种重要的化工原料,可以制备一系列物质(如下图所示)。下列说法错误的是( )

A. 碱式硫酸铁水解能产生Fe(OH)3胶体,可用作净水剂
B. 为防止NH4HCO3分解,生产FeCO3需在较低温度下进行
C. 可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化
D. 常温下,(NH4)2Fe(SO4)2在水中的溶解度比FeSO4的大
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)是一种综合性能优良的陶瓷材料,能缓慢水解,不耐酸碱腐蚀。某小组探究在实验室制备AlN并测定产品纯度,设计实验如下。请回答:
Ⅰ.制备AlN
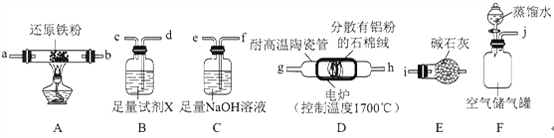
(1)实验时,以空气为原料制备AlN。按气流由左向右的方向,上述装置的正确连接顺序为j→________→i(填仪器接口字母编号)。
(2)上述装置中,需要检漏的仪器名称为________。
(3)试剂X的作用为________。
(4)装置D中发生反应的化学方程式为________。
Ⅱ.测定产品纯度
(5)设计实验证明:装置D的产品中含有Al单质________。
(6)测定产品纯度:取装置D中产品4.37g,加入足量NaOH浓溶液;通入水蒸气,将生成的气体全部蒸出,用V1mLc1mol·L-1的盐酸吸收;以酚酞作指示剂,用c2mol·L-1的NaOH标准溶液滴定过量的盐酸,达到滴定终点时,消耗V2mLNaOH标准溶液。则:
①达到滴定终点的现象为________。
②产品中A1N的质量分数为________(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C8H8O3的芳香族化合物有多种不同的结构,这些物质在食品、化妆品等行业有广泛用途。
(1)C8H8O3的某一同分异构体尼泊金酯的结构简式如图。

① 下列对尼泊金酯的判断不正确的是______。
a.能发生水解反应
b.能与FeCl3溶液发生显色反应
c.分子中所有原子都在同一平面上
d.与浓溴水反应时,1 mol尼泊金酯消耗1 mol Br2
e.1 mol尼泊金酯与足量浓溴水反应后,使其有机产物与NaOH溶液反应,则最多消耗6 mol NaOH溶液。
② 尼泊金酯与NaOH溶液在一定条件下反应的化学方程式是____________________________,其中包含的反应类型有_________________、________________。
(2)C8H8O3的另一种同分异构体甲满足以下条件:① 与足量的NaOH溶液完全反应时,1 mol甲消耗3 molNaOH,② 遇FeCl3溶液显色,③ 苯环上的一氯取代物只有一种。
甲可能的结构简式是_______________、____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O32-+O2+4OH- = Fe3O4↓+S4O62-+2H2O。下列说法不正确的是
A. 参加反应的氧化剂与还原剂的物质的量之比为1∶5
B. 若有2 mol Fe2+被氧化,则被Fe2+还原的O2的物质的量为0.5 mol
C. 每生成1 mol Fe3O4,反应转移的电子为4 mol
D. O2是氧化剂,S2O32-与Fe2+是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】检测明矾样晶(含砷酸盐)中的砷含量是否超标,实验装置如下图所示(夹持装置已略去)。
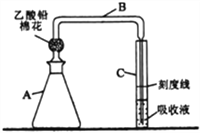
【实验1】配制砷标准溶液
①取0.132gAg2O3,用NaOH溶液完全溶解后,配制成1LNa3AsO3溶液(此溶液1mL相当于0.10mg砷);
②取一定量上述溶液,配制1L含砷量为1mg·L-1的砷标准溶液。
(1)步骤①中,必须使用的玻璃仪器除烧杯、玻璃棒外,还有__________。步骤②需取用步骤①中Na3AsO3溶液____mL。
【实验2】制备砷标准对照液
①往A瓶中加入2.00mL砷标准溶液,再依次加入一定量的盐酸、KI溶液和SnCl2溶液,混匀,室温放置10 min,使砷元素全部转化为H3AsO3。
②往A瓶中加入足量锌粒(含有ZnS杂质),立即塞上装有乙酸铅棉花的导气管B,并使B管右侧末端插入比色管C中银盐吸收液的液面下,控制反应温度25~40℃,45 min后,生成的砷化氢气体被完全吸收,Ag+被还原为红色胶态银。
③取出C管,向其中添加氯仿至刻度线,混匀,得到砷标准对照液。
(2)乙酸铅棉花的作用是_____________________。
(3)完成生成砷化氢反应的离子方程式:
____Zn+____H3AsO3+____H+=____( )+ ____Zn2++____( )________________
(4)控制A 瓶中反应温度的方法是________________________;反应中,A瓶有较多氢气产生,氢气除了搅拌作用外,还具有的作用是_____________________________。
(5)B管右侧末端导管口径不能过大(约为1mm),原因是__________________________。
【实验3】判断样品中砷含量是否超标
称取ag明矾样品替代【实验2】 ①中“2.00m砷标准溶液”,重复【实验2】后续操作。将实验所得液体与砷标准对照液比对,若所得液体的颜色浅,说明该样品含砷量未超标,反之则超标。
(6)国标规定砷限量为百万分之二(质量分数),则a的值为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙偶姻是一个极其重要的香料品种,主要用于配制奶香型、肉香型、草莓香型香精,也可用于合成其他精细化学品。已知乙偶姻中只含有C、H、O三种元素,其相对分子质量为88,分子中C、H、O原子个数比为2:4:1 。
请回答:
(1)乙偶姻的分子式为___________。
(2)X是乙偶姻的同分异构体,属于酯类,写出其结构简式(两种即可)_____________。
已知:
乙偶姻中含有碳氧双键。与乙偶姻有关的反应如下:

(3)写出反应①、②的反应类型:反应① ___________、反应② ___________。
(4)A的一氯代物只有一种。写出A、乙偶姻、C的结构简式:
A ___________________、乙偶姻 __________________、C_________________。
(5)写出D → E反应的化学方程式_____________________________________。
(6)设计实验方案。
I.检验F中的官能团______________________________________。
II.完成反应③的转化___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合硫酸铁( PFS)是一种高效的无机高分子絮凝剂。某工厂利用经浮选的硫铁矿烧渣(有效成分为Fe2O3和Fe3O4)制备PFS,其工艺流程如下图所示。
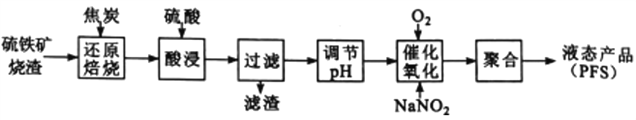
(1)“还原焙烧”过程中,CO还原Fe3O4生成FeO的热化学方程式为__ 。
已知: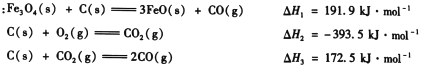
(2) CO是“还原焙烧”过程的主要还原剂。下图中,曲线表示4个化学反应a、b、c、d达到平衡时气相组成和温度的关系,I、Ⅱ、Ⅲ、Ⅳ分别是Fe2O3. Fe3O4. FeO、Fe稳定存在的区域。a属于____(填
“吸热反应”或“放热反应”);570℃时,d反应的平衡常数K=______。
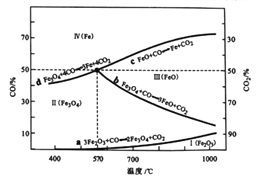
(3)工业上,“还原焙烧”的温度一般控制在800℃左右,温度不宜过高的理由是____。
(4)若“酸浸”时间过长,浸出液中Fe2+含量反而降低,主要原因是_____ 。
(5)已知![]() 若浸出液中
若浸出液中![]() ,为避免“催化氧化”过程中产生Fe(OH)3,应调节浸出液的pH≤___。
,为避免“催化氧化”过程中产生Fe(OH)3,应调节浸出液的pH≤___。
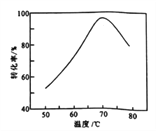
(6) FeS04溶液在空气中会缓慢氧化生成难溶的Fe(OH)SO4,该反应的离子方程式为____。“催化氧化”过程用NaNO2作催化剂(NO起实质上的催化作用)时,温度与Fe2+转化率的关系如右图所示(反应时间相同),Fe2+转化率随温度的升高先上升后下降的原因是 __。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物固氮是指( )
A.生物从土壤中吸收含氮养料
B.豆科植物根瘤菌将含氮化合物转变为植物蛋白质
C.将氨转变成硝酸及其它氮的化合物
D.生物将空气中的氮气转变成含氮化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com