
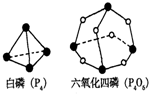
 ��ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̣���ѧ���ļ������γɣ����1mol��ѧ��ʱ�ͷţ������գ�����������֪���ף�P4����P4O6�ķ��ӽṹ��ͼ��ʾ�����ṩ���»�ѧ���ļ��ܣ�P-P 198KJ?mol-1��P-O 360kJ?mol-1��O=O 498kJ?mol-1�������1mol P4��3mol O2��ȫ��Ӧ��P4+3O2=P4O6������ЧӦ˵����ȷ���ǣ�������
��ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̣���ѧ���ļ������γɣ����1mol��ѧ��ʱ�ͷţ������գ�����������֪���ף�P4����P4O6�ķ��ӽṹ��ͼ��ʾ�����ṩ���»�ѧ���ļ��ܣ�P-P 198KJ?mol-1��P-O 360kJ?mol-1��O=O 498kJ?mol-1�������1mol P4��3mol O2��ȫ��Ӧ��P4+3O2=P4O6������ЧӦ˵����ȷ���ǣ�������| A���÷�Ӧ�����ȷ�Ӧ����������1638 kJ |
| B���÷�Ӧ�Ƿ��ȷ�Ӧ�ҷų�����1638 kJ |
| C���÷�Ӧ��Ӧ������ܵ��ڲ������� |
| D���÷�Ӧ��Ӧ��ļ���֮���ڲ������֮�� |


 ����ͼ���������������ϵ�д�
����ͼ���������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������һ�����ԣ��������������ͷ����� |
| B�������Ż������������������찲ȫ��� |
| C�����ࡢ�����ʡ���֬������Ȼ�߷��ӻ����� |
| D����֬�������ɵĸ�֬�������Ƿ�������Ч�ɷ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ͼ�����߷ֱ��ʾ��ͬ�¶��£�ѹǿΪP1��P2�����·������淴Ӧ��mX��g��+nY��g��?2Z��g��+W��s���Ĺ��̣�����˵������ȷ���ǣ�������
ͼ�����߷ֱ��ʾ��ͬ�¶��£�ѹǿΪP1��P2�����·������淴Ӧ��mX��g��+nY��g��?2Z��g��+W��s���Ĺ��̣�����˵������ȷ���ǣ�������| A��P1��P2 |
| B��m+n=2 |
| C��m+n=3 |
| D��P1��P2��ƽ�ⳣ����ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���������Ӹ������ |
| B�����ʵ������ |
| C������ԭ�Ӹ���֮��Ϊ5��1 |
| D�����֮��Ϊ2��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����������з���Ҫ�ϸ�ִ�й���ͳһ�ı� |
| B�����������з������ҪĿ���DZ��������Ĵ�� |
| C�����Ƿ�ֽ�����Թ�Ϊֽ���������л��� |
| D��ѧ���ڿ������ù��ķ�ֽ���Ի����������л������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢� | B���ۢ� | C���ܢ� | D���ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������ڷ����� |
| B�������ڿ�����ȼ�� |
| C������ʹKMnO4������Һ��ɫ |
| D�����ܷ���ȡ����Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��3c-a-b |
| B��a+b-3c |
| C��a+3b-2c |
| D��a+3b-6c |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
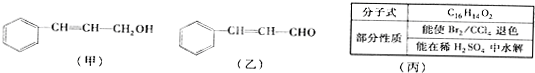
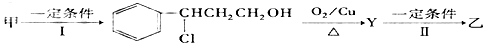
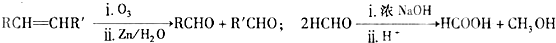
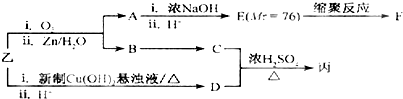
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com