
【题目】反应2SO2(g) + O2(g) ![]() 2SO3(g) ΔH = a kJ/mol,能量变化如图所示。下列说法中,不正确的是( )
2SO3(g) ΔH = a kJ/mol,能量变化如图所示。下列说法中,不正确的是( )
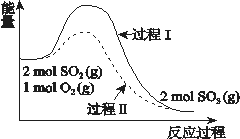
A. 2SO2(g) + O2(g) ![]() 2SO3(l) ΔH > a kJ/mol
2SO3(l) ΔH > a kJ/mol
B. 过程II可能使用了催化剂,使用催化剂不可以提高SO2的平衡转化率
C. 反应物断键吸收能量之和小于生成物成键释放能量之和
D. 将2molSO2(g) 和1mol O2(g)置于一密闭容器中充分反应后放出或吸收的热量小于┃a┃ kJ
 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:
【题目】已知反应:
(1)该反应的生成物中含有的官能团的名称是_______________,只含该官能团的物质在一定条件下不能发生的反应有_________(填序号);
①加成反应 ②酯化反应 ③氧化反应 ④还原反应
(2)已知HCHO分子中所有原子都在同一平面内,若要使![]() 分子中所有原子可能都在同一平面内,
分子中所有原子可能都在同一平面内,![]() 不能是_________(填序号);
不能是_________(填序号);
①![]() ②
②![]() ③
③![]()
(3)某氯代烃A的分子式为![]() ,它可以发生如下转化:
,它可以发生如下转化:

结构分析表明E分子中含有两个甲基且没有支链。
①A、C的结构简式分别为:A_______________,C_______________;
②写出下列转化的反应方程式:A→B:__________________,D→E:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe3O4中含有Fe2+、Fe3+,分别表示为 Fe(Ⅱ)、Fe(Ⅲ),以Fe3O4/Pd为催化材料,可实现用 H2消除酸性废水中的致癌物 NO2-,其反应过程示意图如图所示,下列说法不正确的是
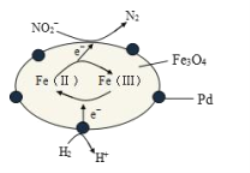
A.用该法处理后水体的 pH降低
B.Fe(Ⅱ)与 Fe(Ⅲ)的相互转化起到了传递电子的作用
C.反应过程中NO2-被 Fe(Ⅱ)还原为 N2
D.Pd 上发生的电极反应为:H2- 2e-== 2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知镁能分别与O2、N2、CO2反应,反应的化学方程式分别是 2Mg+O2![]() 2MgO、3Mg+N2
2MgO、3Mg+N2![]() Mg3N2、2Mg+CO2
Mg3N2、2Mg+CO2![]() 2MgO+C。把等质量的金属镁分别放在:①足量纯氧气中;②足量二氧化碳气体中;③足量空气中,完全燃烧后,得到的固体物质的质量分别对应的是W1g、W2g和W3g。以下三者的关系正确的是( )
2MgO+C。把等质量的金属镁分别放在:①足量纯氧气中;②足量二氧化碳气体中;③足量空气中,完全燃烧后,得到的固体物质的质量分别对应的是W1g、W2g和W3g。以下三者的关系正确的是( )
A.W1>W2>W3B.W3=W1>W2C.W3>W2>W1D.W2>W1>W3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的1/10。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式。
正极:____________;负极:________。
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用下图所示甲的方案,其中焊接在铁闸门的固体材料R可以采用___。
A、铜 B、钠 C、锌 D、石墨
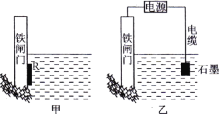
(3)上图中乙方案也可降低铁闸门腐蚀速率,其中铁闸门应该连接在直流电源的________极。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A. 达到化学平衡时4v正(O2)=5v逆(NO)
B. 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C. 达到化学平衡时,若增大容器容积,则正反应速率减小,逆反应速率增大
D. 化学反应速率关系:2v正(NH3)=3v正(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某密闭容器中充入NO2,发生反应2NO2(g)![]() N2O4(g)。其它条件相同时,不同温度下平衡体系中各物质的物质的量分数如下表:(已知:N2O4为无色气体)
N2O4(g)。其它条件相同时,不同温度下平衡体系中各物质的物质的量分数如下表:(已知:N2O4为无色气体)
t/℃ | 27 | 35 | 49 | 70 |
NO2% | 20 | 25 | 40 | 66 |
N2O4% | 80 | 75 | 60 | 34 |
下列说法不正确的是( )
A.27℃,该平衡体系中的NO2转化率为![]()
B.平衡时,NO2的消耗速率为N2O4消耗速率的2 倍
C.室温时,将盛有NO2的密闭玻璃球放入冰水中其颜色会变浅
D.其他条件不变,增大NO2起始量,平衡正移,该反应的化学平衡常数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设氯原子的质量为ag,12C原子的质量为bg,用NA表示阿伏加德罗常数的值,则下列说法不正确的是( )
A.该氯原子的相对原子质量为![]() B.mg该氯原子的物质的量为
B.mg该氯原子的物质的量为![]() mol
mol
C.该氯原子的摩尔质量是aNAgD.ng该氯原子所含的电子数是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值。俗名为“臭碱”的硫化钠广泛应用于治金、染料 、皮革 、电镀等工业。硫化钠的一种制备方法是Na2SO4+2C ![]() Na2S+2CO2↑。下列有关说法正确的是
Na2S+2CO2↑。下列有关说法正确的是
A.2L0.5mol/L Na2SO4 溶液中含有的氧原子数目为4NA
B.1 L0.1mo/L Na2S溶液中含有的阴离子数目小于0.1NA
C.生成 0.25mol还原产物时转移电子数为2NA
D.通常状况下11.2LCO2中含有的共价键数目为 2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com