
【题目】下列措施对增大反应速率有效的是:
A. Fe与稀硫酸反应制取H2时,改用浓硫酸
B. Na与水反应时增大水的用量
C. 在K2SO4与BaCl2两溶液反应时,增大压强
D. 密闭容器中进行的反应:C+O2![]() CO2,增大压强
CO2,增大压强
 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:
【题目】金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用。完成下列填空:
(1)镓(Ga)与铝同族,写出镓的氯化物和氨水反应的化学方程式____________。
(2)硅与铝同周期,SiO2是硅酸盐玻璃 (Na2CaSi6O14)的主要成分,Na2CaSi6O14也可写成Na2O·CaO·6SiO2。盛放NaOH溶液的试剂瓶若用玻璃瓶塞容易形成粘性的硅酸盐而无法打开,发生反应的化学方程式____________________________________________。长石是铝硅酸盐,不同类长石其氧原子的物质的量分数相同,由钠长石化学式NaAlSi3O8可推知钙长石的化学式为_______________________。
(3)用铝和金属氧化物反应制备金属单质是工业上较常用的方法 如:2Al+4BaO![]() 3Ba↑+BaO·Al2O3,常温下Al的金属性比Ba的金属性______(选填“强”“弱”)。利用上述方法可制取Ba的主要原因是________。
3Ba↑+BaO·Al2O3,常温下Al的金属性比Ba的金属性______(选填“强”“弱”)。利用上述方法可制取Ba的主要原因是________。
A.高温时Al的活泼性大于Ba B.高温有利于BaO分解
C.高温时BaO·Al2O3比Al2O3稳定 D.Ba的沸点比Al的低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用硼镁泥为原料制取MgSO4·7H2O粗产品的过程如下:
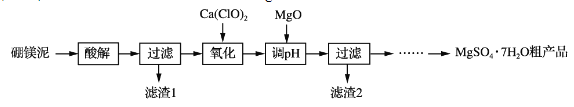
硼镁泥的主要成分如下表:
MgO | SiO2 | FeO、Fe2O3 | CaO | Al2O3 | B2O3 |
30%~40% | 20%~25% | 5%~15% | 2%~3% | 1%~2% | 1%~2% |
(1)“酸解”时为提高Mg2+的浸出率,可采用的措施是_____(写一种)。所加酸不宜过量太多的原因是_____。
(2)“氧化”步骤中,若用H2O2代替Ca(ClO)2,则发生反应的离子方程式为______________。实际未使用H2O2,除H2O2成本高外,还可能的原因是______________________________________。
(3)“调pH”时用MgO而不用NaOH溶液的原因是________________________。
(4)结合附表信息,由MgSO4·7H2O粗产品(含少量CaSO4)提纯获取MgSO4·7H2O的实验方案如下:将粗产品溶于水,_________________________________________________,室温下自然挥发干燥。(实验中必须使用的试剂有:饱和MgSO4溶液,乙醇)附:两种盐的溶解度(g/100 g水)
温度℃ | 10 | 30 | 40 | 50 |
CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 |
MgSO4·7H2O | 30.9 | 35.5 | 40.8 | 45.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前20号元素W、X、Y、Z的原子序数依次增大,且分列四个不同周期和四个不同主族。其中A为Y元素组成的单质;甲、乙、丙、丁、戊为上述四种元素组成的二元或三元化合物;常温下乙为液体。下列说法正确的是

A. 简单离子半径:Z>Y
B. 反应①为吸热反应
C. 反应②为工业上制备漂白粉的反应原理
D. X、Y分别与Z形成的化合物中,化学键类型一定相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知电导率越大导电能力越强。常温下用0.100 mol·L-1NaOH溶液分别滴定10.00mL浓度均为0.100 mol·L-1的盐酸和醋酸溶液,测得滴定过程中溶液的电导率如图所示。下列说法正确的是
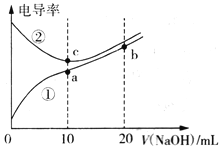
A. 曲线①代表滴定盐酸的曲线
B. a点溶液中: c(OH-)+c(CH3COO-)-c(H+) =0.1 mol/L
C. a、b、c三点溶液中水的电离程度:c>a>b
D. b点溶液中:c(OH-)>c(H+)+c(CH3COO-)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中只含有下列四种离子Fe3+、SO42-、Cl-和M离子,经测定Fe3+、SO42-、Cl-和M离子的物质的量之比为2:4:4:3,则M离子可能是下列中的( )
A.Mg2+B.CO32-C.Ba2+D.Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向200mL 6mol·L-1盐酸中加入一定量的纯净CaCO3,产生气体的体积随时间的变化曲线如图所示(气体体积均在标准 状况下测定)。
请回答下列问题:
(1)设OE段的反应速率为v1,EF段的反应速率为v2,FG段的反应速率为v3,则v1、v2、v3从大到小的顺序为________。
(2)为了减缓上述反应的速率,欲向该溶液中加入下列物质,你认为可行的是______(填字母)。
A.蒸馏水 B.氯化钾固体 C.氯化钠溶液 D.浓盐酸
(3)加入CaCO3的质量为 ______。
(4)若反应过程中溶液体积的变化忽略不计,则EF段用盐酸表示的化学反应速率v(HCl)=___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一支25mL的酸式滴定管中盛入0.1mol/L的HCl溶液,其液面恰好在5mL刻度处,若把滴定管中的溶液全部放入烧杯中,则HCl溶液的体积是
A.大于20mLB.小于20mLC.等于20mLD.等于5mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com