
【题目】已知红热的铁能与水蒸气反应生成氢气。现用如图所示装置进行铁在高温下与水蒸气反应的实验,并用简单的方法收集、检验生成的氢气。请回答下列问题。
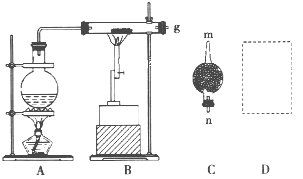
(1)写出铁在高温下与水蒸气反应的化学方程式:____________________________。
(2)干燥管C中盛放的药品是__________,干燥管的_______(填“m”或“n”)端与g导管相连接。
(3)在D处画出用试管收集氢气的装置图(所需其他仪器自行选择)。______________
(4)怎样用简单的方法检验收集到的气体是氢气?简述实验操作步骤和现象:______________。
(5)若收集到标准状况下的![]() 22.4L,则参加反应的铁粉的质量为__________g。
22.4L,则参加反应的铁粉的质量为__________g。
【答案】3Fe+4H2O(g) ![]() Fe3O4+4H2 CaCl2或CaO和NaOH n
Fe3O4+4H2 CaCl2或CaO和NaOH n  试管口向下,用拇指堵住试管口,靠近火焰,松开拇指,能燃烧或发出爆鸣声,说明收集的气体是氢气 42
试管口向下,用拇指堵住试管口,靠近火焰,松开拇指,能燃烧或发出爆鸣声,说明收集的气体是氢气 42
【解析】
(1)在高温条件下水蒸气与铁反应生成Fe3O4和H2;
(2)在高温条件下与铁反应,反应后用干燥管除去多余的水蒸气,所以干燥管C内盛放的药品是固体干燥剂CaCl2和CaO;
(3)由于产生的氢气密度比空气轻,所以收集时要用向下排空气法;
(4)可以用点燃法检验收集到的气体是否是氢气;
(5)根据反应3Fe+4H2O(g) ![]() Fe3O4+4H2计算。
Fe3O4+4H2计算。
(1)根据题目中提供的图可以看出本题实验的原理是前面烧瓶中产生水蒸气,经过横放的硬质玻璃管,在高温条件下与铁反应,反应后用干燥管除去多余的水蒸气,发生的反应为:3Fe+4H2O(g) ![]() Fe3O4+4H2;
Fe3O4+4H2;
(2)在高温条件下与铁反应,反应后用干燥管除去多余的水蒸气,所以干燥管C内盛放的药品是固体干燥剂CaCl2或CaO和NaOH,干燥管的n端与g导管相连接;
故答案为:CaCl2或CaO和NaOH;n;
(3)由于产生的氢气密度比空气轻,所以收集时要用向下排空气法,则收集氢气的装置图 ;
;
(4)可以用点燃法检验收集到的气体是否是氢气.具体做法是试管口向下,用拇指堵住试管口,靠近火焰,松开拇指,能燃烧或发出爆鸣声,说明收集的气体是氢气;
(5)根据反应3Fe+4H2O(g) ![]() Fe3O4+4H2可知,若收集到标准状况下的
Fe3O4+4H2可知,若收集到标准状况下的![]() 22.4L,则参加反应的铁粉的质量为
22.4L,则参加反应的铁粉的质量为![]() ×56g/mol=42g。
×56g/mol=42g。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:

(1)步骤③的实验操作名称是______。
(2)为检验提取碘后的水溶液中是否还含有单质碘,可选择的试剂是:_____。
(3)步骤④反应中能生成可溶性的Mn2+,写出该反应的离子方程式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为测定Na2CO3固体(含少量NaCl)的纯度,设计如下装置(含试剂)进行实验。
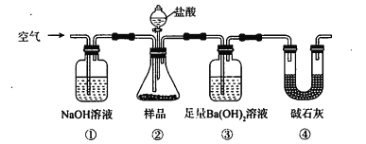
下列说法不正确的是
A. 必须在②③间添加吸收HCl的装置
B. ④的作用是防止空气中的气体影响实验的精确度
C. 通入空气的作用是保证②中产生的气体完全转移到③中
D. 称取样品和③中产生的沉淀的质量即可求算Na2CO3固体的纯度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了研究碳酸钙与盐酸反应的反应速率,某同学通过实验测定反应中生成的CO2气体体积,并绘制出如图所示的曲线。请回答以下问题。
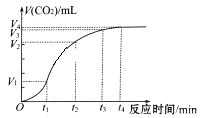
(1)化学反应速率最快的时间段是_________,原因是________________。
A.0~t1 B.t1-t2 C. t2~t3 D.t3~t4
(2)为了减缓上述反应速率,欲向盐酸溶液中加入下列物质,你认为可行的有_________。
A.蒸馏水 B.NaCl固体
C.NaCl溶液 D.通入HCl
(3)若盐酸溶液的体积是20mL,图中CO2的体积是标准状况下的体积,则t1~t2时间段平均反应速率v(HCl)=________________mol·L-1·min-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
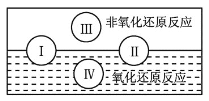
(1)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”可用如图表达。试写出有水参加的符合反应类型Ⅳ的一个化学方程式:_______,其中水为________剂。
(2)氯化铵常用作焊接。如:在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为:
____CuO+____NH4Cl ![]() ____Cu+____CuCl2+____N2↑+____H2O
____Cu+____CuCl2+____N2↑+____H2O
①配平此氧化还原反应方程式。
②该反应中,被氧化的元素是______(填元素名称),氧化剂是______(填化学式)。
③反应中若产生0.2mol的气体,则有________mol的电子转移。
(3)写出下列反应的离子方程式。
①NaHCO3溶于醋酸:____________________
②过量CO2与NaOH溶液反应:____________________
③Al(OH)3溶于NaOH溶液中:___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是( )

A. 微生物促进了反应中电子的转移
B. 正极反应中有CO2生成
C. 质子通过交换膜从负极区移向正极区
D. 电池总反应为C6H12O6+6O2===6CO2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)常温下,有pH相同、体积相同的①盐酸和②醋酸两种溶液,采取以下措施:
①加适量醋酸钠晶体后,两溶液中的c(H+)变化是醋酸溶液中c(H+)___(填“增大”、“减小”或“不变”),盐酸溶液中c(H+)___(填“增大”、“减小”或“不变”)。
②加水稀释10倍后,醋酸溶液中的c(H+)___盐酸溶液中的c(H+)(填“>”、“=”或“<”)。
③加等浓度的NaOH溶液至恰好中和,所需NaOH溶液的体积:醋酸___盐酸(填“>”、“=”或“<”)。
④使温度都升高20℃,溶液中c(H+):醋酸___盐酸(填“>”、“=”或“<”)。
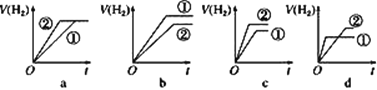
⑤分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是___(填字母)。
(2)将0.1mol·L-1的CH3COOH加水稀释,有关稀释后醋酸溶液的说法中,正确的是___(填字母)。
a.电离程度增大 b.溶液中离子总数增多
c.溶液导电性增强 d.溶液中醋酸分子增多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将2mol A和2mol B两种气体混合于2L密闭容器中,发生反应3A(g)+B(g)xC(g)+2D(g),2min末反应达到平衡状态,生成0.8mol D,并测得C的浓度为0.4mol/L。由此推断:
(1)x值等于______________
(2)B的平衡浓度为_____________
(3)A的转化率为____________
(4)生成D的反应速率______________
(5)如果增大反应体系的压强,则平衡体系中C的质量分数____________(填“增大”或“减小”或“不变”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com