
【题目】为了研究碳酸钙与盐酸反应的反应速率,某同学通过实验测定反应中生成的CO2气体体积,并绘制出如图所示的曲线。请回答以下问题。
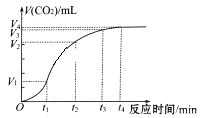
(1)化学反应速率最快的时间段是_________,原因是________________。
A.0~t1 B.t1-t2 C. t2~t3 D.t3~t4
(2)为了减缓上述反应速率,欲向盐酸溶液中加入下列物质,你认为可行的有_________。
A.蒸馏水 B.NaCl固体
C.NaCl溶液 D.通入HCl
(3)若盐酸溶液的体积是20mL,图中CO2的体积是标准状况下的体积,则t1~t2时间段平均反应速率v(HCl)=________________mol·L-1·min-1。
【答案】B 反应放热 AC (V2-V1)/[224x(t2-t1)]
【解析】
(1)从图中可以看出,化学反应速率最快的时间段是.t1-t2。答案为:.B
因为随着反应的进行,c(H+)不断减小,如果影响反应速率的因素只有c(H+),则反应速率应不断减慢,但.t1-t2段反应速率加快,说明还有其它因素影响反应速率,只能是温度,从而说明反应放热。,答案为:反应放热
(2)A.蒸馏水,稀释溶液,使c(H+)减小,反应速率减慢,A符合题意;
B.NaCl固体,不影响c(H+),溶液的温度也没有变化,所以对反应速率不产生影响,B不符合题意;
C.NaCl溶液,相当于加水稀释,c(H+)减小,反应速率减慢,C不合题意;
D.通入HCl,增大c(H+),加快反应速率,符合题意。
故选AC。
(3)若盐酸溶液的体积是20mL,图中CO2的体积是标准状况下的体积,则t1~t2时间段平均反应速率v(HCl)=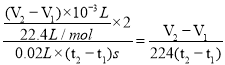 mol·L-1·min-1。
mol·L-1·min-1。
答案为:![]()


科目:高中化学 来源: 题型:
【题目】工业上,向500~600 ℃的铁屑中通入氯气生产无水氯化铁。现用如图所示的装置模拟上述过程进行实验。
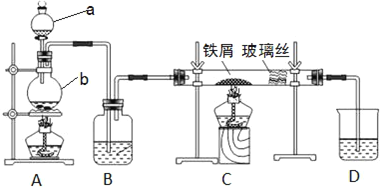
(1)写出仪器的名称:a_______,b________。
(2)A中反应的化学方程式为________。C中反应的化学方程式为________。
(3)装置B中加入的试剂是________。
(4)已知:向热铁屑中通入氯化氢气体可以生产无水氯化亚铁。为防止有杂质FeCl2生成,可在装置__和__(填字母)间增加一个盛有________的洗气瓶。
(5)装置D的作用是________。为防止水蒸气影响无水氯化铁的制取,请你提出一个对装置D的改进方案:________。
(6)反应结束后,取少量装置C中的固体于试管中,加入足量盐酸,固体完全溶解,得到溶液X。证明溶液X中含有FeCl3的试剂是________,观察到的现象是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金合欢醇广泛应用于多种香型的香精中,其结构简式如图所示。下列说法不正确的是( )

A.金合欢醇的同分异构体中不可能有芳香烃类
B.金合欢醇可发生加成反应、取代反应、氧化反应
C.金合欢醇分子的分子式为C15H26O
D.1 mol金合欢醇与足量Na反应生成0.5 mal氢气,与足量NaHCO3溶液反应生成1 mol CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压下,将0. 3 mol CO2通入盛有23.4 gNa2O2的容器中,一段时间后排出气体,所得固体的质量为29. 0 g,则参加反应的CO2的物质的量与产物Na2CO3的质量分别为( )
A.0. 3 mol 29. 0 gB.0. 3 mol 21. 2 g
C.0. 2 mol 21. 2 gD.0. 2 mol 29. 0 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2CO3溶液中存在水解平衡:CO32-+H2O ![]() HCO3-+OH-。下列说法错误的是
HCO3-+OH-。下列说法错误的是
A.加水稀释,溶液中所有离子的浓度都减小
B.通入CO2,溶液pH增大
C.加入NaOH固体,c(HCO3-)/c(CO32-)减小
D.升高温度,平衡常数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知红热的铁能与水蒸气反应生成氢气。现用如图所示装置进行铁在高温下与水蒸气反应的实验,并用简单的方法收集、检验生成的氢气。请回答下列问题。
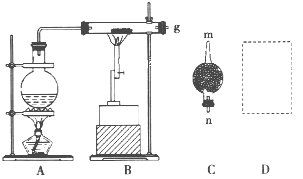
(1)写出铁在高温下与水蒸气反应的化学方程式:____________________________。
(2)干燥管C中盛放的药品是__________,干燥管的_______(填“m”或“n”)端与g导管相连接。
(3)在D处画出用试管收集氢气的装置图(所需其他仪器自行选择)。______________
(4)怎样用简单的方法检验收集到的气体是氢气?简述实验操作步骤和现象:______________。
(5)若收集到标准状况下的![]() 22.4L,则参加反应的铁粉的质量为__________g。
22.4L,则参加反应的铁粉的质量为__________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸乙酯(无色液体,难溶于水,沸点213℃)天然存在于桃、菠萝、红茶中,稍有水果气味,常用于配制香精和人造精油,也可用作食品添加剂。实验室利用如图所示装置,在环己烷中通过反应 制备。已知:环己烷沸点为80.8℃,可与乙醇和水形成共沸物,其混合物沸点为62.1℃。下列说法错误的是( )
制备。已知:环己烷沸点为80.8℃,可与乙醇和水形成共沸物,其混合物沸点为62.1℃。下列说法错误的是( )

A.实验时最好采用水浴加热,且冷却水应从b口流出
B.分水器可及时放出水层,避免水层升高流入烧瓶
C.环己烷的作用是在较低温度下带出生成的水,促进酯化反应向右进行
D.实验时应依次向圆底烧瓶中加入碎瓷片、浓硫酸、苯甲酸、无水乙醇、环己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,分别稀释![]() 的
的![]() 溶液和氨水,溶液pH的变化如下图所示。
溶液和氨水,溶液pH的变化如下图所示。
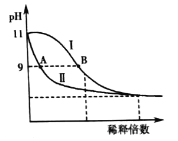
已知:![]() 。下列说法正确的是( )
。下列说法正确的是( )
A.若35℃时分别稀释上述两种溶液,则图中Ⅰ、Ⅱ曲线将比原来靠近
B.保持25℃不变,取A、B两点对应的溶液等体积混合后,![]()
C.由水电离产生的![]() :A点>B点
:A点>B点
D.曲线Ⅰ上任意点对应的溶液中,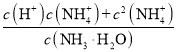
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某硫酸铝和硫酸镁的混合液中,c(Mg2+)=2mol/L,c(S042-)=6.5mol/L,若将100 mL的此混合液中的Mg2+和Al3+分离,至少应加入1.6mol/L的氢氧化钠溶液 ( )
A.1.0LB.0.5 LC.1.8LD.2L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com