
【题目】滴有酚酞的Ba(OH)2溶液显红色,在上述溶液中分别滴加X溶液后有下列现象。下列说法不正确的是
序号 | 装置 | X溶液 | 现象 |
I |
| 盐酸 | 溶液红色褪去,无沉淀,灯泡亮度没有明显变化 |
II | Na2SO4 | 溶液红色不变,有白色沉淀生成,灯泡亮度没有明显变化 | |
III | H2SO4 | 溶液红色褪去,有白色沉淀生成,灯泡逐渐变暗 |
A. 实验I中溶液红色褪去,说明发生了反应H+ + OH- =H2O
B. 实验II中溶液红色不变,且灯泡亮度没有明显变化,说明溶液中依然存在有大量的Na+与OH-
C. 实验III中溶液红色褪去,有白色沉淀生成,灯泡逐渐变暗,说明发生了反应Ba2+ + 2OH- + 2H+ + SO42- == BaSO4↓+ 2H2O
D. 将实验II中Na2SO4溶液换成CuSO4溶液,现象与原实验II中的现象相同
【答案】D
【解析】
A. 显红色的酚酞,Ba(OH)2溶液显碱性,滴加盐酸,发生酸碱中和反应:H+ + OH- =H2O溶液红色褪去,故A不符合题意;
B. Ba(OH)2 与Na2SO4发生复分解反应:Ba(OH)2 +Na2SO4= BaSO4↓ + 2NaOH,溶液中依然存在有大量的Na+与OH-,故B不符合题意;
C. H2SO4 与Ba(OH)2发生复分解反应:Ba2+ + 2OH- + 2H+ + SO42- == BaSO4↓+ 2H2O,溶液中离子浓度减小,灯泡变暗,氢氧根浓度逐渐减小,红色逐渐褪去,故C不符合题意;
D. CuSO4 与Ba(OH)2发生复分解反应:Ba(OH)2 +CuSO4= BaSO4↓ + Cu(OH)2 ↓,溶液中离子浓度逐渐减小,灯泡逐渐变暗,氢氧根浓度逐渐减小,红色逐渐褪去,与Na2SO4的实验现象不同,故D符合题意;
综上所述,本题应选D。


科目:高中化学 来源: 题型:
【题目】氯化亚砜(SOCl2)在农药、制药行业中用途广泛,沸点为77℃,遇水剧烈反应,液面上产生白雾,并产生带有刺激性气味的气体。实验室用干燥的Cl2与SO2合成SOCl2,反应原理是:SO2+Cl2+SCl2==2SOCl2。回答以下问题:
(1)氯气的制备
氯气的制备可选择下列装置完成:

①制取氯气的发生装置可以选择上图中的______,反应的化学方程式________________________。
②预收集一瓶干燥纯净的氯气,选择上图中的装置,其连接顺序为:_____________。(按气流方向,用小写字母表示)。
(2)二氧化硫的制备
按下图提供的装置、试剂,制取SO2反应的化学方程式为___________________________。

(3)氯化亚砜的制备
在仪器I中Cl2与SO2反应成合SOCl2
①仪器J的名称是________,冷凝水入口是_____,装置K的作用是____________________________________________________________。
②本实验的主要副产物是SCl2,已知:SOCl2沸点为77℃,SCl2的沸点为50℃,提纯SOCl2的实验操作是____________;
(4)氯化亚砜的性质与检测
某同学认为,SOCl2与水反应后的溶液中有盐酸和亚硫酸生成。
欲证明反应后形成的溶液中有H2SO3,可以使用的试剂是_________________。
欲证明反应后形成的溶液中有Cl-,实验的操作方法是__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列方程式的书写及配平。
(1) _____NaBO2+____SiO2+____Na+____H2=____NaBH4+____Na2SiO3;________
(2) _____P+____FeO+_____CaO ![]() _____Ca3(PO4)2+____Fe;________
_____Ca3(PO4)2+____Fe;________
(3) _____P4+_____KOH+_____H2O=_____K3PO4+_____PH3;________
(4) _____BiO3-+_____Mn2++_______=_____Bi3++_____ MnO4-+________;_______。
(5)向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为_________________。
(6)烟气中含有SO2和NO,写出用NaClO2溶液将烟气中NO转化成NO3-的离子方程式:________________。
(7)一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中BH4- (B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和B(OH)4-,其离子方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是

A. 图甲表示某吸热反应在无催化剂(a)和有催化剂(b)时反应的能量变化
B. 图乙表示常温下,0.1mol/LNaOH溶液滴定20.00mL0.1mol/L醋酸溶液的滴定曲线
C. 图丙表示某可逆反应的反应速率随时间的变化关系,t0时刻改变的条件是使用了催化剂
D. 图丁表示一定质量冰醋酸加水稀释过程中、溶液导电能力变化曲线,且醋酸电离程度:a<b<c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂电池的构造如图所示,电池内部“→”表示放电时Li+的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC6 ![]() LiCoO2+6C,下列说法错误的是( )
LiCoO2+6C,下列说法错误的是( )
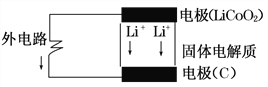
A. 该电池的负极为LiCoO2
B. 充电时Li+向C电极电极移动
C. 充电时的阴极反应:Li1-xCoO2+xLi++xe-===LiCoO2
D. 外电路上的“→”表示放电时的电子流向
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿(主要成分CuFeS2)是提取Cu的主要原料。
已知:2CuFeS2+4O2![]() Cu2S+3SO2+2FeO(Ⅰ)
Cu2S+3SO2+2FeO(Ⅰ)
产物Cu2S在1200 ℃高温下继续反应:2Cu2S+3O2==2Cu2O+2SO2 (Ⅱ)
2Cu2O+Cu2S==6Cu +SO2↑ (Ⅲ)
假定各步反应都完全。则下列说法正确的是
A. 反应Ⅰ中CuFeS2仅作还原剂
B. 取12.5g黄铜矿样品,经测定含3.60g硫,则矿样中CuFeS2质量分数一定为82.8%
C. 由6molCuFeS2生成6molCu消耗O2的物质的量为14.25mol
D. 6molCuFeS2和15.75molO2反应,理论上可得到铜的物质的量为3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol·L-1的溶液。在FeCl2溶液中需加入少量铁屑,其目的是___________。
(2)甲组同学取2 mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为____________。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mL FeCl2溶液中先加入0.5 mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是_____。
(4)丙组同学取10 mL 0.1 mol·L-1 KI溶液,加入6 mL 0.1 mol·L-1 FeCl3溶液混合。分别取2 mL 此溶液于3支试管中进行如下实验:
①第一支试管中加入1 mL CCl4充分振荡、静置,CCl4层显紫色;
②第二支试管中加入1滴K3[Fe(CN)6]溶液,生成蓝色沉淀;
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是____(填离子符号);实验①和③说明:在I-过量的情况下,
溶液中仍含有___(填离子符号),由此可以证明该氧化还原反应为________。
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为___________________;一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生气泡的原因是_______________;生成沉淀的原因是__________________(用平衡移动原理解释)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2气体是一种优良的消毒剂,常用于自来水的消毒。已知:NaClO2饱和溶液在低于38℃时析出NaClO23H2O,高于38℃时析出NaClO2。
(1)工业上常将ClO2制备成NaClO2固体以便运输和贮存,流程如下:

①吸收器中,H2O2的作用是____。(填“氧化剂”或“还原剂”)。
②在吸收器反应时应控制温度低于5℃的原因是:____。
③操作a:55℃蒸发至有大量晶体析出、____、用介于38℃~60℃的温水洗涤、低于60℃干燥,得到NaClO2固体。
(2)将ClO2溶于水得到溶液,为测定其浓度,进行以下实验操作:
步骤1:取待测ClO2溶液20.00mL于锥形瓶中;
步骤2:用稀H2SO4调节溶液pH <2.0,加入足量的KI晶体充分反应;
步骤3:加入几滴淀粉溶液,逐滴加入0.1 mol· L-1的Na2S2O3溶液,恰好完全反应时,消耗Na2S2O3溶液20.00mL;
已知:2ClO2+10KI+4H2SO4=2KCl+5I2+4K2SO4+4H2O,I2+2Na2S2O3=Na2S4O6+2NaI,试计算溶液中ClO2的物质的量浓度(写出计算过程)。____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com