
【题目】用适量水稀释0.1mol/L氨水时,溶液中随着水量的增加而减小的是( )
A.c(OH﹣)
B.n(NH4+)
C.![]()
D.n(OH﹣)
【答案】A
【解析】解:A.稀释过程中一水合氨的电离程度增大,由于溶液体积变化更大,则氢氧根离子的浓度减小,故A正确;B.稀释过程中铵根离子、氢氧根离子的物质的量增大,故B错误;
C.稀释过程中氢氧根离子、铵根离子的物质的量增大,一水合氨的物质的量减小,由于溶液体积相同,则 ![]() 的比值会增大,故C错误;
的比值会增大,故C错误;
D.稀释过程中一水合氨的电离程度增大,溶液中氢氧根离子的物质的量增大,故D错误;
故选A.
【考点精析】本题主要考查了弱电解质在水溶液中的电离平衡的相关知识点,需要掌握当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理才能正确解答此题.


科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种短周期元素在周期表中的位置关系如图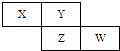
(1)Ⅰ若Z元素原子的最外层电子数是电子层数的2倍①W在周期表中的位置为 .
②Y和Z元素可组成的化合物的化学式为 .
③写出铜和X的最高价氧化物水化物的稀溶液反应的离子方程式为 .
④W最高价氧化物水化物的浓溶液不稳定,受热可分解,产物之一是黄绿色气体,且当有28mol电子转移时,共产生9mol气体,写出该反应的化学方程式 .
(2)Ⅱ若Y和Z的核外电子数之和为22①Y的气态氢化物电子式为 , 工业合成该物质的化学方程式为 .
②将X的最高价氧化物通入到苯酚钠溶液中,实验现象是 .
③X单质与W的最高价氧化物水化物的浓溶液反应,当电子转移0.4mol时,产生气体体积(标准状况下)是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分类是化学学习和研究的常用手段,下列关于物质分类的正确组合是( )
酸 | 碱 | 盐 | 氧化物 | |
A | HNO3 | NaOH | NaCl | H2O |
B | HCl | CaO | Na2CO3 | NH3 |
C | H2SO4 | Ba(OH)2 | CO2 | Na2O2 |
D | H3PO4 | KOH | Al(OH)3 | BaSO4 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素A和B的原子序数都小于18。已知A元素原子最外层电子数为a,次外层电子数为b;B元素原子的M层电子数是a-b,L层电子数是a+b,则A、B两元素所形成的化合物的晶体类型为
A.分子晶体B.原子晶体C.离子晶体D.金属晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组利用下列装置探究氯气与氨气的反应.其中A、B分别为氯气和氨气的发生装置,C为纯净干燥的氯气与氨气反应的装置.
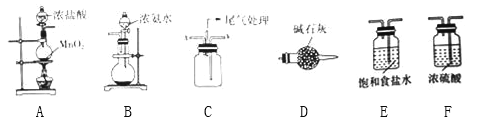
(1)若Cl2从左向右流动,NH3从右向左流动,则上述实验装置中,依次连接的合理顺序为:A→________________→B;为使NH3与Cl2更充分混合,Cl2应从C装置的__口进入(填“x”或“y”).
(2)简述装置A中使用分液漏斗向圆底烧瓶中滴加浓盐酸的操作是__________________.
(3)装置A中发生反应的离子方程式为_______________________________.
(4)装置B中圆底烧瓶内的试剂为______________(填名称).
(5)装置D的作用是____________________________.
(6)反应开始后,装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气中的主要成分之一,该反应的化学方程式为________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将在空气中暴露一段时间后的氢氧化钠固体样品溶于水得溶液A,将所得溶液中遂滴滴加稀硫酸至过量,生成的二氧化碳体积(标准状况下)与加入稀硫酸体积关系如图所示。
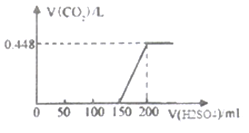
(1)溶液A中滴加硫酸的体积在0-150mL间无CO2气体生成的原因是(用化学方程式表示)_________________________________________________________;
(2)硫酸滴加至150mL时溶波中溶质主要成分为(写化学式)_______________;
(3)溶液A中碳酸钠的质量为____g;
(4)硫酸的物质的量浓度为______mol/L。
(5)该样品中Na2CO3与NaOH物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度时,N2与H2反应过程中能量变化的曲线如图.下列叙述正确的是( ) 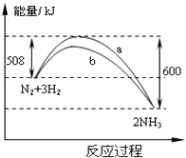
A.该反应的热化学方程式为:N2+3H22NH3△H=﹣92kJ/moL
B.b曲线是加入催化剂时的能量变化曲线
C.加入催化剂,该化学反应的放热增多
D.加入催化剂可增大正反应速率,降低逆反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度不同压强(P1<P2)下,可逆反应2X(g)2Y(g)+Z(g)中,生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是( )
A.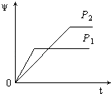
B.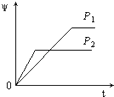
C.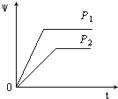
D.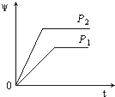
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com