
����Ŀ�����������һ�����Ϳɳ����,����ͨ������,�õ���ܽϳ�ʱ�䱣���ȶ��ķŵ��ѹ��������ص��ܷ�ӦΪ3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH����ش���������:
3Zn(OH)2+2Fe(OH)3+4KOH����ش���������:
(1)������صĸ���������____��
(2)�ŵ�ʱ,��������____(���������ԭ��)��Ӧ;��֪������ӦΪZn-2e-+2OH-====Zn(OH)2,��������ӦΪ_______________________��
(3)�ŵ�ʱ,____(���������)��������Һ�ļ�����ǿ��
���𰸡� Zn��п ��ԭ FeO42-+3e-+4H2O�TFe��OH��3+5OH- ��
��������������ԭ����и�������ʧȥ���ӵ�������Ӧ�����������õ����ӵĻ�ԭ��Ӧ�����ݸ�����ص��ܷ�Ӧ�жϻ�ԭ���������������ԭ���ԭ���������
��⣺��1�������ܷ�Ӧʽ��֪пʧȥ���ӣ�����������Ӧ�����Ը�����صĸ���������п��
��2���ŵ�ʱ,���������õ����ӵĻ�ԭ��Ӧ����֪������ӦΪ3Zn-6e-+6OH-��3Zn(OH)2���������ܷ�Ӧʽ��ȥ������Ӧʽ���ɵõ�������ӦΪFeO42-+3e-+4H2O��Fe��OH��3+5OH-��
��3���ŵ�ʱ������ӦΪFeO42-+3e-+4H2O��Fe��OH��3+5OH-����Ӧ�в�����������������Ũ��������������������Һ�ļ�����ǿ��


 ͬ����ϰǿ����չϵ�д�
ͬ����ϰǿ����չϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(NaNO2)����Ҫ�ķ�������ijʵ��С������ͼ��ʾ��װ�ú��Լ���ͨ����Ӧ�Ʊ��������� (���ּг�װ����)��
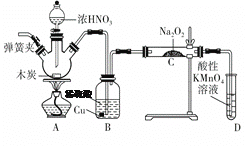
��֪�������£���2NO��Na2O2===2NaNO2��
�����������£�NO��NO2������MnO4-��Ӧ����NO3-��Mn2����
���������գ�
��1��д��A��������Ҫ�������������� __________ ��___________��_________��
��2��д��Ũ������ľ̿��Ӧ�Ļ�ѧ����ʽ��_______________________��
��3��B�й۲쵽����Ҫ����������ɫ���������______________��Dװ�õ�������___________________________��
��4��������C�����г�������������и�����̼���ƺ��������ƣ�Ϊ���������Щ��������Ӧ��B��Cװ�ü�����װ�ã����װ����ʢ�ŵ�ҩƷ������________��
��5����NO2����ȫ��ת����NO����1.56 g����������ȫת����Ϊ�������ƣ�������������Ҫľ̿________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾ��װ���У��۲쵽������ָ��ƫת��M����֣�N����ϸ������õ������Һ��������С���ɴ��ж��±�������M��N��P���ʣ����п��Գ������ǣ� ��
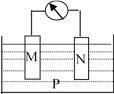
M | N | P | |
A | Zn | Cu | ϡ������Һ |
B | Cu | Fe | ϡ���� |
C | Ag | Zn | ��������Һ |
D | Zn | Fe | ����������Һ |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���10 mL 0.40 mol��L-1 H2O2��Һ�м�������FeCl3��Һ����ͬʱ�̲������O2�������������Ϊ��״�������±���ʾ��
t / min | 0 | 2 | 4 | 6 |
V(O2) / mL | 0 | 9.9 | 17.2 | 22.4 |
������ʾ����Ӧ���������У�
��2Fe3++ H2O2 ![]() 2Fe2++O2��+2H+
2Fe2++O2��+2H+
�� H2O2 + 2Fe2++2H+ ![]() 2H2O+2Fe3+
2H2O+2Fe3+
��Ӧ�����������仯����ͼ��ʾ������˵������ȷ����

A. 0��6 min��ƽ����Ӧ���ʣ�v(H2O2) = 3.33��10-2 mol��L-1��min-1
B. Fe3+�������Ǽӿ��������ķֽ�����
C. ��Ӧ�������ȷ�Ӧ����Ӧ���Ƿ��ȷ�Ӧ
D. ��Ӧ2H2O2(aq)![]() 2H2O(l) + O2(g)�ġ�H =E1-E2 < 0
2H2O(l) + O2(g)�ġ�H =E1-E2 < 0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ǧ���仯����㷺�������ء���е���졢���»�������ҵ��
��1��Ǧ��̼��ͬ��Ԫ�أ���̼��4�����Ӳ㡣Ǧ��Ԫ�����ڱ���λ��Ϊ_________��
��2��Ǧ������һ����;�㷺�Ķ��ε�ء�Ǧ���صĵ�ط�Ӧͨ����ʾ���£�Pb+PbO2+2H2SO4 ![]() 2PbSO4 +2H2O��
2PbSO4 +2H2O��
Ǧ���س��ʱ��������Ǧ�缫Ӧ����ӵ�Դ��_________________�����������������������������ӣ��õ缫�ĵ缫��ӦʽΪ________________________________��
��3�����õ�ⷨ���Ƶý���Ǧ����PbO�ܽ���HCl��NaCl�Ļ����Һ�У��õ���[PbC14]2-�ĵ��Һ���ö��Ե缫���Na2PbCl4��Һ�Ƶý���Pb��װ������ͼ��ʾ��
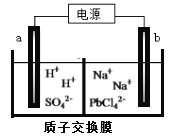
a�缫��������__________��b�缫�ĵ缫��ӦʽΪ______________________
��4��PbO2����ͨ��ʯīΪ�缫���Pb(NO3)2 ��Cu(NO3)2�Ļ����Һ��ȡ��������������Ӧ�ĵ缫��ӦʽΪ______________�������Ϲ۲쵽��������____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʱ��11��1���峿5ʱ58��07�룬�й�����������F��ң�����ػ���ھ�Ȫ���Ƿ����������˺��췢�䳡����䣬����ĵ�����ʹ�õ��ƽ�����Һ���Һ����
��֪������298Kʱ���Ȼ�ѧ����ʽ��
2H2(g)+O2(g)== 2H2O(l) ��H=-571.6 kJ��mol-1
CH4(g)+2O2(g)==CO2(g)+2H2O (l)��H=-890.3 kJ��mol-1
C(s)+O2(g)== CO2(g)��H=-393.5 kJ��mol-1
����������Ȼ�ѧ����ʽ����������⣺
��1��ͨ������˵����������H2��C��CH4��ȫȼ��ʱ�ų�����������_________��
��2���������Ϸ�Ӧ����C(s)+2H2(g)== CH4(g)���ʱ䦤H=________________��
��3����֪H2O(l)== H2O(g) ��H=+44.0 kJ��mol-1
��д������ȼ�����ɶ�����̼��ˮ�������Ȼ�ѧ����ʽ��________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ڰ��շ�����ȫ������������ڱ�����Ԫ�ص������Ϣ��ͼ��ʾ,�����й����˵���������
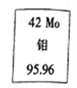
A. 95Moԭ�Ӻ�����53������ B. 95Moԭ�Ӻ�����42������
C. 92Mo��95Mo��98MoΪ��ͬ���� D. 92Mo��95Mo��98Mo�Ļ�ѧ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����к͵ζ����ⶨ�ռ�Ĵ��ȣ��ռ��е����ʲ����ᷴӦ���������ʵ��ش�
��1���������õ�8.8g�ռ���Ʒ���Ƴ�500mL����Һ�����ƹ���ʹ�õ���Ҫ������500mL����ƿ����Ͳ���ձ�����ͷ�ι��⣬����һ�ֱ���ʹ�õ������� ��
��2����ʽ�ζ�����ȡ10.00mL����Һ����ƿ�У����뼸�η�̪��
��3����0.20molL��1�ı�����ζ�����Һ���жϵζ��յ�������ǣ� ��
��4�����ʵ�������ȷ���ӵζ���ʼ����������Һ�е�����Ũ�ȹ�ϵ���Գ��ֵ����������ĸ��ţ�
A.c��Na+����c��Cl������c��H+����c��OH����
B.c��Na+����c��OH������c��Cl������c��H+��
C.c��Na+��+c��H+��=c��OH����+c��Cl����
D.c��Cl����+c��Na+����c��OH����+c��H+��
��5�������������ݼ��㣬c��NaOH�� mol/L
�ζ����� | ����Һ�����mL�� | �����������mL�� | |
�ζ�ǰ������mL�� | �ζ��������mL�� | ||
��һ�� | 10.00 | 0.60 | 20.50 |
�ڶ��� | 10.00 | 3.00 | 23.10 |
��6�������������֣�����ʵ��IJⶨ������ռ��ʵ�ʴ���ƫ�ߣ�������Ŀ���ԭ����
A.�ζ�ǰƽ�ӣ��ζ�����
B.δ�ñ�Һ��ϴ�ζ���
C.�ô���Һ��ϴ��ƿ
D.��С�Ľ���Һ������ƿ���森
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ժ��ܷϴ���(��Ҫ�ɷ�ΪCo��Fe��SiO2)Ϊԭ�ϣ���ȡ�����ܵ��������¡�
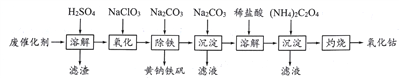
(1)�ܽ�:�ܽ����ˣ�������ϴ��2~3�Σ�ϴҺ����Һ�ϲ�����Ŀ����__________________��
(2)����:���Ƚ��������¼���NaC1O3����������_______________________________��
(3)����:����������Na2CO3������ȣ����ɻ�������Na2[Fe6(SO4)4(OH)12]������д���÷�Ӧ�Ļ�ѧ����ʽ:__________________________________________________��
(4)����:���ɳ�����ʽ̼����[(CoCO3)2��3Co(OH)2]��������ϴ�ӣ���������Ƿ�ϴ�Ӹɾ��IJ�����_________________________________________________________��
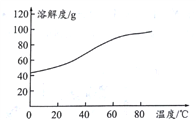
(5)�ܽ�:CoCl2���ܽ��������ͼ��ʾ�����ʽ̼�����м�������ϡ���ᣬ���ȱ߽�������ȫ�ܽ������ȹ��ˣ���ԭ����__________________________________��
(6)����:ȷ��ȡ����CoC2O4����2.205g���ڿ��������յõ��ܵ�һ��������1.205g��д����������Ļ�ѧʽ_________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com