
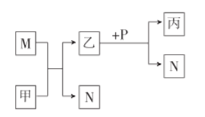
【题目】X、Y、Z、W是原子序数依次增大的短周期主族元素。甲、乙、丙是由这些元素组成的化合物,M、N、P是这些元素对应的单质,甲常温下为液态,丙中滴入盐酸开始有沉淀,继续沉淀消失,其溶液呈碱性。上述物质间的转化关系如图所示。下列说法错误的是( )
A.原子半径:Z>W>Y
B.X与Z形成的化合物能与水反应产生N
C.常温下,P不能与浓硝酸发生反应
D.Y分别与X、Z形成的化合物均不止一种
【答案】C
【解析】
甲常温下为液态,应为H2O,丙中滴入盐酸开始有沉淀,继续沉淀消失,其溶液呈碱性,可知丙为NaAlO2,由转化关系可知M为Na,N为H2,乙为NaOH,P为Al,由此可知X、Y、Z、W分别为H、O、Na、Al元素,据此分析解答。
由以上分析可知X、Y、Z、W分别为H、O、Na、Al元素。
A.原子核外电子层数越多,原子半径越大,同周期元素,从左到右,原子半径减小,则原子半径![]() ,即Z>W>Y,故A正确;
,即Z>W>Y,故A正确;
B.X与Z形成的化合物为NaH,具有还原性,可与水发生氧化还原反应,生成氢氧化钠和氢气,故B正确;
C.常温下,铝与浓硝酸发生钝化反应,钝化属于化学变化,故C错误;
D.氧元素可与氢、钠两元素分别形成过氧化氢、水,过氧化钠、氧化钠等化合物,形成的化合物均不止一种,故D正确;
故选C。


科目:高中化学 来源: 题型:
【题目】密闭容器中,反应aA(g)+bB(g)![]() cC(g)+dD(g)达平衡时,B的浓度为0.6mol/L,若保持温度不变,将容器的容积扩大到原来的3倍,达新平衡时B的浓度降为0.3mol/L.下列判断正确的是
cC(g)+dD(g)达平衡时,B的浓度为0.6mol/L,若保持温度不变,将容器的容积扩大到原来的3倍,达新平衡时B的浓度降为0.3mol/L.下列判断正确的是
A. a+b<c+d
B. 平衡向正反应方向移动
C. D的体积分数减小
D. 达到新平衡时,A、B的浓度减小,C、D浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解煤浆液的方法制H2的反应为C(s)+2H2O(l)=CO2(g)+2H2(g)。现将一定量的1mol/LH2SO4溶液和适量煤粉充分混合,制成含碳量为0.02g/mL~0.12g/mL的煤浆液,置于如图所示装置中进行电解(两电极均为惰性电极)。下列说法错误的是
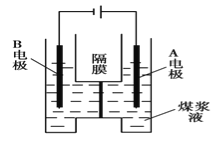
A. A极是阳极,B极为阴极
B. A极的电极反应式为C+2H2O-4e-=CO2↑+4H+
C. B极的电极反应式为2H++2e-=H2↑
D. 电解一段时间后,煤浆液的pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年的化学诺贝尔奖颁给了为锂电池研究作出贡献的三位科学家,其研究的是两种常见锂电池:一种是采用镍钴锰酸锂Li(NiCoMn)O2或镍钴铝酸锂为正极的“三元材料锂电池”;另一种是采用磷酸铁锂(LiFePO4)为正极的电池。请回答下列问题:
(1)利用FeSO4、(NH4)2HPO4、LiOH为原料以物质的量之比1∶1∶1反应生成LiFePO4,该化学反应方程式为________________。
(2)Mn位于元素周期表的_____区(填“s”或“p”或“d”或“ds”或“f”),基态钴原子的未成对电子数为______,1mol [CoCl (NH3)5] Cl2 中含σ键数目为__NA。
(3)磷元素可以形成多种含氧酸H3PO4、H3PO2、H3PO3、HPO3,这四种酸中酸性最强的是_____。PO43-的空间构型是___,中心原子的杂化方式是______。
(4)PH3是_____分子(填“极性”或“非极性”),其在水中的溶解性比NH3小,原因是______。
(5)硫化锂Li2S(摩尔质量Mgmol-1)的纳米晶体是开发先进锂电池的关键材料,硫化锂的晶体为反萤石结构,其晶胞结构如图。若硫化锂晶体的密度为ag·cm-3,则距离最近的两个S2-的距离是_______nm。(用含a、M、NA的计算式表示)
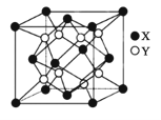
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究几种气态氧化物的性质,某同学设计了如图所示的一组实验:用三个集气瓶收集满SO2、NO2,然后分别倒置于盛有水的水槽中;分别缓慢通入适量O2或Cl2;一段时间后,装置A、B的集气瓶中充满溶液,装置C的集气瓶中还有气体剩余。
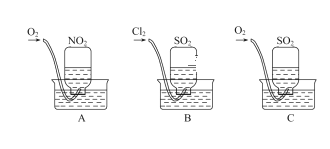
(1)实验前,在装置C的水槽里滴加几滴紫色石蕊溶液,观察到的现象_______________,通入氧气后,可观察到的现象是____________________________________,写出发生反应的总化学方程式:___________________________________。
(2)装置B中,溶液充满集气瓶后,在水槽里滴加适量的Ba(NO3)2溶液,写出有关反应的离子方程式:_______________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组为研究水垢的生成,查得CaCO3和Mg(OH)2溶解度曲线如图所示。已知:40°C时,Ksp(MgCO3)=7×10-6,下列有关分析错误的是( )
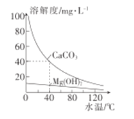
A.CaCO3、Mg(OH)2溶解均放热
B.MgCl2溶液中加入少量CaCO3粉末加热搅拌,有Mg(OH)2生成
C.含有Ca(HCO3)2和Mg(HCO3)2的自来水长时间加热,水垢的主要成分为CaCO3和MgCO3
D.40℃时,Ksp(CaCO3)=1.6×10-7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近期瑞士科学院研发出一种负载氧化铜的纳米晶粒的聚合物氮化碳二维纳米材料(类石墨相氮化碳),大幅度提高水分解的催化效率,将为实现氢能源大规模应用打下坚实的基础。回答下列问题:
(1)铜在周期表中的位置为___,其原子核外电子排布的最高能层符号为___。
(2)1989年A.Y.Liu和M.L.Cohen根据β-氮化硅的晶体结构,用C替换Si,从理论上预言了β-氮化碳这种硬度可以和金刚石相媲美的新共价化合物。
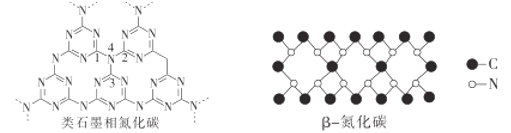
①石墨晶体可以一层层剥离开来,层间的作用力主要是___。
②类石墨相氮化碳中1、2、3、4共四个原子的空间构型为___;β-氮化碳中N的杂化类型是___。
③β-氮化碳的化学式为___;从化学键键长的角度分析金刚石、β-氮化碳的硬度大小:__。
(3)CuO晶胞如图:
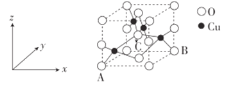
①若氧化铜晶胞中原子坐标参数A为(0,0,0),B为(1,1,0),则C原子坐标参数为___。
②NA代表阿伏加德罗常数的值,晶胞参数为anm,则晶体密度为__g·cm-3(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
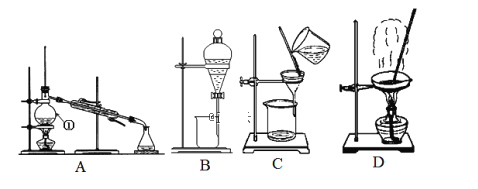
Ⅰ.(1)从碘水中分离出I2,选择装置_______,该分离方法的名称为_________。
(2)写出上图中仪器①的名称___________________ ;
(3)冷凝管中冷却水的方向为________________________ 。
Ⅱ.实验室要配制2mol/L稀硫酸240mL。
(1)量取18.4mol/L的浓硫酸时,用下面那种规格的量筒___(填序号)
①10mL ②50mL ③100mL ④500mL
(2)配制该稀硫酸时使用的仪器除量筒、烧杯外,还必须用到的仪器有玻璃棒、胶头滴管、________。
(3)在配制过程中,如果出现下列情况,将对所配溶液的物质的量浓度有何影响?(填“偏高”、“偏低”或“无影响”)
①用量筒量取浓硫酸时,仰视量筒进行读数________;
②定容时,液面超过刻度线后用胶头滴管吸至液面处______;
Ⅲ.200mL 5mol/L NaOH溶液中,取出20mL溶液,其溶质的质量是___________;将取出的溶液稀释至100mL,其溶质的物质的量浓度是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用元素的化合价推测物质的性质是化学研究的重要手段,氮元素的常见化合价与部分物质类别的对应关系如图所示。
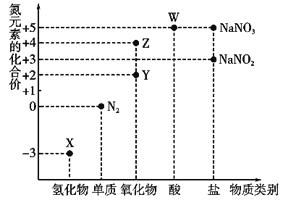
(1)从氮元素化合价的角度分析,X、Y、Z、W中既具有氧化性又具有还原性的有______(填化学式)。
(2) N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为_______________。尾气中的NO用酸性NaClO溶液吸收,其原理是HClO氧化NO生成Cl和NO3-,其离子方程式为______________________________________。
(3)将集满红棕色气体Z的试管倒置于盛有水的水槽中,观察到的现象为_______________________。
(4)W的稀溶液与铜单质发生反应的离子方程式为__________________________。
(5)已知NaNO2能被酸性KMnO4溶液氧化为NaNO3,则50mL0.01 mol·L-1 NaNO2溶液与10mL0.02 mol·L-1 KMnO4溶液恰好完全反应时,还原产物中Mn元素的化合价为__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com