


科目:高中化学 来源: 题型:
| A、大多数有机物难溶于水,易溶于有机溶剂 |
| B、有机物反应比较复杂,一般反应较慢 |
| C、绝大多数有机物熔点高,硬度大 |
| D、绝大多数有机物是非电解质,不易导电,熔点低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KHC2O4溶液中:c(C2O42-)<c(H2C2O4) |
| B、当滴定至中性时:c(C2O42-)═c(Na+)+c(H2C2O4) |
| C、滴入20mL 0.1 mol?L-1NaOH溶液时,溶液中:c(Na+)═c(K+)=2c(C2O42-) |
| D、滴定过程中:c(H+)+c(Na+)+c(K+)═c(OH-)+c(HC2O4-)+c(C2O42-) |
查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
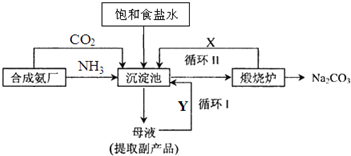
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)某可逆反应在不同条件下的反应历程分别为A、B,如图所示.
(1)某可逆反应在不同条件下的反应历程分别为A、B,如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
 柠檬酸铁可用作食品铁质强化剂、营养增补剂,用于饼干、钙质奶粉等,它可以由柠檬酸(熔点为153°C)与氢氧化铁制得.其结构如图.
柠檬酸铁可用作食品铁质强化剂、营养增补剂,用于饼干、钙质奶粉等,它可以由柠檬酸(熔点为153°C)与氢氧化铁制得.其结构如图.查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示为高温超导领域里的一种化合物--钙钛矿晶体结构,该结构是具有代表性的最小重复单位.
如图所示为高温超导领域里的一种化合物--钙钛矿晶体结构,该结构是具有代表性的最小重复单位.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com