
【题目】二氧化氯(ClO2)是一种黄绿色易溶于水的气体,常用作饮用水消毒。实验室通过如下过程制备二氧化氯。
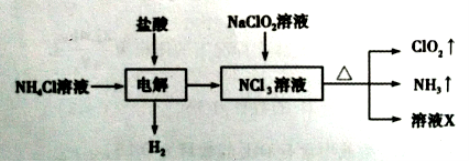
下列说法正确的是( )
A.电解时发生反应的离子方程式为NH4++3Cl-![]() 2H2↑+NCl3
2H2↑+NCl3
B.溶液X中大量存在的阴离子有Cl-、OH-
C.可用饱和食盐水除去ClO2中的NH3
D.可用明矾除去饮用水中残留的NaClO2
科目:高中化学 来源: 题型:
【题目】分类是化学学习与研究的常用方法,下列分类正确的是
A.Cl2O7、P2O5、SO3、CO2均属于酸性氧化物
B.Na2O、Na2O2为相同元素组成的金属氧化物,都属于碱性氧化物
C.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体
D.根据溶液导电能力强弱,将电解质分为强电解质、弱电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016届唐山二模】亚硝酸钠是一种工业盐,外观与食盐非常相似,毒性较强。某化学兴趣小组对食盐与亚硝酸钠进行多角度探究:
(一)鉴别NaCl和NaNO2
甲同学用沉淀分析法
经查:常温下Ksp(AgNO2)=2×10-8, Ksp(AgCl)=1.8×10-10.分别向盛有5mL 0.0001 mol/L两种盐溶液的试合中同时逐滴滴加0.0001mol/L硝酸银溶液,先生成沉淀的是装有 溶液的试管。
乙同学侧定溶液pH
用pH试纸分别测定0.1 mol/L两种盐溶液的pH,测得NaNO2溶液呈碱性。该溶液呈碱性的原因是 (用离子方程式解释)。
(二)该小组用如下装置(略去夹持仪器)制备亚硝酸钠

已知:① 2NO+ Na2O2 = 2NaNO2 ;
② 酸性条件下,NO和NO2都能与MnO4一反应生成NO3一和Mn2+·
(1)使用铜丝的优点是 。
(2)装置A中反应方程式为 。
装置C 中盛放的药品是 ;(填字母代号)
A.浓硫酸 B.NaOH 溶液 C.水 D.四氯化碳
仪器F的作用 。
(3)该小组称取5.000g制取的样品溶于水配成250.0 mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol/L酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
滴定次数 | 1 | 2 | 3 | 4 |
消耗KMnO4溶液体积/mL | 20.70 | 20.12 | 20.00 | 19.88 |
① 第一次实验数据出现异常,造成这种异常的原因可能是 (填字母代号)。
A.锥形瓶洗净后未干燥
B.酸式滴定管用蒸馏水洗净后未用标准液润洗
C.滴定终点时仰视读数
②酸性KMnO4溶液滴定亚硝酸钠溶液的离子方程式为 。
③该样品中亚硝酸钠的质量分数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下图所示的转化关系中,A~J分别表示中学化学中常见的一种物质,其中部分反应物、生成物没有列出。已知反应③是一种重要的工业生产原理,A、B、C、D、E、F六种物质中含有同一种元素。请回答下列问题:

(1)I、G、J三种物质中所含同一种元素在周期表中的位置是 。
(2)写出反应④的离子方程式 。
(3)写出反应⑥的化学方程式 。
(4)写出反应③的电极反应式:阳极: ;阴极: 。
(5)从能量变化的角度看,①②③④反应中焓变ΔH<0的反应是 。(填序号)
(6)A、B、C、D、E、F六种物质中所含同一种元素的电子排布式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某胶体在电泳时,它的胶粒向阴极移动。在这种胶体中分别加入下列物质:
①淀粉溶液②硫酸镁溶液③硅酸胶体④氢氧化铁胶体,不会发生聚沉的是
A.①③B.①④C.②③D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构如图所示,这种有机物不可能具有的性质是( )

①可以与氢气发生加成反应;②能使酸性KMnO4溶液褪色;③能跟NaOH溶液反应; ④能发生酯化反应;⑤能发生加聚反应;⑥能发生水解反应.
A.①④ B.只有⑥
C.只有⑤ D.④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的A、B混合于2L密闭容器中发生如下反应:3A(g)+B(g) ![]() xC(g)+2D(g),4min时测得D的浓度为0.4mol/L,c(A):c(B)=3:5,C的平均反应速率是0.1mol/(L.min),列式计算:
xC(g)+2D(g),4min时测得D的浓度为0.4mol/L,c(A):c(B)=3:5,C的平均反应速率是0.1mol/(L.min),列式计算:
(1)x=__________;
(2)B在这4min内的平均反应速率__________;
(3)此时A的浓度及反应开始前容器中A、B的物质的量__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】催化还原CO2是解决温室效应及能源问题的重要手段之一。研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平衡反应,分别生成CH3OH和CO。反应的热化学方程式如下:
CO2(g)+3 H2(g)![]() CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1 I
CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1 I
CO2(g)+ H2(g)![]() CO(g)+H2O(g)ΔH2 II
CO(g)+H2O(g)ΔH2 II
某实验室控制CO2和H2初始投料比为1:2.2,经过相同反应时间测得如下实验数据:

【备注】Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醛的百分比
已知:①CO和H2的标准燃烧热分别为-283.0kJ·mol-1和-285.8kJ·mol-1
②H2O(l)![]() H2O(g) ΔH3=44.0kJ·mol-1
H2O(g) ΔH3=44.0kJ·mol-1
请回答(不考虑温度对ΔH的影响):
(1)反应I的平衡常数表达式K= ;反应II的ΔH2= kJ·mol-1。
(2)有利于提高CO2转化为CH3OH平衡转化率的措施有 。
A.使用催化剂Cat.1 B.使用催化剂Cat.2 C.降低反应温度
D.投料比不变,增加反应物的浓度 E.增大CO2和H2的初始投料比
(3)表中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com