
����Ŀ��������X������Ԫ����ɣ�Ϊ̽������ɵ����ʣ���Ʋ��������ʵ�飺
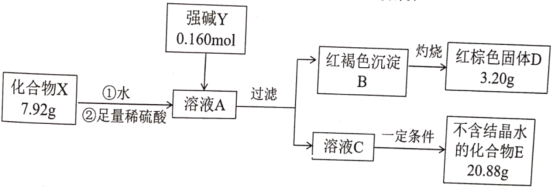
��ʾ��������E����ɫ��ӦΪ��ɫ������ɫ�ܲ�����
��ش�
��1��X�Ļ�ѧʽ��________________��ǿ��Y�ĵ���ʽΪ________________��
��2���ڳ��º���������£�������X�����ȶ����ڣ�������ˮ��Һ�в��ȶ���һ��ʱ���ת��Ϊ���ɫ������һ�����嵥�ʡ�
�ٻ�����X��ˮ��Ӧ�����ӷ���ʽΪ________________��
��������Ի�����X���ȶ��Խ����˴������о�����ȡ����һ���Ľ�չ���������ʿ����������X��ˮ��Һ���ȶ��Ե���________________��
A KHSO4 B K2CO3 C CH3COOK D K2SO3
��Ϊ�о��¶ȶԻ�����Xˮ��Һ�ȶ��Ե�Ӱ�죬�����һ��ʵ�鷽����________________________________________________��
��3��������X�ж����Ʊ���������һ�ַ�������ǿ��Y�������ô����������ɫ����B��Ӧ���仯ѧ����ʽΪ________________��
���𰸡�K2FeO4 ![]() 4 FeO42-+10H2O=4Fe(OH)3��+3O2��+8OH- BC ȡ����������������ֱ����������Թ��в��ӵ�����ˮ�ܽ⣬Ȼ��һ֧�Թ�������ˮ�У���һ֧�Թ�������ˮ�У��۲���������Ŀ����� 3KClO+4KOH+2 Fe(OH)3=2 K2FeO4+3KCl+5H2O
4 FeO42-+10H2O=4Fe(OH)3��+3O2��+8OH- BC ȡ����������������ֱ����������Թ��в��ӵ�����ˮ�ܽ⣬Ȼ��һ֧�Թ�������ˮ�У���һ֧�Թ�������ˮ�У��۲���������Ŀ����� 3KClO+4KOH+2 Fe(OH)3=2 K2FeO4+3KCl+5H2O
��������
���������֪��������E����ɫ��ӦΪ��ɫ������ɫ�ܲ���������˵���û�����E�к�KԪ�أ���������˼ά��������X��ˮ�����ᷴӦ�õ�����ҺA�м���ǿ�����Ӧ�����ĺ��ɫ�ij���ΪFe(OH)3����֤��X�к���Ԫ�أ�3.20g����ɫ����DΪFe2O3����n(Fe2O3)= ![]() =
=![]() =0.02mol����n(Fe) =0.04mol����Һ��һ�������������ɵõ�һ�ִ����IJ����ᾧˮ������K2SO4������Ϊ20.88 g��n(K2SO4)=
=0.02mol����n(Fe) =0.04mol����Һ��һ�������������ɵõ�һ�ִ����IJ����ᾧˮ������K2SO4������Ϊ20.88 g��n(K2SO4)=![]() =0.12mol������ԭ�����к��е�K+�����ʵ���Ϊ0.12mol��2-0.16mol=0.08mol����˿��Ƴ�����X�л�����KԪ�أ�����һ��Ԫ��ӦΪ��Ԫ�أ�������m(O)= 7.92g -0.04mol��56g/mol- 0.08mol�� 39g/mol= 2.56g������n(O)=
=0.12mol������ԭ�����к��е�K+�����ʵ���Ϊ0.12mol��2-0.16mol=0.08mol����˿��Ƴ�����X�л�����KԪ�أ�����һ��Ԫ��ӦΪ��Ԫ�أ�������m(O)= 7.92g -0.04mol��56g/mol- 0.08mol�� 39g/mol= 2.56g������n(O)=![]() =0.16mol������ڻ�����A�и�Ԫ��ԭ�ӵĸ�����ΪK��Fe:O=0.08��0.04��0.16=2:1:4���ʻ�ѧʽΪK2FeO4���ݴ˷�������
=0.16mol������ڻ�����A�и�Ԫ��ԭ�ӵĸ�����ΪK��Fe:O=0.08��0.04��0.16=2:1:4���ʻ�ѧʽΪK2FeO4���ݴ˷�������
��������������֪��
��1��X������Ԫ�طֱ�ΪK��Fe��O����ԭ�Ӹ�����Ϊ2:1:4���ʻ�ѧʽΪK2FeO4��ǿ��YΪ�������أ��ɼ����������������ӹ��ɣ������ʽΪ��![]() ���ʴ�Ϊ��K2FeO4��
���ʴ�Ϊ��K2FeO4��![]() ��
��
��2���ڳ��º���������£�������X�����ȶ����ڣ�������ˮ��Һ�в��ȶ���һ��ʱ���ת��Ϊ���ɫ����Ϊ�������������������ԭ��Ӧ�Ĺ�����֪�����������嵥��ӦΪ��������
�ٸ��������ˮ��Ӧ�����ӷ���ʽΪ��4FeO42-+10H2O=4Fe(OH)3��+3O2��+8OH-��
�ڸ���������Ӧ��֪��Ҫ������ȶ��ԣ�Ӧ��ʹ��Һ�Լ��ԣ���
A. KHSO4��ˮ�е���������ӣ�ʹ��Һ�����ԣ����������ȶ��ԣ�
B. K2CO3ˮ���Լ��ԣ��������⣻
C. CH3COOKˮ���Լ��ԣ��������⣻
D. K2SO3��ˮ���Լ��ԣ������л�ԭ�ԣ�����K2FeO4����������ԭ��Ӧ�������棬���������ȶ��ԣ�
��ѡBC��
�۹̶������������ı��¶ȣ������������Ŀ����������ʵ��Ϊȡ����������������ֱ����������Թ��в��ӵ�����ˮ�ܽ⣬Ȼ��һ֧�Թ�������ˮ�У���һ֧�Թ�������ˮ�У��۲���������Ŀ�����
��3����KOH�����������ô�������������������Ʊ�������صĻ�ѧ����ʽ3KClO+4KOH+ 2Fe(OH)3= 2K2FeO4+3KCl+5H2O��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȼ�ϵ��(MFC)��һ���ִ�������ȥ����������ͼΪMFC̼������ͬʱȥ����ת��ϵͳԭ��ʾ��ͼ������˵����ȷ����

A. �������ﷴӦ���з�ӦΪ��NH4++2O2==NO3��+2H++H2O
B. B�����Ʊ�A�����Ƶ�
C. A���ĵ缫��ӦʽCH3COO��+8e��+2H2O==2CO2+7H+
D. ����·��ͨ��1mol����ʱ���������ܹ�����2.24LN2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B����������Ԫ����ɵĻ����A��ij��Ԫ�ص���������Ϊ![]() ��B��һ�ֵ���ɫ���壬C��J��ͬ����Ԫ�ص���̬�⻯�����C�Ǻ�������ߵ�����DΪ��������ǿ����������ǿ��İ�ɫ��״���ʣ�XΪ��������ɫҺ�塣��Ӧ���ɵ�ˮ������ȥ������������ͼ��ʾ�Ĺ�ϵ��
��B��һ�ֵ���ɫ���壬C��J��ͬ����Ԫ�ص���̬�⻯�����C�Ǻ�������ߵ�����DΪ��������ǿ����������ǿ��İ�ɫ��״���ʣ�XΪ��������ɫҺ�塣��Ӧ���ɵ�ˮ������ȥ������������ͼ��ʾ�Ĺ�ϵ��
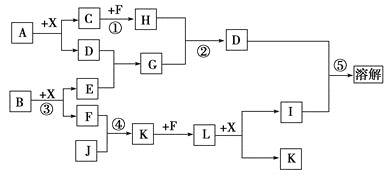
(1)д��A�Ļ�ѧʽ��________
(2)д�� B�ĵ���ʽ______________
(3)��Ӧ![]() ��ÿ����
��ÿ����![]() ��ת�Ƶ��ӵ���ĿΪ________
��ת�Ƶ��ӵ���ĿΪ________![]() ��
��![]() ��ʾ�����ӵ�����
��ʾ�����ӵ�����![]()
(4)��Ӧ![]() �Ļ�ѧ����ʽΪ��______________________________
�Ļ�ѧ����ʽΪ��______________________________
(5)д��H����ʱ��Ӧ![]() �����ӷ���ʽ_______________________________________
�����ӷ���ʽ_______________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ع㷺Ӧ���ڻ�϶�������ϵͳ���缫������Ni(OH)2��̼�ۡ���������Ϳ�����������Ƴɡ����ڵ��ʹ�ú�缫���϶Ի�����Σ����ij��ȤС��Ըõ�ص缫���Ͻ�����Դ�����о������ʵ���������£�
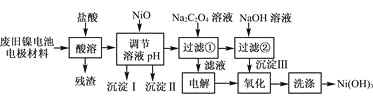
��֪����NiCl2������ˮ��Fe3����������Ni2����
����֪ʵ���¶�ʱ���ܽ�ȣ�NiC2O4��NiC2O4��H2O��NiC2O4��2H2O
��ij�¶���һЩ�������������Ksp����������������pH���±���ʾ��
|
| ��ʼ����pH | ������ȫpH |
|
|
|
|
|
|
|
|
|
|
|
|
�ش��������⣺
(1) ��NiO������Һ��pH����������������________�ͳ�����__________(�ѧʽ)��
(2) д������Na2C2O4��Һ�ķ�Ӧ�Ļ�ѧ����ʽ��_____________________��
(3) ��������Һʱ��������������ķ�����___________________________��
(4) д������������Ӧ�����ӷ���ʽ��___________________________________��
(5) ��μ���Ni(OH)3��ϴ�Ӹɾ���_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������淶���ܴﵽʵ��Ŀ�ĵ���
���� | Ŀ�� | |
A | ��ȡ5.0gCuSO4��5H2O����27.0gˮ��,�����ܽ� | ����10%CuSO4��Һ |
B | ����ϡ����ϴ�ӣ�����ˮ��ϴ | ϴ�ӷֽ�KMnO4��O2���Թ� |
C | �ò�����պȡ��Һ�����ڸ����pH��ֽ�ϣ�Ƭ�̺������ɫ���Ƚϲ����� | �ⶨ0.05mol.L-1NaClO��Һ��pH |
D | ���ֵ�����ձ��У��ձ��ڷ�һʢ����ˮ����ƿ����ʯ�������ձ����ȣ�Ȼ���ռ���ƿ��ڵĹ��� | �ᴿ����NH4Cl�Ĵֵ� |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ����ָʹ�ú��ʵĻ�ԭ����ʹ��Һ�еĽ������ӻ�ԭ�ɽ����������ڶƼ������ϵ�һ�ֶƸ����ա���ѧ�ƹ㷺�������������ϡ��������մɵ�������ϵ�װ�κͷ�������ABS�������ϱ�����л�ѧ�������������£�
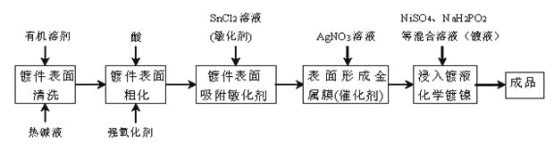
�ش��������⣺
��1����ѧ�����ƱȽϣ��ŵ�֮һ��_________��
��2���Ƽ��������ȼ�Һ��ϴ��������_________���Ƽ�����ֻ���Ŀ������ǿ��ˮ�Լ�_________��
��3���Ƽ�����AgNO3��Һ�Ƽ�����������SnCl2��AgNO3��ԭ�����д����ԵĽ���������Ӧ�Ļ�ѧ����ʽ��_________��
��4������ʱ����Һ�е�Ni2+��H2PO2-�ڴ������Ϸ�Ӧ��������ͬʱ������ǿ��H3PO3������������ʵ�����ȵ��������÷�Ӧ�����ӷ���ʽ��_________��
��5����ѧ��ij�ֽ���ʱ����Ӧʱ����Ʋ��ȵ�ʵ�����ݼ�¼���±���ʾ��

�ɴ��ƶϣ��Ʋ���y�뷴Ӧʱ��t�Ĺ�ϵʽΪ_________����ʹ�Ʋ���Ϊ6anm����Ҫ�ķ�Ӧʱ��Ϊ_________��
��6����ѧ������Һ�к���Ni2+����Ⱦ���ת��Ϊ������ȥ����֪25����Ksp[Ni(OH)2]=2.0��10-15����������ʹ��Һ��pH=10��������ķ�Һ����Ԫ�صĺ���Ϊ_________mg��L-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������þ[Mg(ClO3)2]����������������ݼ��ȣ�ʵ�����Ʊ�����Mg(ClO3)2��6H2O���������£�

��֪����±����Ҫ�ɷ�ΪMgCl2��6H2O������MgSO4��FeCl2�����ʡ�
�����ֻ�������ܽ��(S)���¶�(T)�仯������ͼ��ʾ��

��1����������Ҫ����Ҫ����������___����MgO�����������������Ҫ�ɷ�Ϊ___��
��2������BaCl2��Ŀ���dz�ȥSO42������μ���SO42���ѳ�����ȫ����___��
��3������NaClO3������Һ������ӦΪ��MgCl2��2NaClO3��Mg(ClO3)2��2NaCl�����ٽ�һ����ȡMg(ClO3)2��6H2O��ʵ�鲽������Ϊ����___����___����___���ܹ��ˡ�ϴ�ӡ�
��4����Ʒ��Mg(ClO3)2��6H2O�����IJⶨ��
����1��ȷ����3.50 g��Ʒ���100 mL��Һ��
����2��ȡ10 mL����ƿ�У�����10 mLϡ�����20 mL 1.000 mol��L��1��FeSO4��Һ���ȡ�
����3����ȴ�����£���0.100 mol��L��1K2Cr2O7��Һ�ζ����յ㣬�˹����з�Ӧ�����ӷ���ʽΪ��Cr2O72����6Fe2����14H����2Cr3����6Fe3����7H2O��
����4��������2��3�ظ����Σ�ƽ������K2Cr2O7��Һ15.00 mL��
��д������2�з�����Ӧ�����ӷ���ʽ��___
�ڲ�Ʒ��Mg(ClO3)2��6H2O����������Ϊ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ũ�ȹ�ϵ��ȷ���ǣ� ��
A.��0.1mol/LNH4HSO4��Һ�еμ�0.1mol/L��Ba(OH)2��Һ�������պ���ȫ��c(NH4+)��c(OH-)��c(SO42-)��c(H+)
B.��0.1mol/L��KOH��Һ��ͨ���״���µ�CO2����3.36L��������Һ�У�c(K+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-)
C.pH��ͬ��NaOH��Һ��CH3COONa��Һ��Na2CO3��Һ��NaHCO3��Һ��Ũ�ȣ�c(NaOH)��c(CH3COONa)��c(NaHCO3)��c(Na2CO3)
D.0.1mol/L��NaOH��Һ��0.2mol/L��HCN��Һ�������ϣ�������Һ�ʼ��ԣ�c(HCN)��c(Na+)��c(CN-)��c(OH-)��c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС��ͬѧ��FeCl3��KI�ķ�Ӧ����̽����
������̽���������½����±�����ʵ�顣
��� | ���� | ���� |
ʵ���� | ȡ5mL 0.1mol/L KI��Һ���μ�0.1mol/L FeCl3��Һ56�Σ������ҺpH��5�� | ��Һ��Ϊ�ػ�ɫ |
ʵ���� | ȡ2mLʵ������Ӧ�����Һ���μ�2��0.1molL1 KSCN��Һ | ��Һ�ʺ�ɫ |
(1)֤��ʵ��������Fe2+ ���ɣ�������Լ�Ϊ____________________________��
(2)д��ʵ������Ӧ�����ӷ���ʽ��_____________________________________��
(3)����ʵ���������֤��Fe3+��I�������淴Ӧ��ʵ����������ϵ�������__________
(4)��ʵ��I����Һ�м���CCl4��ʵ��������____________________________��ȡ���ϲ���Һ�еμ�KSCN��Һ����δ�������Եĺ�ɫ����ԭ��Ϊ����ƽ���ƶ��ĽǶȽ��ͣ�_________________________________________________________��
������̽����20min������۲�ʵ������ʵ������Һ�ػ�ɫ���ʵ������Һ��ɫ��dz��
(5)��֪�����Խ�ǿ�������£�I�ɱ���������ΪI2���ʼ�ͬѧ������裺�÷�Ӧ�����¿�����I����ΪI2��ʹʵ�������Һ�ػ�ɫ�����ͬѧ���ʵ�飺____________________________________��20min����Һ��������֤���ü��費������������Һ�����������ؿ�����__________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com