
| ||
| △ |

| (18n+48)g |
| 18ng |
| 10-x |
| y |
| 24 |
| 9n |
| 10-x |
| y |
| (18n+48)g |
| 18ng |
| 10-x |
| y |
| 24 |
| 9n |
| 10-x |
| y |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)t℃时水的离子积为1×10-13,则该温度(选填大于、小于或等于)
(1)t℃时水的离子积为1×10-13,则该温度(选填大于、小于或等于)查看答案和解析>>
科目:高中化学 来源: 题型:
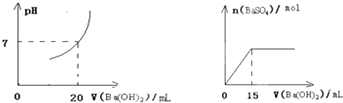
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
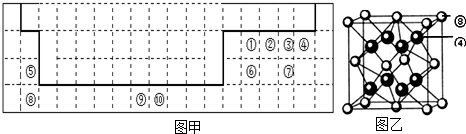
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| H2X | 187 | 202 | 2.6 |
| H2Y2 | 272 | 423 | 以任意比互溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)在粗制CuSO4?5H2O晶体中常含有杂质Fe2+.在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是
(1)在粗制CuSO4?5H2O晶体中常含有杂质Fe2+.在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com