
【题目】已知反应4CO+2NO2![]() N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
A.v(CO)=1.5mol·L-1·min-1B.v(NO2)=0.8mol·L-1·min-1
C.v(N2)=0.3mol·L-1·min-1D.v(CO2)=1.1mol·L-1·min-1
 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:
【题目】表为元素周期表短周期的一部分,下列有关A、B、C、D四种元素的叙述正确的是( )

A.原子半径大小比较为D>C>B>A
B.生成的氢化物分子间均可形成氢键
C.A与C形成的阴离子可能有AC32-、A2C42-
D.A、B、C、D的单质常温下均不导电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求作答:
(1)常温下,pH=2的醋酸和pH=12的氢氧化钠等体积混合,混合后溶液呈_____性
(2)25℃时,柠檬水的pH是3,其中氢氧根离子浓度是_______mol/L
(3)已知下列反应:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H1= -akJ/mol
②C(s)+O2(g)=CO2(g) △H2= -bkJ/mol
则反应2C(s)+2H2O(l) =CH3COOH(l)的反应热为△H=_____________kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下不能实现的是
①S![]() SO3
SO3![]() H2SO4
H2SO4
②N2![]() NO
NO![]() NO2
NO2![]() HNO3
HNO3
③MgCl(aq)![]() 无水MgCl2
无水MgCl2![]() Mg
Mg
④Fe![]() Fe2O3
Fe2O3![]() Fe2(SO4)3
Fe2(SO4)3
⑤铝土矿![]() NaAlO2溶液
NaAlO2溶液![]() Al(OH)2
Al(OH)2![]() Al2O2
Al2O2![]() Al
Al
A.①③⑤
B.②③④
C.③④⑤
D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)![]() CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H2=-58 kJ/mol
CH3OH(g)+H2O(g) △H2=-58 kJ/mol
③CO2(g)+H2(g)![]() CO(g)+H2O(g) △H3=+41 kJ/mol
CO(g)+H2O(g) △H3=+41 kJ/mol
回答下列问题:
(1)CO2的电子式是 。
(2)△H1= kJ/mol,①反应正向的熵变△S 0(填>、<或=)。
(3)在容积为2L的密闭容器中,充入一定量CO2和H2合成甲醇(上述②反应),在其他条件不变时,温度T1、T2对反应的影响图像如图,下列说法正确的是__________(填序号)
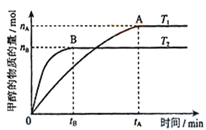
①温度为T1时,从反应到平衡,生成甲醇的平均速率为:v(CH3OH)=nA/tA mol/(L·min)
②当v(CH3OH) = v(H2O)时,说明反应达到平衡
③混合气体的平均相对分子质量A点大于B点
④处于A点的反应体系从T1变到T2,达到平衡时n(H2)与n(CH3OH)比值增大
(4)在T1温度时,将2molCO2和6molH2充入2L密闭容器中,充分反应(上述②反应)达到平衡后,若CO2转化率为50%,,则容器内的压强与起始压强之比为__________;T1温度,反应CH3OH(g)+H2O(g)![]() CO2(g)+3H2(g)的平衡常数数值为__________。
CO2(g)+3H2(g)的平衡常数数值为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,装置Ⅰ为新型电池,放电时B电极的反应式为NaBr3+2Na++2e-=3NaBr,装置Ⅱ为铅蓄电池。首先闭合K1和K2,当铅蓄电池充电结束后,断开K1,闭合K2。下列说法正确的是

A.装置Ⅰ放电时的A电极反应式为2Na2S2-2e-=Na2S4+2Na+
B.闭合K1、K2时,每有0.1molNa+通过离子交换膜,装置Ⅱ溶液中有0.1mol电子转移
C.断开K1、闭合K2时,b电极的电极反应式为PbO2+2e-+SO42-+4H+=PbSO4+2H2O
D.断开K1、闭合K2时,装置Ⅱ中SO42-向a电极迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z为元素周期表中前四周期元素,且原子序数依次增大.W的基态原子中占据哑铃形原子轨道的电子数为3,![]() 与
与![]() 具有相同的电子层结构;W与X的最外层电子数之和等于Y的最外层电子数;Z元素位于元素周期表的第11列.请回答:
具有相同的电子层结构;W与X的最外层电子数之和等于Y的最外层电子数;Z元素位于元素周期表的第11列.请回答:
(1)Z的基态原子M层的电子排布式为____________________.
(2)W的简单氢化物分子中W原子的__________轨道与氢原子的__________轨道重叠形成![]() 键.(填轨道名称)
键.(填轨道名称)
(3)比较Y的含氧酸的酸性:![]() __________
__________![]() (填“>”或“<”),原因为___________________.
(填“>”或“<”),原因为___________________.
(4)关于Z的化合物![]() (EDTA的结构简式如下图)的说法正确的是_____选项字母).
(EDTA的结构简式如下图)的说法正确的是_____选项字母).
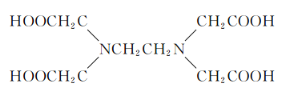
A.![]() 中所含的化学键有离子键、共价键、配位键和氢键
中所含的化学键有离子键、共价键、配位键和氢键
B.EDTA中碳原子的杂化轨道类型为![]() 、
、![]()
C.![]() 的组成元素的第一电离能顺序为
的组成元素的第一电离能顺序为![]()
D.![]() 与
与![]() 互为等电子体,空间构型均为正四面体形
互为等电子体,空间构型均为正四面体形
(5)某离子型氢化物![]() 的晶胞结构如图所示:
的晶胞结构如图所示:
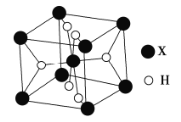
①![]() 的配位数为__________________.
的配位数为__________________.
②![]() 是一种储氢材料,遇水会缓慢反应,该反应的化学方程式为____________.
是一种储氢材料,遇水会缓慢反应,该反应的化学方程式为____________.
③若该晶胞的密度为![]() ,则晶胞的体积为______________
,则晶胞的体积为______________![]() .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水中有机物可用C6H10O5 表示。有关说法正确的是 ( )

A.该装置为原电池,b为原电池的负极
B.a极区溶液的pH减小,中间室Na+移向左室
C. 当左室有4.48L(标准状况下)CO2生成时,右室产生的N2为0.8mol
D.a电极反应式:C6H10O5-24e-+7H2O===6CO2↑+24H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现以CO、O2、熔融盐Z(Na2CO3)组成的燃料电池,采用电解法处理CO同时制备N2O5,装置如图所示,其中Y为CO2。下列说法不合理的是( )
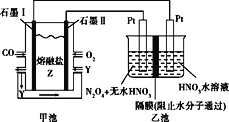
A.石墨Ⅰ是原电池的负极,发生氧化反应
B.乙池中,若使用质子交换膜,每生成1molN2O5,则有2mol H+通过交换膜进入右室
C.石墨II的电极反应式:O2+2CO2+4e-=2CO32-
D.若甲池消耗标准状况下的氧气2.24L,则乙池中产生氢气0.2mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com