
����Ŀ��һ���¶��£���һ���ݻ�Ϊ1L���ܱ������У�����1molH2(g)��1mol I2(g)��������ӦH2(g)��I2(g)![]() 2HI(g)������ַ�Ӧ�ﵽƽ������ɵ�HI(g)ռ���������50%�����¶��£�����һ���ݻ�Ϊ2L���ܱ������г���1molHI(g)������ӦHI(g)
2HI(g)������ַ�Ӧ�ﵽƽ������ɵ�HI(g)ռ���������50%�����¶��£�����һ���ݻ�Ϊ2L���ܱ������г���1molHI(g)������ӦHI(g)![]()
![]() H2(g)��
H2(g)��![]() I2(g)���������ж���ȷ����(����)
I2(g)���������ж���ȷ����(����)
A.��һ��Ӧ��ƽ�ⳣ��Ϊ1
B.��һ��Ӧ��ƽ�ⳣ��Ϊ0.5
C.��һ��Ӧ�ﵽƽ��ʱ��H2��ƽ��Ũ��Ϊ0.25 mol��L��1
D.��һ��Ӧ�ﵽƽ��ʱ��HI(g)��ƽ��Ũ��0.5 mol��L��1
���𰸡�B
��������
A��B��һ���¶��£���H2��I2��1mol����̬��������1L���ܱ������У�������ӦH2(g)��I2(g)![]() 2HI(g)���ﵽƽ������ɵ�HI(g)���������Ϊ50%�����ڸ÷�Ӧǰ��������������䣬����ƽ��ʱ����������ʵ���Ϊ2mol����HIΪ2mol��50%=1mol��H2��I2�����ʵ�����ȣ���Ϊ0.5mol�����Ϊ1L����HI��H2��I2��Ũ�Ⱥ����ʵ�����ȣ��ֱ�Ϊ1mol/L��0.5mol/L��0.5mol/L������H2(g)��I2(g)
2HI(g)���ﵽƽ������ɵ�HI(g)���������Ϊ50%�����ڸ÷�Ӧǰ��������������䣬����ƽ��ʱ����������ʵ���Ϊ2mol����HIΪ2mol��50%=1mol��H2��I2�����ʵ�����ȣ���Ϊ0.5mol�����Ϊ1L����HI��H2��I2��Ũ�Ⱥ����ʵ�����ȣ��ֱ�Ϊ1mol/L��0.5mol/L��0.5mol/L������H2(g)��I2(g)![]() 2HI(g)��ƽ�ⳣ��Ϊ
2HI(g)��ƽ�ⳣ��Ϊ![]() =
=![]() =4���¶Ȳ��䣬ƽ�ⳣ�����䣬����2HI(g)
=4���¶Ȳ��䣬ƽ�ⳣ�����䣬����2HI(g) ![]() H2(g)��I2(g)��ƽ�ⳣ��ΪH2(g)��I2(g)
H2(g)��I2(g)��ƽ�ⳣ��ΪH2(g)��I2(g)![]() 2HI(g)�ĵ�������
2HI(g)�ĵ�������![]() ��HI(g)
��HI(g)![]()
![]() H2(g)��
H2(g)��![]() I2(g)��ƽ�ⳣ��Ϊ2HI(g)
I2(g)��ƽ�ⳣ��Ϊ2HI(g) ![]() H2(g)��I2(g)��
H2(g)��I2(g)��![]() �������
�η�������![]() =0.5����A����B��ȷ��
=0.5����A����B��ȷ��
C��2L���ܱ������г���1molHI(g)������ӦHI(g)![]()
![]() H2(g)��
H2(g)��![]() I2(g)�������ݻ�Ϊ1L���ܱ������У�����1molH2(g)��1mol I2(g)�ﵽ��Чƽ�⣬ƽ��ʱ����ֵ����������ȣ����Ժ�һ��Ӧƽ���HI���������Ϊ50%�������ʵ���Ϊ1mol��50%=0.5mol��H2��I2�����ʵ�����ȣ���Ϊ0.25mol�����Ϊ2L������H2��ƽ��Ũ��Ϊ
I2(g)�������ݻ�Ϊ1L���ܱ������У�����1molH2(g)��1mol I2(g)�ﵽ��Чƽ�⣬ƽ��ʱ����ֵ����������ȣ����Ժ�һ��Ӧƽ���HI���������Ϊ50%�������ʵ���Ϊ1mol��50%=0.5mol��H2��I2�����ʵ�����ȣ���Ϊ0.25mol�����Ϊ2L������H2��ƽ��Ũ��Ϊ![]() =0.125mol/L����C����
=0.125mol/L����C����
D���������ϼ����һ��Ӧ�ﵽƽ��ʱ��HI(g)��ƽ��Ũ��Ϊ![]() =0.25mol/L����D����ѡB��
=0.25mol/L����D����ѡB��


 �������Ͽ�ʱͬ��ѵ��ϵ�д�
�������Ͽ�ʱͬ��ѵ��ϵ�д� �������ͬ����ϰϵ�д�
�������ͬ����ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����£�����ij�������Һ�д��ܽ�ƽ��ʱ�����������ӵ�Ũ����S2-Ũ�ȵı仯������ͼ��ʾ����ͼ�жϣ�����˵���������� ( )
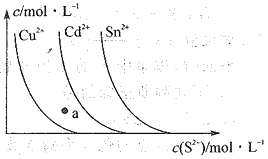
A.�������ʵ��ܶȻ���СΪKsp(CuS)��Ksp(CdS)��Ksp(SnS)
B.��SnS����Һ�м�������CuSO4���壬c(Sn2+)�����
C.a����CdS��������
D.�����ʵ���Ũ�ȵ�Cu2+��Sn2-�Ļ��Һ�У��μ�Na2S��Һ��������CuS����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�ܱ�������ͨ��A��B�������壬��һ�������·�����Ӧ2A(g)��B(g)![]() 2C(g) ��H<0������Ӧ�ﵽƽ��ı�һ������(x)���±�����(y)һ��������ͼ�����ߵ��ǣ� ��
2C(g) ��H<0������Ӧ�ﵽƽ��ı�һ������(x)���±�����(y)һ��������ͼ�����ߵ��ǣ� ��
x | y |
| |
A | �¶� | ��������ƽ����Է������� | |
B | ѹǿ | A�İٷֺ��� | |
C | ��ͨ��A | B��ת���� | |
D | ������� | A���������� |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�����������ķ�Ӧ��ʵ�����¡�
ʵ�� (20C) | ���� |
�� | ��ɫ����(�����������ɫ)����Һ��Ϊ��ɫ |
�� | 6mL��ɫ����(�����ΪH2)����Һ������ɫ |
�����в�������ɫ������______��
������������
�ټ�ͬѧ��Ϊ��Ũ�ȵ�������H+�������Դ���NO3��������NO3��û�з�����Ӧ����ͬѧ����������֤���˼�˵������ȷ����ʵ��֤����______��
![]() ��ͬѧͨ���������Ʋ��NO3��Ҳ�ܱ���ԭ��������______��������ͨ��ʵ��֤ʵ����Һ�к���NH4+����ʵ�������______��
��ͬѧͨ���������Ʋ��NO3��Ҳ�ܱ���ԭ��������______��������ͨ��ʵ��֤ʵ����Һ�к���NH4+����ʵ�������______��
![]() ��ȫ����NO3������ԭΪ
��ȫ����NO3������ԭΪ![]() �Ĺ��̣�NO3�� + ______e�� + ______= NH4+ + ______H2O
�Ĺ��̣�NO3�� + ______e�� + ______= NH4+ + ______H2O
���о�Ӱ�����H2������
ʵ�� | ���� |
�� | 3.4m L����(�����ΪH2������Һ�Դ���ɫ |
�� | 2.6m L����(�����ΪH2������ɫ��Һ |
�� | ��ɫ����(�����������ɫ)������ɫ��Һ |
���ϣ�Fe[(NO)]2+����Һ�г���ɫ�� �ܶԱ��������������¶Ȳ�ͬʱ�ռ��������������ͬ��ԭ����______�� ��������ɫ�����ǻ�����壬��һ�����������������ɫ�������______�� �ȸ���ʵ�飬���������ᷴӦʱ��Ӱ������Ļ�ԭ���ﲻͬ��������______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴Ӧ��mA���̣�+nB������![]() eC������+fD����������Ӧ�����У���������������ʱ��C���������(C%)���¶�T��ѹǿP�Ĺ�ϵ��ͼ������������ȷ����
eC������+fD����������Ӧ�����У���������������ʱ��C���������(C%)���¶�T��ѹǿP�Ĺ�ϵ��ͼ������������ȷ����
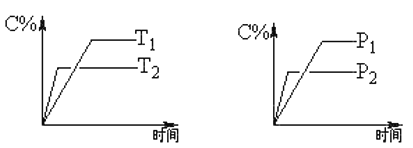
A.�ﵽƽ��������C������
B.�ﵽƽ���������ƽ��������
C.m+n��e+f
D.��ƽ�������ѹƽ�������ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25 ��ʱ���ֱ���20.00 mL 0.100 0 mol��L��1�İ�ˮ���������Һ�еμ�0.100 0 mol��L��1�����ᣬ��ҺpH�������������ı仯��ϵ��ͼ��ʾ������˵���������(����)
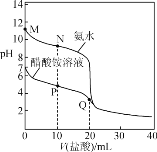
A.��ˮ�ĵ���ƽ�ⳣ����������Լ��10-5
B.N�㣺c(NH4+)>c(Cl��)>c(NH3��H2O)>c(OH��)
C.P�㣺c(NH4+)<2c(CH3COO��)��c(NH3��H2O)
D.Q�㣺2c(Cl��)��c(CH3COOH)��c(NH4+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A.�����£���ϡ��ˮ��μ���ϡ�����У�����Һ��![]() ʱ��
ʱ��![]()
B.���ִ�����Һ�����ʵ���Ũ�ȷֱ�Ϊ![]() ��
��![]() ��pH�ֱ�Ϊa��
��pH�ֱ�Ϊa��![]() ����
����![]()
C.�����£�![]() ��NaOH��Һ��
��NaOH��Һ��![]() �Ĵ�����Һ�������ϣ�����ʯ����Һ�ʺ�ɫ
�Ĵ�����Һ�������ϣ�����ʯ����Һ�ʺ�ɫ
D.��![]() �İ�ˮ�м�����������粒��壬����Һ��
�İ�ˮ�м�����������粒��壬����Һ��![]() ��ֵ����
��ֵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y��Z��W��Ԫ�����ڱ��е�λ����ͼ��ʾ������X��Y��Z����Ԫ�ص�������֮��Ϊ21��
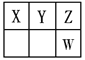
��1��д��W�ļ����ӵ�ԭ�ӽṹʾ��ͼΪ_____________����Ԫ����Z�γ�ԭ�Ӹ�����Ϊ1��1�Ļ������ṹʽΪ__________��
��2��Y������������Ӧ��ˮ������Y���⻯��ǡ����ȫ��Ӧ���������ˮ��Һ�����ԣ���ԭ���ǣ������ӷ���ʽ��ʾ��_______________��
��3��д��Y������������Ӧˮ�����Ũ��Һ��X�ڼ��������·�Ӧ�Ļ�ѧ����ʽΪ___________����Ӧ��ÿת��8mol ���ӣ����ĵĻ�ԭ������Ϊ_______g��
��4��д����˵��Y�ķǽ����Ա�Z����һ��ʵ����ʵ��_____________��
����1L�������������м���0.200mol CO��1.00mol H2O(g)����t��ʱ��Ӧ��CO+ H2O(g)![]() CO2+ H2�ﵽƽ�⣬���÷�Ӧ�Ļ�ѧƽ�ⳣ��K=1����t��ʱCO ��ת����Ϊ___________��
CO2+ H2�ﵽƽ�⣬���÷�Ӧ�Ļ�ѧƽ�ⳣ��K=1����t��ʱCO ��ת����Ϊ___________��
�״�ȼ�ϵ����һ������������ɫ��Դ�������ڵ綯�����ĵ�Դ������ȼ�ϵ��������Ϊ�������Һ���ܷ�ӦΪ��2CH3OH + 3O2= 2CO2+ 4H2O�����������ĵ缫��Ӧʽ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() ʱ��
ʱ��![]() ��
��![]() ��
��![]() ����������10mL
����������10mL![]() ��Һ����μ���
��Һ����μ���![]() ��Һ����ͼ����Һ�к�̼Ԫ�������ʵ���������pH���Ͷ��仯��ͼ��
��Һ����ͼ����Һ�к�̼Ԫ�������ʵ���������pH���Ͷ��仯��ͼ��![]() �����ݳ�δ����
�����ݳ�δ����![]() ������˵���������
������˵���������
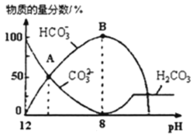
A.A����ʾ��Һ��![]()
B.B����ʾ��Һ��![]()
C.A��![]() �㷢����Ӧ�����ӷ���ʽΪ
�㷢����Ӧ�����ӷ���ʽΪ![]()
D.�ֲ������̪�ͼ��ȣ��õζ����ɲⶨ![]() ��
��![]() ���������
���������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com