
【题目】A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转换关系 (部分反应中得水已忽略)

(1)若A为氯碱工业的产品,C为厨房中的用品。
①反应Ⅰ的离子方程式为____________________________________________;
②氯碱工业制备A的化学方程式是__________________________________________________。
(2)若A、D均为单质,且A为气体,D元素的一种红棕色氧化物常用作颜料。
①B溶液可净水的原因是____________________________________________;
②A的实验制法的化学方程式____________________________________________。
(3)若B是一种两性氢氧化物,请写出反应Ⅲ的离子方程式____________________________________。
【答案】2OH-+CO2 =CO32-+H2O 2NaCl+2H2O ![]() 2NaOH + Cl2↑+ H2↑FeCl3水解生成Fe(OH)3胶体,可吸附水中杂质MnO2 + 4HCl(浓)
2NaOH + Cl2↑+ H2↑FeCl3水解生成Fe(OH)3胶体,可吸附水中杂质MnO2 + 4HCl(浓) ![]() MnCl2 + Cl2↑ + 2H2OAl3++3AlO2-+6H2O=4Al(OH)3↓
MnCl2 + Cl2↑ + 2H2OAl3++3AlO2-+6H2O=4Al(OH)3↓
【解析】
(1)若A为氯碱工业的产品,C为厨房中的用品,可知A为NaOH,C为NaHCO3,B为Na2CO3,D为CO2,Na2CO3,NaHCO3是弱酸强碱盐,是在水的作用下而发生水解显碱性;(2)D元素的一种红棕色氧化物常用作颜料,应为氧化铁,则D为Fe,A为Cl2,B为FeCl3,C为FeCl2。
(1)若A为氯碱工业的产品,C为厨房中的用品,可知A为NaOH,C为NaHCO3,B为Na2CO3,D为CO2,Na2CO3,NaHCO3是弱酸强碱盐,是在水的作用下而发生水解显碱性,
①反应Ⅰ为NaOH和少量CO2的反应,反应的离子方程式是2OH-+CO2 =CO32-+H2O;②氯碱工业制备A,即NaOH时,电解饱和食盐水生成氢氧化钠、氯气和氢气,反应的化学方程式是2NaCl+2H2O ![]() 2NaOH + Cl2↑+ H2↑;(2)D元素的一种红棕色氧化物常用作颜料,应为氧化铁,则D为Fe,A为Cl2,B为FeCl3,C为FeCl2,B为FeCl3,FeCl3水解生成Fe(OH)3胶体,可吸附水中杂质,可用于净水;
2NaOH + Cl2↑+ H2↑;(2)D元素的一种红棕色氧化物常用作颜料,应为氧化铁,则D为Fe,A为Cl2,B为FeCl3,C为FeCl2,B为FeCl3,FeCl3水解生成Fe(OH)3胶体,可吸附水中杂质,可用于净水;
②A为Cl2,实验室利用加热二氧化锰和浓盐酸反应生成氯化锰、氯气和水的方法得到氯气,反应的化学方程式为MnO2 + 4HCl(浓) ![]() MnCl2 + Cl2↑ + 2H2O;(3)若B是一种两性氢氧化物则为氢氧化铝,反应Ⅲ是偏铝酸盐与铝盐发生双水解反应生成氢氧化铝,反应的离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓。
MnCl2 + Cl2↑ + 2H2O;(3)若B是一种两性氢氧化物则为氢氧化铝,反应Ⅲ是偏铝酸盐与铝盐发生双水解反应生成氢氧化铝,反应的离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓。


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
【题目】已知A是灰黑色、有金属光泽的固体单质。根据如图所示的物质之间的转化关系,回答下列有关问题。
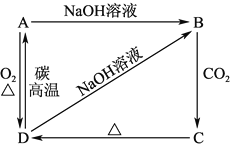 (少量)
(少量)
(1)写出A、B、C、D的化学式:A________,B________,C________,D________。
(2)写出D→A的化学方程式:___________________________________。
(3)写出B→C的离子方程式:___________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是
A. 该溶液的pH=4
B. 升高温度,溶液的pH增大
C. 此酸的电离平衡常数约为1×10-7
D. 由HA电离出的c(H+)约为水电离出的c(H+)的106倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述正确的是( )
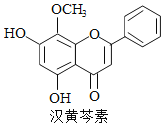
A. 汉黄芩素的分子式为C16H13O5
B. 该物质遇FeCl3溶液不显色
C. 1 mol该物质与溴水反应,最多消耗2 mol Br2
D. 与足量H2发生加成反应后,该分子中官能团的种类减少1种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物A:
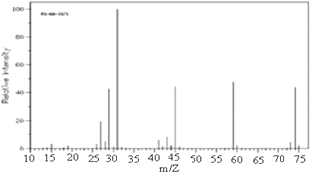
①由C、H、O三种元素组成,经燃烧分析实验测定其碳的质量分数是64.86%,氢的质量分数是13.51%;
②如图是该有机物的质谱图
③A的红外光谱图上有C-H键、O-H键、C-O键的振动吸收峰.
④A的核磁共振氢谱有两个峰.请回答:
(1)A的实验式(最简式)为_____________,分子式为_____________;
(2)已知A的最简式能否确定A的分子式(填“能”或“不能”)_______,为什么?________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有以下物质相互转化:
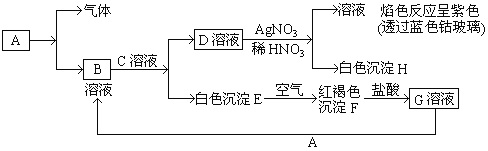
试回答
(1)写出C的化学式____________;
(2)A与水蒸气反应方程式为:__________________________ ;
(3)写出由E转变成F的化学方程式_______________________;
(4)鉴别G溶液中阳离子的方法是:____________________,现象为:________;用G溶液可以腐蚀铜印刷电路板,离子反应方程式为___________________________;
(5)金属铝与A的氧化物可用来焊接火车铁轨,实验室中该反应所需药品有_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有部分元素的原子结构特点如表:
X | L层电子数是K层电子数的3倍 |
Y | 核外电子层数等于原子序数 |
Z | L层电子数是K层和M层电子数之和 |
W | 最外层电子数是次外层电子数的2.5倍 |
(1)画出W原子结构示意图________________________。
(2)元素X与元素Z相比,非金属性较强的是________(填元素名称),写出一个能表示X、Z非金属性强弱关系的化学反应方程式:________________________________________。
(3)X、Y、Z、W四种元素形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为____________________。
(4)元素X和元素Y以原子个数比1∶1化合形成的化合物Q,写出Q的电子式________。元素W和元素Y化合形成的化合物M,Q和M的电子总数相等。以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的、且在自然界中稳定存在的物质,写出该反应的化学方程式:____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式正确的是
A. KH2PO4溶于水:H2PO4-![]() 2H++PO43-
2H++PO43-
B. NaHS溶于水:NaHS===Na++HS-,HS-![]() H++S2-
H++S2-
C. HF溶于水:HF===H++F-
D. NH4Cl溶于水:NH4++H2O![]() NH3·H2O+H+
NH3·H2O+H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com