
【题目】淀粉水解的产物(C6H12O6)用硝酸酸化可以制备草酸(H2C2O4),装置如图所示:
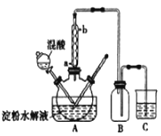
实验过程如下:
①将1:1的淀粉水乳液与少许98%硫酸加入烧杯中,水浴加热30 min;
②将一定量的淀粉水解液加入三颈烧瓶中;
③在5560℃条件下,缓慢滴加混酸(65%HNO3与98%H2S04的质量比为4 : 3)溶液;
④反应3h左右,冷却、过滤后再重结晶得二水合草酸晶体(H2C2O4·2H2O)。
硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3=3H2C2O4+9NO2↑+3NO↑+9 H2O
C6H12O6+8HNO3=6CO2↑+8NO↑+10H2O
C6H12O6+2HNO3=6CO2↑+2NO↑+4H2O
请回答下列问题:
(1)实硷①加入98%硫酸少许的目的是_____________。
(2)检验淀粉是否水解完全所用的试剂为____________。
(3)冷凝水的进口是_______(填“a”或“b”)。
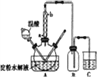
(4)装置B的作用为___________。
(5)实验中若混酸滴加过快,将导致草酸产量下降,其原因是______________。
(6)当尾气中n(NO2) :n(NO)=1:1时,过量的NaOH溶液能将氮氧化物全部吸收,只生成一种钠盐,化学方程式为__________。若用步驟④后含硫酸的母液来吸牧氮氧化物,其优点是_____,缺点是________。
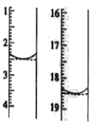
(7)二水合草酸晶体纯度的测定。称取该晶体0.12g,加水溶解,用0.020 mol L-1的酸性KMnO4溶液滴定(杂质不参与反应),该反应的离子方程式为 2MnO4-+5H2C2O4+6H+=2Mn2++10CO2+8H2O。此时溶液颜色由_____变为_____。滴定前后液面读数如图所示,则该晶体中二水合草酸的质量分数为____________。
【答案】 加快淀粉水解的速度(或起到催化剂的作用) 碘水 a 作安全瓶 硝酸浓度过大.导致葡萄糖被氧化为C〇2,且H2C2O4进一步被氧化 NO2+NO+2NaOH=2NaNO2+H2O 提高硝酸利用率(或循环使用氮氧化物): NOx (或循环使用氮氧化物)吸收不完全 无色 浅紫色 84.0%
【解析】(1)实硷①加入98%硫酸少许的目的是:淀粉水解时,硫酸能起到催化剂的作用,加快淀粉水解的速度;(2)检验淀粉是否水解完全所用的试剂为碘水,溶液由蓝色变为无色且30S不变色即水解完全;(3)选择a作为冷凝水入口,下进上出,可以加快冷凝速度;(4)装置B起到安全瓶的作用,防止尾气吸收时引起倒吸;(5)实验中温度过高 、硝酸浓度过大,都会导致H2C2O4进一步被氧化 ,故要控制混酸滴加速度;(6)当尾气中n(NO2) :n(NO)=1:1时,过量的NaOH溶液能将氮氧化物全部吸收,只生成一种钠盐亚硝酸钠(亚硝酸钠中氮的化合价为+3价,为二氧化氮和一氧化氮的中间价态),其化学方程式为:NO2+NO+2NaOH=2NaNO2+H2O;若用步驟④后含硫酸的母液来吸牧氮氧化物,其优点是提高硝酸利用率,循环使用氮氧化物,缺点是NOx吸收不完全;(7)用酸性高锰酸钾滴定草酸,当最后一滴酸性高锰酸钾溶液滴入时,显示其颜色,则溶液颜色由无色变为浅紫色,滴定前后液面读数如图所示,反应为:2MnO4- +5H2C2O4 + 6H+=2Mn2++10CO2+8H2O;则:
2MnO4- --------------------------------------------5H2C2O4
2 5
(18.5-2.5)×10-3×0.020mol/L n
解得n=0.8×10-3mol
故m(二水合草酸)=126g/mol×0.8×10-3mol=0.1008g
则该草酸晶体样品中二水合草酸的质量分数ω=![]() ×100% = 84.0%。
×100% = 84.0%。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在某无色透明的酸性溶液中,能大量共存的离子组是
A. Na+ 、K+、SO42-、CO32- B. Al3+、K+、SO42-、OH
C. Na+、 K+、Cl、 NO3 D. K+、Fe3+、MnO4-、I
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验设计及其对应的离子方程式均正确的是
A. 用铜电极电解NaCl溶液制备Cl2:2C1—+2H2O![]() Cl2↑+H2↑+2OH—
Cl2↑+H2↑+2OH—
B. 向MgCl2溶液中加入氨水制备Mg(OH)2:Mg2++2OH—==Mg(OH)2↓
C. 将FeS溶于稀硝酸制备Fe(NO3)3:FeS+4H++NO3==Fe3++NO↑+S↓+2H2O
D. 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4—+6H++5H2O2==2Mn2++5O2↑+8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图,下列说法正确的是( )
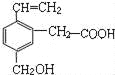
A. 该有机物的分子式为C11H15O3
B. 该有机物不能发生取代反应
C. 1 mol该物质与足量的钠反应可以生成1 mol氢气
D. 1 mol该有机物可以与1 mol碳酸钠发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A化学式为CxHyOz , 15 g A完全燃烧可生成22 g CO2和9 g H2O。试求:
(1)该有机物的最简式______________;
(2)若A的相对分子质量为60,且A和Na2CO3溶液反应有气体放出,A和醇能发生酯化反应, 则A的结构简式为_________________;
(3)若A的相对分子质量为60,且A是易挥发有水果香味的液体,能发生水解反应,则其结构简式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氯化砜(SO2Cl2)是一种无色液体,主要用于有机物和无机物的氯化等。其熔点为-54.1℃.沸点为69.2℃;常温下比较稳定,受热易分解,遇水剧烈反应生成硫酸和盐酸。
(1)制备。实验室可利用SO2和Cl2按下列装置制取少量SO2Cl2(丙中放有樟脑液,起催化作用)。已知SO2(g)+Cl2(g)![]() SO2Cl2(g) △H<0
SO2Cl2(g) △H<0
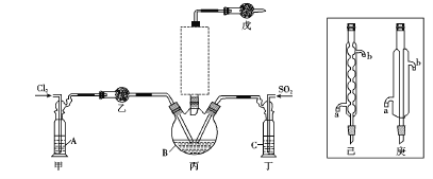
①可以用浓盐酸和酸性高锰酸钾制取氯气,该反应的化学方程式为 ;溶液A为 。
②上图实框中仪器己的名称为 ;反应装置图的虚框中未画出的仪器是 (填“己”或“庚”)。
③如果将丙装置放入冰水中,会更有利于二氯化砜的生成,其原因是 。
④下列有关说法错误的是 (填编号)。
a.乙、戊装置相同,在实验中的作用也完全相同
b.甲、丁装置为洗气装置,可用于气体的除杂和干燥
c.组装仪器后首先要进行的操作是检查装置的气密性
d.为提高反应物的利用率,可控制甲、丁装置中产生气泡的速率相等
(2)提纯。将收集到的产物进行减压蒸馏,减压蒸馏的目的是 。
(3)测定。取1.00g蒸馏后液体,小心地完全溶于水,向所得的溶液中加入足量氯化钡溶液,测得生成沉淀的质量为1.60g,则所得蒸馏成分中二氯化砜的质量百分含量为 %。
(4)贮存。二氯化砜应储存于阴凉、干燥、通风良好的库房。但久置后微显黄色,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组同学利用氧化还原反应:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,盐桥中装有饱和溶液。下列说法正确的是( )

A. a电极上发生的反应为:MnO4-+8H++5e-═Mn2++4H2O
B. 外电路电子的流向是从a到b
C. 电池工作时,盐桥中的SO42-移向甲烧杯
D. b电极上发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物E(结构简式为 )是合成消毒剂α——萜品醇(结构简式为
)是合成消毒剂α——萜品醇(结构简式为 )的中间体。由甲苯经一系列变化制取E的流程如下:
)的中间体。由甲苯经一系列变化制取E的流程如下:

请回答下列问题:
(1)化合物E中含有的官能团名称为________,α—萜品醇的分子式为_________,甲苯的结构简式为_____。
(2)反应I的化学方程式为____________。
(3)反应II的反应类型是__________________。
(4)反应III的试剂与条件为__________________。
(5)写出一种符合下列条件的有机物的结构简式_____________。
①是化合物D的一种同分异构体;②能与NaHCO3反应;③能与新制氢氧化铜浊液在加热条件下反应生成红色固体;④在核磁共振氢谱上有5个峰。
(6)下面是由化合物E合成一种α—萜品醇的流程的一部分,请将其中有G生成H的几步流程补充完整(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).________________。

提示:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com