
����Ŀ�������ӵ�����ԼΪ6.02��1023mol��1��������������ȷ����(����)
A. 7.8 g Na2S��Na2O2�Ļ�����к���������������0.1��6.02��1023
B. 2 mol NO��1 mol O2������ܱ������У����������ʷ�����С��2��6.02��1023
C. 6.8 g���ڵ�KHSO4�к���0.1NA��������
D. 1.00 mol NaCl�У�����Na����������������Ϊ10��6.02��1023
���𰸡�B
��������A. Na2S��Na2O2����Է�����������78�����������ӵĸ���֮�Ⱦ���1:2������7.8 g Na2S��Na2O2�Ļ�����к�����������Ϊ0.1��6.02��1023��A����B. 2 mol NO��1 mol O2������ܱ�����������2molNO2�������ڴ���ƽ���ϵ��2NO2![]() N2O4���������������ʷ�����С��2��6.02��1023��B��ȷ��C. ���ڵ�KHSO4����������Ӻ�����������ӣ�6.8 g���ڵ�KHSO4��6.8g��136g/mol��0.05mol�����к���0.05NA����������C����D. 1.00 mol NaCl�У�����Na����������������Ϊ8��6.02��1023��D����ѡB��
N2O4���������������ʷ�����С��2��6.02��1023��B��ȷ��C. ���ڵ�KHSO4����������Ӻ�����������ӣ�6.8 g���ڵ�KHSO4��6.8g��136g/mol��0.05mol�����к���0.05NA����������C����D. 1.00 mol NaCl�У�����Na����������������Ϊ8��6.02��1023��D����ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ʒ�ںϳɡ�ҽҩ��Ⱦ�ϵȹ�ҵ���й㷺��;����ṹʽ��ͼ��ʾ������ȩˮ��Һ�백ˮ����������Ƶ�������Ʒ����ԭ����ȫ��Ӧ����������Ʒ�����ȩ�백�����ʵ���֮��Ϊ

A. 1��1 B. 2��3 C. 3��2 D. 2��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�Ƚ�Fe3+��Cu2+��H2O2�ֽ�Ĵ�Ч����������ͬѧ�ֱ��������ͼһ��ͼ����ʾ��ʵ�顣
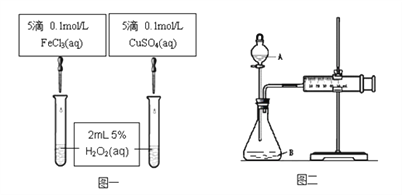
��1�� ͼһ��ͨ���۲�____________________���������ԱȽϵó����ۡ���ͬѧ�����CuSO4��ΪCuCl2��Ϊ��������������__________________������Ϊ���������������ָĽ��� _____________________��
��2�� ͼ�������ڶ����ȽϷ�Ӧ�Ŀ��������ͼ��װ�������Եķ�����________________��
����ͼ����ʵ��ʱ�������������_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A��1 mol�κ����ʶ�����6.02��1023������
B����״���£�1 mol H2��1 mol H2O��ռ�������ԼΪ22.4 L
C��HNO3��Ħ��������63 g
D��0.5 mol 13Hԭ�Ӻ��е�������ĿΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������1���pH=2.5��������10���ijһԪǿ����Һǡ����ȫ��Ӧ����ü���Һ��pH����(����)
A. 9.0 B. 9.5 C. 1 0.5 D. 1 1.0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.ij������ɫ��Ӧ�ʻ�ɫ���������п��ܺ���K+
B.�㷺pH��ֽ���ij������ˮ��pHΪ4
C.����240mLij��Һ��Ӧѡ240mL����ƿ
D.�����ű���ʳ��ˮ���ռ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڵ������Һ��������ȷ����
A. �����£�PH=7��NH4Cl�백ˮ�Ļ����Һ�У�c(Cl-)��c(NH4+)>c(H+)=c(OH-)
B. pH=11��NaOH��Һ��pH=3������Һ�������ϣ�����ʯ����Һ�ʺ�ɫ
C. ��PH��ͬ��������Ȼ����Һ��ˮ�ĵ���̶���ͬ
D. ��0.1mol/L�İ�ˮ�м�����������粒��壬����Һ��![]() ����
����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������ԭ�����͵���
A. �����ڳ�ʪ�Ŀ�������������
B. �غ�ɫNO2��ѹ����ɫ�ȱ�����dz
C. ���¼������������ʹ�ϳɰ��ķ�Ӧ���ʼӿ�
D. H2��I2��HIƽ��������ѹ����ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ�в����������ӵ���( )
A����ˮ B���Ȼ�����Һ C���������Һ D����84������ҺҺ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com