
【题目】依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题: 
(1)电极X的材料是 , 电解质溶液Y是;
(2)银电极为电池的极,发生的电极反应为 X电极上发生的电极反应为 .
(3)外电路中的电子是从电极流向电极.
【答案】
(1)Cu; AgNO3
(2)正;2Ag++2e﹣═2Ag; Cu﹣2e﹣═Cu2+
(3)Cu; Ag
【解析】解:(1)由反应2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)可知,在反应中,Cu被氧化,失电子,应为原电池的负极,所以X电极材料是Cu,Ag+在正极上得电子被还原,电解质溶液为AgNO3 ,
故答案为:Cu;AgNO3;(2)正极为活泼性较Cu弱的Ag,Ag+在正极上得电子被还原,电极反应为2Ag++2e﹣═2Ag,X(铜)电极失电子发生氧化反应,电极反应为Cu﹣2e﹣═Cu2+,
故答案为:正极; 2Ag++2e﹣=2Ag;Cu﹣2e﹣═Cu2+;(3)电子从负极Cu沿导线流向正极Ag,
故答案为:Cu;Ag.
(1)根据电池反应式知,失电子化合价升高的金属作负极,不如负极活泼的金属或导电的非金属作正极,得电子的化合价降低的可溶性反应物作电解质溶液,据此设计原电池;(2)原电池中,易失电子的电极铜为负极,银作正极,正极上得电子发生还原反应;(3)电子从负极沿导线流向正极.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
【题目】已知某反应A(g)+B(g)C(g)+D(g),反应过程中的能量变化如图所示,回答下列问题.
(1)该反应是反应(填“吸热”或“放热”),该反应的△H=kJ/mol(用含E1、E2的代数式表示),1mol 气体A和1mol气体B具有的总能量比1mol 气体C和1mol气体D具有的总能量(填“一定高”“一定低”或“高低不一定”).
(2)若在反应体系中加入催化剂使逆反应速率增大,则E1和E2的变化是:E1 , E2 , △H(填“增大”“减小”或“不变”).
(3)一般硫粉含有S(单斜)和S(正交)两种同素异形体.已知常温下: S(单斜)+O2(g)═SO2(g)△H=﹣297.16kJ/mol
S(正交)+O2(g)═SO2(g)△H=﹣296.83kJ/mol
下列说法正确的是
A.S(g)+O2(g)═SO2(g)△H>﹣297.16kJ/mol
B.单斜硫转变为正交硫的能量变化可用如图所示
C.常温下正交硫比单斜硫稳定
D.单斜硫转化为正交硫的反应是物理变化.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学一选修5: 有机化学基础】化合物G是重要的有机合成中间体,常用的合成路线如下:
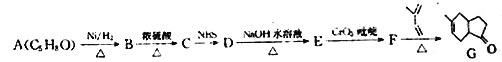
已知:①CH2==CH-CH3![]() CH2==CH-CH2-Br ②
CH2==CH-CH2-Br ②![]()
请回答下列问题:
(1)核微共振氢谱显示环状化合物A有两种化学环境的氢,则A 的结构简式为________,E→ F 的反应类型为_________________。
(2)合成线路中NBS 的作用是_________________________________________。
(3)请用“*”标出化合物G 中的手型碳原子 。______
。______
(4)写出D在NaOH 的醇溶液环境中加热的反应方程式(同一个碳原子不能连有两个双键)____________________________________________________。
(5)满足下列条件的E的同分异构体有______种。
a.能发生银镜反应 b.含有两种官能团
(6)请参考题中合成路线,设计由1-溴丁烷和必要的试剂合成1,3-丁二烯的路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明必要的试剂和反应条件)________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚石和石墨均为碳的同素异形体,它们燃烧氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示. 
(1)等量金刚石和石墨完全燃烧(填“金刚石”和“石墨”)放出热量更多,写出石墨完全燃烧的热化学方程式 .
(2)在通常状况下,金刚石和石墨(填“金刚石”和“石墨”)更稳定,写出石墨转化为金刚石的热化学方程式: .
(3)12g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分类是化学学习与研究的常用方法,下列分类正确的是( )
A. 混合物:水玻璃、氯水、福尔马林、聚乙烯
B. CO2、NO2、P2O5均为酸性氧化物,Na2O、Na2O2均为碱性氧化物
C. 根据能否发生丁达尔效应,将分散系分为溶液、胶体和浊液
D. 根据溶液导电能力强弱,将电解质分为强电解质和弱电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的沸点按由高到低的顺序排列正确的是
①CH3(CH2)2CH3 ②CH3(CH2)3CH3 ③(CH3)3CH ④(CH3)2CHCH2CH3
A.②④①③B.④②①③C.④③②①D.②④③①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,将一氧化氮、二氧化氮、氧气三种气体按一定比例充满一固定容积的容器,并将该容器倒置在水槽中,充分反应后,容器中无气体剩余,所得溶液的浓度为Mmol·L-1。则M的取值范围是( )
A. 0<M<![]() B.
B. ![]() <M<
<M<![]() C.
C. ![]() <M<
<M<![]() D.
D. ![]() <M<
<M<![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.4mol CuSO4和0.4mol NaCl溶于水,配成1L溶液,用惰性电极进行电解,当一个电极得到0.3mol Cu时,另一个电极上生成的气体在标准状况下的体积是( )
A.5.6L
B.6.72L
C.1.344L
D.11.2L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛因为其优越的性能被称为“未来金属”,其工业冶炼涉及到的反应如下:TiO2+2C+2Cl2![]() TiCl4+2CO
TiCl4+2CO
回答下列相关问题:
(1)钛的价层电子排布式为______________。
(2)已知部分物质熔沸点如下:
名称 | 金红石 | 金刚石 | 四氯化钛 | 四溴化钛 | 四碘化钛 |
化学式 | TiO2 | C | TiCl4 | TiBr4 | TiI4 |
熔点 | 1830℃ | 3550℃ | -24.1℃ | 38℃ | 150℃ |
沸点 | 2927℃ | 4827℃ | 136.4℃ | 233.1℃ | 377.2℃ |
晶型 | 离子晶体 | 分子晶体 | |||
表中金刚石的晶型为_________;自左向右,表中的三种钛的卤化物熔沸点依次升高的原因是_____________。
(3)配位数为6,组成为TiCl3·6H2O的晶体有两种:化学式为[TiCl(H2O)5]Cl2·H2O的X呈绿色,定量实验表明,X与AgNO3以1:2物质的量比反应生成沉淀。Y呈紫色,且Y与AgNO3以1:3物质的量比反应生成沉淀,则Y的化学式为___________,Y配离子的空间构型为_________。
(4)钙钛矿是重要的含钛矿物之一,其主要成分Z的晶胞如下图所示:
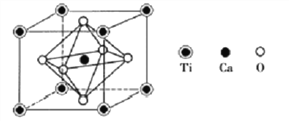
推测Z的化学式为________________。
(5)若晶胞参数a=384.1pm,Z晶体的密度为______g/cm3(已知NA≈6.0×1023;3.8413≈![]() )。
)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com