
在25℃的条件下,下列叙述正确的是
A.将稀氨水逐滴加入稀硫酸中,当溶液的pH=7时,c(SO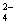 )= c(NH4+)
)= c(NH4+)
B.pH=3的醋酸溶液,稀释至原体积的10倍后pH=4
C.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,溶液pH<7
D.向0.1mol·L-1的氨水中加入少量硫酸铵固体,则溶液中c(OH-) 增大
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列说法中正确的是
A.离子晶体中每个离子周围均吸引着6个带相反电荷的离子
B.金属导电的原因是在外电场作用下金属产生自由电子,电子定向运动
C.分子晶体的熔沸点很低,常温下都呈液态或气态
D.原子晶体中的各相邻原子都以共价键相结合
查看答案和解析>>
科目:高中化学 来源: 题型:
通常情况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀。请回答:
(1)用化学符号表示下列4种微粒:
A: B : C: D :
(2)写出A、B、E三种微粒反应的离子方程式:
、
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是
A.非金属元素呈现的最高化合价不超过该元素原子的最外层电子数
B.非金属元素呈现的最低化合价,其绝对值等于元素原子的最外层最子数
C.最外层有2个电子的原子都是金属原子
D.最外层有5个电子的原子都是非金属原子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A H与D,16O与18O互为同位素;H216O、D216O、H218O、D218O互为同素异形体;甲醇、乙二醇和丙三醇互为同系物
B 在SiO2晶体中,1个Si原子和2个O原子形成2个共价键
C HI的相对分子质量大于HF,所以HI的沸点高于HF
D 由ⅠA族和ⅥA族元素形成的原子个数比为1∶1、电子总数为38的化合物,是含有共价键的离子型化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上也可以用CO2和H2反应制得甲醇。在2×105Pa、300℃的条件下,若有44g CO2与6g H2恰好完全反应生成气体甲醇和水,放出49.5kJ的热量。试写出该反应的热化学方程式: 。
某次实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如下图所示(实线)。
试回答下列问题:


(1)a点正反应速率 (填大于、等于或小于)逆反应速率。
(2)下列时间段平均反应速率最大的是 ,最小的是 。
A.0~1min
B.1~3min
C.3~8min
D.8~11min
(3)计算该实验平衡时氢气的转化率和该条件下反应的平衡常数K(写出计算过程)。
(4)仅改变某一实验条件再进行两次实验,测得H2的物质的量随时间变化如图中虚线所示,曲线I对应的实验条件改变是 ,曲线II对应的实验条件改变是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的数值。下列说法正确的是(用到的相对原子质量:H 1 O16 Al27)
A.18g 2H2O含有10NA个电子
B.1mol苯含有6NA个C-H键
C.常温常压下,22. 4L NH3约含有NA个NH3分子
D.27 g铝片投入足量浓H2SO4中生成1.5NA个SO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列过程或现象与水解无关的是
A.纯碱溶液去油污 B.配制氯化铁溶液时加入少量的盐酸
C.NaHCO3与Al2(SO4)3混合作泡沫灭火剂 D.铁在潮湿的环境下生锈
查看答案和解析>>
科目:高中化学 来源: 题型:
判断存放的FeCl2溶液是否变质。从现象观察看 ;鉴定的方法为加入 试剂,若溶液出现 ;则证明有 存在。实验室为了防止FeCl2溶液变质,在配制时常加入 。向FeSO4溶液中滴加NaOH溶液,并放置一段时间,此过程中观察到的现象 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com