
【题目】世界能源消费的90%以上依靠化学技术。请回答下列问题:
(1)质子交换膜燃料电池中作为燃料的H2通常来自水煤气。
已知:C(s)+![]() O2(g)=CO(g)ΔH1=-110.35kJ·mol-1
O2(g)=CO(g)ΔH1=-110.35kJ·mol-1
2H2(g)+O2(g)=2H2O(l)ΔH2=-571.6kJ·mol-1
H2O(l)=H2O(g)ΔH3=+44.0kJ·mol-1
①则反应C(s)+H2O(g)![]() CO(g)+H2(g) ΔH4=__________。
CO(g)+H2(g) ΔH4=__________。
②某实验小组在实验室模拟反应C(s)+H2O(g)CO(g)+H2(g),其平衡常数表达式为K=_______。一定温度下,在2L盛有足量炭粉的恒容密闭容器(固体所占体积忽略不计)中通入0.8molH2O,6min时生成0.7gH2,则6min内以CO表示的平均反应速率为________(保留3位有效数字)。
(2)燃料气(流速为1800mL·min-1;体积分数为50%H2,0.98%CO,1.64%O2,47.38%N2)中的CO会使电极催化剂中毒,使用CuO/CeO2催化剂可使CO优先氧化而脱除。
①160℃、CuO/CeO2作催化剂时,CO优先氧化的化学方程式为__________。
②CeO2可由草酸铈[Ce2(C2O4)3]隔绝空气灼烧制得,同时生成两种气体,则发生反应的化学方程式为____________。
③在CuO/CeO2催化剂中加入不同的酸(HIO3或H3PO4),测得燃料气中CO优先氧化的转化率随温度的变化如下图所示。
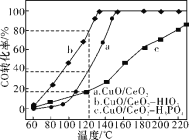
加入________(填酸的化学式)的CuO/CeO2催化剂催化性能最好。温度为120℃,催化剂为CuO/CeO2HIO3时,反应0.5h后CO的体积为______mL。
(3)LiOH是制备锂离子电池正极材料的重要原料,采用惰性电极电解制备LiOH的装置如下图所示。
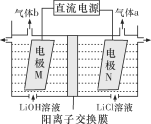
①通电后,Li+通过阳离子交换膜向________(填“M”或“N”)极区迁移。
②电极N产生的气体a通入淀粉-KI溶液,溶液变蓝,持续一段时间后,蓝色可逐渐褪去。据此写出电极N的电极反应式:___________;蓝色逐渐褪去是因为溶液中逐渐生成HIO3,写出此反应的化学方程式:_______。
【答案】+131.45kJ·mol-1 ![]() 0.0292mol·L-1·min-1 2CO+O2
0.0292mol·L-1·min-1 2CO+O2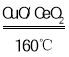 2CO2 Ce2(C2O4)3
2CO2 Ce2(C2O4)3![]() 2CeO2+4CO↑+2CO2↑ HIO3 105.84 M 2Cl--2e-=Cl2↑ 5Cl2+I2+6H2O=2HIO3+10HCl
2CeO2+4CO↑+2CO2↑ HIO3 105.84 M 2Cl--2e-=Cl2↑ 5Cl2+I2+6H2O=2HIO3+10HCl
【解析】
⑴①利用盖斯定律来计算反应C(s)+H2O(g) ![]() CO(g) +H2(g)的ΔH4;②根据方程式得到平衡常数表达式,再计算6min时生成H2质量和浓度,根据反应转化的c(CO)=c(H2),计算速率。
CO(g) +H2(g)的ΔH4;②根据方程式得到平衡常数表达式,再计算6min时生成H2质量和浓度,根据反应转化的c(CO)=c(H2),计算速率。
⑵①160℃、CuO/CeO2作催化剂时,CO优先氧化为CO2;②隔绝空气灼烧草酸铈[Ce2(C2O4)3]分解制得CeO2,同时生成CO和CO2;③相同时间内,CO的转化率越高,说明催化性能越好,由图象可知加入HIO3的CuO/CeO2催化剂催化性能最好;根据题知信息计算反应0.5h后CO的体积。
⑶电极N上产生的气体a通入淀粉-KI溶液,溶液变蓝,持续一段时间后,蓝色可逐渐褪去,则气体a为Cl2,电极N为阳极;电极M是阴极,电极N的电极反应式为2Cl--2e- = Cl2↑;蓝色逐渐褪去是因为溶液中逐渐生成HIO3,说明Cl2将I2氧化成了HIO3。
⑴①已知:①C(s)+![]() O2(g) = CO(g) ΔH1=-110.35kJ·mol-1;②2H2(g) +O2(g) = 2H2O(l) ΔH2=-571.6kJ·mol-1;③H2O(l)= H2O(g) ΔH3=+44.0kJ·mol-1。则反应C(s)+H2O(g)
O2(g) = CO(g) ΔH1=-110.35kJ·mol-1;②2H2(g) +O2(g) = 2H2O(l) ΔH2=-571.6kJ·mol-1;③H2O(l)= H2O(g) ΔH3=+44.0kJ·mol-1。则反应C(s)+H2O(g) ![]() CO(g) +H2(g) 可以通过①-②×
CO(g) +H2(g) 可以通过①-②×![]() -③得到,所以ΔH4=①-②×
-③得到,所以ΔH4=①-②×![]() -③=(-110.35kJ·mol-1)-(-571.6kJ·mol-1)×
-③=(-110.35kJ·mol-1)-(-571.6kJ·mol-1)×![]() -(+44.0kJ·mol-1)=+131.45kJ·mol-1。②反应C(s)+H2O(g)
-(+44.0kJ·mol-1)=+131.45kJ·mol-1。②反应C(s)+H2O(g) ![]() CO(g) +H2(g)的平衡常数表达式为
CO(g) +H2(g)的平衡常数表达式为![]() ;6min时生成0.7gH2,
;6min时生成0.7gH2,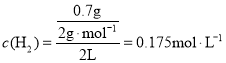 ,根据反应C(s)+H2O(g)
,根据反应C(s)+H2O(g) ![]() CO(g) +H2(g)可知,转化的c(CO)=c(H2),则6min内以CO表示的平均反应速率为
CO(g) +H2(g)可知,转化的c(CO)=c(H2),则6min内以CO表示的平均反应速率为![]() ;故答案为:+131.45kJ·mol-1;
;故答案为:+131.45kJ·mol-1;![]() ;0.0292mol·L-1·min-1。
;0.0292mol·L-1·min-1。
⑵①160℃、CuO/CeO2作催化剂时,CO优先氧化为CO2,方程式为2CO+O2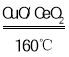 2CO2;故答案为:2CO+O2
2CO2;故答案为:2CO+O2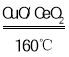 2CO2。
2CO2。
②隔绝空气灼烧草酸铈[Ce2(C2O4)3]分解制得CeO2,同时生成CO和CO2,反应方程式为Ce2(C2O4)3![]() 2CeO2+4CO↑+2CO2↑;故答案为:Ce2(C2O4)3
2CeO2+4CO↑+2CO2↑;故答案为:Ce2(C2O4)3![]() 2CeO2+4CO↑+2CO2↑。
2CeO2+4CO↑+2CO2↑。
③相同时间内,CO的转化率越高,说明催化性能越好,由图象可知加入HIO3的CuO/CeO2催化剂催化性能最好。120℃时,0.5h后CO的转化率是80%,燃料流速为1800mL·min-1,CO的体积分数为0.98%,则反应0.5h后CO的体积为1800mL·min-1×0.5h×60min·h-1×0.98%×(1-80%)=105.84mL;故答案为:HIO3;105.84。
⑶电极N上产生的气体a通入淀粉-KI溶液,溶液变蓝,持续一段时间后,蓝色可逐渐褪去,则气体a为Cl2,电极N为阳极;电极M是阴极,电极M上H+放电产生H2,促进水的电离,LiOH在M极区制得,Li+通过阳离子交换膜向M极区迁移。电极N为阳极,电极N的电极反应式为2Cl--2e- = Cl2↑;蓝色逐渐褪去是因为溶液中逐渐生成HIO3,说明Cl2将I2氧化成了HIO3,则Cl2被还原成HCl,反应的化学方程式为5Cl2+I2+6H2O = 2HIO3 +10HCl;故答案为:M;2Cl--2e-=Cl2↑;5Cl2+I2+6H2O=2HIO3+10HCl。


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
【题目】某化学小组以苯甲酸为原料,制取苯甲酸甲酯,已知有关物质的沸点如下表:
物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 | |
沸点/℃ | 64.7 | 249 | 199.6 | |
密度/g.cm-3 | 0.792 | 1.2659 | 1.0888 | |
Ⅰ.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入12.2 g苯甲酸和20 mL甲醇(密度约为0.79 g·cm-3),再小心加入3 mL浓硫酸,混匀后,投入几块碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品。
(1)浓硫酸的作用是______________;若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式:_________________________________________。
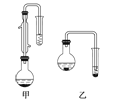
(2)甲和乙两位同学分别设计了如图所示的两套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去)。根据有机物的沸点,最好采用__________装置(填“甲”或“乙”)
(3)反应物CH3OH应过量,理由是__________________________。
Ⅱ.粗产品的精制
(4)苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用下列流程图进行精制,请在流程图中方括号内填入操作方法的名称。

(5)通过计算,苯甲酸甲酯的产率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂—铜空气燃料电池(如图)容量高、成本低,该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为:2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法错误的是

A. 整个反应过程中,氧化剂为O2
B. 放电时,正极的电极反应式为:Cu2O+H2O+2e-=2Cu+2OH-
C. 放电时,当电路中通过0.1 mol电子的电量时,有0.1 mol Li+透过固体电解质向Cu极移动,有标准状况下1.12 L氧气参与反应
D. 通空气时,铜被腐蚀,表面产生Cu2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种形状像布袋结构的烯烃分子,其形状和结构如图所示,有关说法不正确的是( )

A. 该烯烃的分子式为C5H4
B. 该分子所有碳原子在同一平面
C. 1 mol该有机物最多可与2 mol Br2发生加成反应
D. 与其互为同分异构体且只含三键的链烃不止—种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Z是一种常见的工业原料,实验室制备Z的化学方程式如下图所示。下列说法正确的是( )
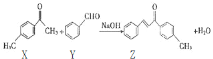
A.1molZ最多能与7molH2反应
B.Z分子中的所有原子一定共平面
C.可以用酸性KMnO4溶液鉴别X和Y
D.X的同分异构体中含有苯环和醛基的结构有14种(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下述转化关系,回答问题:

已知:①+CH3Br![]() CH3+HBr;
CH3+HBr;
②C物质苯环上一卤代物只有两种。
(1)写出B物质的名称__________;D物质的结构简式________。
(2)写出反应②的类型________;反应⑤的条件________。
(3)写出反应⑥的化学方程式:________________________________。
(4)写出D+E反应的化学方程式:_______________。
(5)反应②还有可能生成一种C16H18的有机物,其苯环上一卤代物也只有两种,写出它的结构简式:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,下列说法正确的是( )
A.0.1 mol·L-1 (NH4)2SO4溶液中c(![]() )<c(
)<c(![]() )
)
B.0.02 mol·L-1氨水和0.01 mol·L-1氨水中的c(OH-)之比是2∶1
C.向醋酸钠溶液中加入醋酸使溶液的pH=7,此时混合液中c(Na+)>c(CH3COO-)
D.向0.1 mol·L-1 NaNO3溶液中滴加盐酸使溶液的pH=5,此时混合液中c(Na+)=c(![]() )(不考虑酸的挥发与分解)
)(不考虑酸的挥发与分解)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向10 mL ![]() 溶液中滴加
溶液中滴加![]() 的
的![]() 溶液,滴加过程中,溶液中
溶液,滴加过程中,溶液中![]() 与
与![]() 溶液体积(V)的关系如图所示,下列说法正确的是( )已知:
溶液体积(V)的关系如图所示,下列说法正确的是( )已知: ![]() 。
。

A. 该温度下 ![]()
B. X、Y、Z三点中,Y点水的电离程度最小
C. ![]() 溶液中:
溶液中:![]()
D. 向100 mL ![]() 浓度均为
浓度均为![]() 的混合溶液中逐滴加入
的混合溶液中逐滴加入![]() 的
的![]() 溶液,
溶液,![]() 先沉淀
先沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A. 苯酚钠溶液中通入少量的二氧化碳,产物是苯酚和碳酸钠
B. 苯的同系物中,苯环和侧链相互影响,使得二者均易被氧化
C. ![]() 在核磁共振氢谱中出现两组峰,其氢原子数之比为3:2
在核磁共振氢谱中出现两组峰,其氢原子数之比为3:2
D. 苯甲醛、苯乙烯分子中的所有原子可能处于同一平面
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com