
【题目】图为H2与O2反应生成H2O(g)的能量变化示意图:

下列有关叙述不正确的是
A. 1molH2分子断键需要吸收436kJ的能量
B. H2(g)+1/2O2(g)=H2O(g)ΔH=-241.8kJ/mol
C. 分解1mol气态水生成氢气和氧气总共需要吸收926.8kJ的热量
D. 形成化学键释放的总能量比断裂化学键吸收的总能量大
【答案】C
【解析】
A、化学键断裂需要吸收能量,1molH2分子断键需要吸收436kJ的能量,选项A正确;
B、H2(g)+![]() O2(g)═H2O(g)反应焓变=反应物总键能-生成物总键能=(436+
O2(g)═H2O(g)反应焓变=反应物总键能-生成物总键能=(436+![]() ×498-2×463.4)=-241.8kJ/mol,标注物质聚集状态和对应反应焓变写出热化学方程式为,H2(g)+
×498-2×463.4)=-241.8kJ/mol,标注物质聚集状态和对应反应焓变写出热化学方程式为,H2(g)+![]() O2(g)═H2O(g)△H=-241.8kJ/mol,选项B正确;
O2(g)═H2O(g)△H=-241.8kJ/mol,选项B正确;
C、根据热反应方程式H2(g)+![]() O2(g)═H2O(g)△H=-241.8kJ/mol可知,分解1mol气态水生成氢气和氧气总共需要吸收483.6kJ的热量,选项C不正确;
O2(g)═H2O(g)△H=-241.8kJ/mol可知,分解1mol气态水生成氢气和氧气总共需要吸收483.6kJ的热量,选项C不正确;
D、反应为放热反应,依据能量守恒可知,形成化学键释放的总能量比断裂化学键吸收的总能量大,选项D正确;
答案选C。


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
【题目】计算:
(1)用14.2g无水硫酸钠配制成500mL溶液,其物质的量浓度为____mol·L-1。
(2)若从中取出50mL,其物质的量浓度为____mol·L-1;溶质的质量为___g。
(3)若将这50mL溶液用水稀释到100mL,所得溶液中Na+的物质的量浓度为____mol·L-1,SO42-的物质的量浓度为_____mol·L-1。
(4)已知:a g某气体A含有b个分子,则c g该气体在标准状况下的体积为____ L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑
B. 铁片与氯化铜溶液反应:Fe+Cu2+=Cu+Fe2+
C. 氢氧化镁溶于盐酸:Mg(OH)2+H+=Mg2++H2O
D. Cu(OH)2与稀硫酸反应:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,pH 均为2的两种一元酸HA和HB各1mL,分别加水稀释,pH 随溶液体积的变化曲线如图所示。下列说法正确的是

A. HA的酸性比HB的酸性弱
B. a点溶液的导电性比c点溶液的导电性弱
C. 若两溶液加水稀释,则所有离子的浓度都减小
D. 对a、b两点溶液同时升高温度,则c(A-)/c(B-)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气作为清洁能源有着广泛的应用前景,含硫天然气制备氢气的流程如下。

请回答下列问题:
I.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如下。
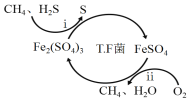
(1)过程i的离子反应方程式为_________________________________________。
(2)已知:
①Fe3+在pH=l.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如下表。
pH | 0.7 | 1.1 | 1.5 | 1.9 | 2.3 | 2.7 |
Fe2+的氧化速率/g·L-1·h-1 | 4.5 | 5.3 | 6.2 | 6.8 | 7.0 | 6.6 |
在转化脱硫中,请在上表中选择最佳pH范围是_______<pH<_______,这样选择的原因是:_______________________________________________。
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合下图回答问题。
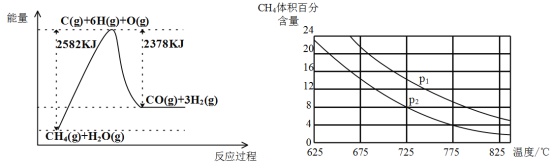
(3)①该过程的热化学方程式是__________________________________________。
②比较压强P1和p2的大小关系:P1 _________ P2(选填“>”“<”或“=”)。
③在一定温度和一定压强下的体积可变的密闭容器中充入1molCH4和1mol的水蒸气充分反应达平衡后,测得起始时混合气的密度是平衡时混合气密度的1.4倍,若此时容器的体积为2L,则该反应的平衡常数为______________(结果保留2位有效数字)。
Ⅲ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅳ.H2提纯:将CO2和H2分离得到H2的过程如示意图
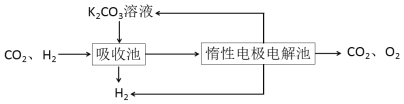
(4)吸收池中发生反应的离子方程式是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,某反应达平衡,平衡常数K=c(CO).c(H2O)/[c(CO2).c(H2)]。保持容器容积不变,升高温度,H2浓度减小,则下列说法不正确的是
A. 该反应的焓变为正值
B. 恒温恒容下,再充入CO2气体,H2浓度一定减小
C. 升高温度,会使正反应速率增大,逆反应速率减小,平衡正移
D. 该反应化学方程式为CO2+H2![]() CO+H2O
CO+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,在容积为2L的恒容密闭容器中,将2molN气体和3molM气体相混合,发生如下反应:2N(g)+3M(g)![]() xQ(g)+3R(g),4s后该反应达平衡时,生成2.4molR,并测得Q的反应速率为0.1mol/(L·s),下列有关叙述正确的是
xQ(g)+3R(g),4s后该反应达平衡时,生成2.4molR,并测得Q的反应速率为0.1mol/(L·s),下列有关叙述正确的是
A. N的转化率为80% B. 0~4s内,混合气体的平均相对分子质量不变
C. x值为2 D. 平衡时M的浓度为0.6mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苦杏仁酸在医药工业可用于合成头孢羟唑、羟苄唑、匹莫林等的中间体,下列路线是合成苦杏仁酸及其衍生物的一种方法:

(1)试写出B的结构简式_____,C中官能团的名称为_____。
(2)反应①的反应类型为_____,D的核磁共振氢谱共有_____组峰。
(3)1molE最多可以与_____molNaOH反应。反应③的化学方程式为_____。
(4)两个C分子可以反应生成具有三个六元环的化合物F,则F的结构简式为_____。
(5)写出满足下列条件的C的同分异构体的结构简式_____。
A.既能发生银镜反应,又能发生水解反应
B.遇FeCl3能显紫色
C.苯环上具有两个位于对位的取代基
(6)已知:RCH2COOH![]() RCHClCOOH,请以冰醋酸为原料(无机试剂任选)设计制备聚乙醇酸(
RCHClCOOH,请以冰醋酸为原料(无机试剂任选)设计制备聚乙醇酸(![]() )的合成路线_____。
)的合成路线_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com