
【题目】肼(N2H4)又称联氨,广泛用于火箭推进剂、有机合成及燃料电池,NO2的二聚体N2O4则是火箭中常用氧化剂.试回答下列问题 
(1)肼燃料电池原理如图所示,N2H4通入的一极应为电池的极(填“正”或“负”).
(2)火箭常用N2O4作氧化剂,肼作燃料,已知: N2(g)+2O2(g)═2NO2(g)△H=﹣67.7kJmol﹣1
N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=﹣534.0kJmol﹣1
2NO2(g)N2O4(g)△H=﹣52.7kJmol﹣1
试写出气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式 .
(3)联氨的工业生产常用氨和次氯酸钠为原料获得,也可用尿素[CO(NH2)2]和次氯酸钠﹣氢氧化钠溶液反应获得,请写出尿素法反应的离子方程式为 .
【答案】
(1)负
(2)2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=﹣947.6kJ?mol﹣1
(3)CO(NH2)2+ClO﹣+2OH﹣=N2H4+CO32﹣+Cl﹣+H2O
【解析】解:(1)燃料电池中负极发生氧化反应,正极发生还原反应,依据图中装置可知,肼在反应中失去电子生成氮气发生氧化反应,所以N2H4通入的一极应为电池的负极,通入氧气的一极为正极;
所以答案是:负;(2)由N2(g)+2O2(g)=2NO2(g)△H=﹣67.7kJmol﹣1①
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=﹣534.0kJmol﹣1 ②
2NO2(g)N2O4(g)△H=﹣52.7kJmol﹣1 ③根据盖斯定律可知②×2﹣①﹣③得2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g),△H=(﹣534.0kJmol﹣1)×2﹣(﹣67.7kJmol﹣1)﹣(﹣52.7kJmol﹣1)=﹣947.6 kJmol﹣1,
即热化学方程式为2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=﹣947.6 kJmol﹣1,所以答案是:2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=﹣947.6 kJmol﹣1;(3)由在高锰酸钾催化剂存在下,尿素和次氯酸钠、氢氧化钠溶液反应生成联氨、另外两种盐和水,根据质量守恒定律可知两种盐为氯化钠和碳酸钠,该反应为CO(NH2)2+ClO﹣+2OH﹣=N2H4+CO32﹣+Cl﹣+H2O,
所以答案是:CO(NH2)2+ClO﹣+2OH﹣=N2H4+CO32﹣+Cl﹣+H2O;


科目:高中化学 来源: 题型:
【题目】如图为阳离子交换膜法以石墨为电极电解饱和食盐水原理示意图.据图判断下列说法不正确的是( ) 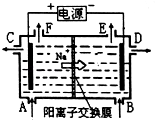
A.标准状况下,生成22.4LCl2的同时有2molNaOH生成
B.从C口流出的是NaOH溶液
C.从E口逸出的气体是H2
D.从F口逸出的气体是Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为以惰性电极进行电解的装置: 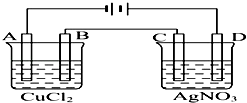
(1)写出A、B、C、D各电极上的电极反应式和总反应方程式: A: , B: , 总反应方程式:;
C: , D: , 总反应方程式: .
(2)在A、B、C、D各电极上析出生成物的物质的量之比为 .
(3)A极发生反应,B极发生反应.(填“氧化”或是“还原”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiOOH+2H2O ![]() Cd(OH)2+2Ni(OH)2有关其说法正确的是( )
Cd(OH)2+2Ni(OH)2有关其说法正确的是( )
A.充电过程是化学能转化为电能的过程
B.放电时负极附近溶液的碱性不变
C.放电时电解质溶液中的OH﹣向正极移动
D.充电时阳极反应:Ni(OH)2﹣e﹣+OH﹣=NiOOH+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质一定属于同系物的是( ) ① ![]() ②
② ![]() ③
③ ![]() ④C2H4 ⑤CH2=CH﹣CH=CH2⑥C2H6⑦
④C2H4 ⑤CH2=CH﹣CH=CH2⑥C2H6⑦  ⑧
⑧ 
A.④和⑧
B.①、②和③
C.⑤、⑦和⑧
D.⑥和⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A.常温常压下,1mol丙烷共用电子对数为10 NA
B.0.5 mol甲烷和0.5 mol乙酸完全燃烧消耗的O2分子数都为0.2NA
C.标准状况下,1L辛烷充分燃烧后生成气态产物的分子数为 ![]() NA
NA
D.1 mol甲醇与足量钠反应,转移电子数目为2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(CH3OCH3)是一种重要的清洁燃料气,其储运、燃烧安全性、理论燃烧温度等性能指标均优于液化石油气,也可用作燃烧电池的燃料,具有很好的好展前景.
(1)已知H2、CO和CH3OCH3的燃烧热(△H)分别为﹣285.5kJ/mol、﹣283kJ/mol和﹣1460.0kJ/mol,则工业上利用水煤气成分按1:1合成二甲醚的热化学方程式为
(2)工业上采用电浮远凝聚法处理污水时,保持污水的pH在5.0,通过电解生成Fe(OH)3胶体,吸附不溶性杂质,同时利用阴极产生的H2 , 将悬浮物带到水面,利于除去.实验室以二甲醚燃料电池模拟该方法设计的装置如图所示: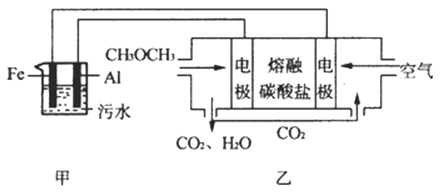
①乙装置以熔融碳酸盐为电解质,稀土金属材料为电极.写出该燃料电池的正极电极反应式 下列物质可用做电池熔融碳酸盐的是
A.MgCO3 B.Na2CO3 C.NaHCO3 D.(NH4)CO3
②写出甲装置中阳极产物离子生成Fe(OH)3沉淀的离子方程式:
③已知常温下Kap[Fe(OH)3]=4.0×10﹣38 , 电解一段时间后,甲装置中c(Fe3+)=
④已知:H2S的电离平衡常数:K1=9.1×10﹣8、K2=1.1×10﹣12;H2CO3的电离平衡常数:K1=4.31×10﹣7、K2=5.61×10﹣11 . 测得电极上转移电子为0.24mol时,将乙装置中生成的CO2通入200mL 0.2mol/L的Na2S溶液中,下列各项正确的是
A.发生反应的离子方程式为:CO2+S2﹣+H2O═CO32﹣+H2S
B.发生反应的离子方程式为:CO2+S2﹣+H2O═HCO3﹣+HS﹣
C.c(Na+)=2[c(H2S)+c(HS﹣)+c(S2﹣)]
D.c(Na+)+c(H+)=2c(CO32﹣)+2c(S2﹣)+c(OH﹣)
E.c(Na+)>c(HCO3﹣)>c(HS﹣)>c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在25℃、101kPa下,1g C8H18(l)燃烧生成CO2和液态H2O时放出48.40kJ的热量,表示上述反应的热化学方程式正确的是( )
A.C8H18(l)+ ![]() O2(g)═8CO2(g)+9H2O(g)△H=﹣48.40 kJmol﹣1
O2(g)═8CO2(g)+9H2O(g)△H=﹣48.40 kJmol﹣1
B.C8H18(l)+ ![]() O2(g)═8CO2(g)+9H2O(l)△H=﹣5 517.6 kJmol﹣1
O2(g)═8CO2(g)+9H2O(l)△H=﹣5 517.6 kJmol﹣1
C.C8H18(l)+ ![]() O2(g)═8CO2(g)+9H2O(g)△H=+5 517.6 kJmol﹣1
O2(g)═8CO2(g)+9H2O(g)△H=+5 517.6 kJmol﹣1
D.2C8H18(l)+25O2(g)═16CO2(g)+18 H2O(l)△H=﹣5 517.6 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组准备用环己醇制备环己烯,查得相关资料如下.反应原理:  反应物与产物的物理性质:
反应物与产物的物理性质:
密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | ﹣103 | 83 | 难溶于水 |
(1)实验过程中可能发生的有机副反应的方程式为 .
(2)根据上述资料,装置(A,B,C)最适宜用来完成本次制备实验. 
(3)制备粗产品 将5mL加入试管A中,再加入10m , 摇匀后放入碎瓷片,缓慢加热至反应完全.
(4)粗产品提纯 ①环己烯粗产品中含有环己醇和少量酸性杂质等.粗产品需依次经过水洗、加碳酸钠溶液洗涤以及第二次水洗.在此过程中加入碳酸钠溶液的目的是;分液时,环己烯应从分液漏斗的(填“上”或“下”)口取出.
②向水洗后的环己烯中加入少量的无水氯化钙,再将混合物放入图D所示装置的(填仪器名称)中,进行蒸馏,收集产品时,温度计显示的温度应为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com