
【题目】Ⅰ.某实验小组对H2O2的分解做了如下探究。下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同的粉末状和块状的MnO2分别加入盛有15 ml 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5min |
块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30min |
(1)写出上述实验中发生反应的化学方程式:______。
(2)实验结果表明,催化剂的催化效果与_____有关。
(3)某同学在10 mL H2O2 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的反应速率最慢的是_____。

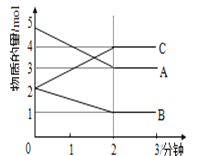
Ⅱ.某反应在体积为5L的恒容密闭容器中进行, 在0-3分钟内各物质的量的变化情况如图所示(A,B,C均为气体,且A气体有颜色)。
(4)该反应的的化学方程式为__________。
(5)反应开始至2分钟时,B的平均反应速率为____。
(6)能说明该反应已达到平衡状态的是____。
a.v(A)= 2v(B) b.容器内各物质的物质的量相等
c.v逆(A)=v正(C) d.容器内气体的颜色保持不变
(7)由图求得平衡时A的体积分数______。
【答案】2H2O2 ![]() 2H2O + O2↑ 催化剂的表面积 C 2A + B
2H2O + O2↑ 催化剂的表面积 C 2A + B ![]() 2C 0.1mol·(L·min)-1 cd 37.5%
2C 0.1mol·(L·min)-1 cd 37.5%
【解析】
Ⅰ.(1)二氧化锰是过氧化氢分解的催化剂,由带火星木条复燃,可知产物,由此可写出方程式;
(2)由实验现象可知催化剂作用大小的影响因素;
(3)A、B、C三点的斜率代表反应速率,斜率越大,反应速率越大;
Ⅱ.(4)从物质的物质的量的变化趋势判断反应物和生成物,根据物质的物质的量变化值等于化学计量数之比书写化学方程;
(5)化学反应速率是单位时间内浓度的变化,据此可求得反应速率;
(6)可逆反应达到平衡状态时,正逆反应速率相等,各组分浓度不再变化,若存在有色物质,则有色物质的颜色也不再变化,据此对各选项进行判断;
(7)根据![]() ,可求得平衡时A的体积分数.
,可求得平衡时A的体积分数.
:(1)上述实验中发生反应的化学方程式为:![]() ;
;
(2)时间少,则反应速率快,则实验结果表明,催化剂的催化效果与催化剂的表面积有关,故答案为:催化剂的表面积;
(3)由图可知,曲线斜率变小,反应速率减小,则A、B、C三点所表示的反应速率最慢的是C,故答案为:C;
Ⅱ.(4)由图象可以看出,A、B的物质的量逐渐减小,则A、B为反应物,C的物质的量逐渐增多,所以C为生成物,当反应到达2min时,△n(A)=2mol,△n(B)=1mol,△n(C)=2mol,化学反应中,各物质的物质的量的变化值与化学计量数呈正比,则△n(A):△n(B):△n(C)=2:1:2,故答案为:![]() ;
;
(5)由图象可以看出,反应开始至2分钟时,△n(B)=1mol,B的平均反应速率为:![]() =0.1mol/(Lmin),故答案为:0.1mol/(Lmin);
=0.1mol/(Lmin),故答案为:0.1mol/(Lmin);
(6)a.v(A)=2v(B)不能说明正反应和逆反应的关系,故无法判断反应是否达到平衡,故a错误;
b.容器内各物质的物质的量相等,不能说明各组分的浓度不再变化,无法判断是否达到平衡状态,故b错误;
c.在该反应中A和C的计量数相等,当v逆(A)=v正(C)时,正逆反应速率相等,说明反应已达平衡状态了,故c正确;
d.只有A为有色物质,当容器内气体的颜色保持不变,说明各组分的浓度不再变化,该反应已经达到平衡状态,故d正确;
故答案为:cd;
(7)由图象可知:达平衡时A的物质的量为3mol,平衡时总物质的量为1mol+3mol+4mol=8mol,
所以A的体积分数为![]() ,故答案为:37.5%;
,故答案为:37.5%;


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知反应H2(g)+ ![]() O2(g)=H2O(g)的能量变化如图所示,a、b、c表示能量变化,为正值,单位为kJ,下列说法正确的是 ( )
O2(g)=H2O(g)的能量变化如图所示,a、b、c表示能量变化,为正值,单位为kJ,下列说法正确的是 ( )
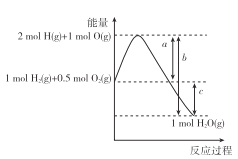
A. H2(g)+ ![]() O2(g)=H2O(g) △H=c kJ·mol-1
O2(g)=H2O(g) △H=c kJ·mol-1
B. 2H2O(g)=2H2 (g)+O2 (g) △H=—2(a-b) kJ·mol-1
C. 1 mol氢气与0.5 mol氧气总能量为akJ
D. 2 mol氢气与1 mol氧气完全反应生成2 mol液态水放出的热量小于2(b-a)kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业合成氨反应:N2+3H2![]() 2NH3是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1 mol H-H键、1 mol N-H键、1 mol N≡N键放出能量分别为436 kJ、391 kJ、946 kJ。则:
2NH3是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1 mol H-H键、1 mol N-H键、1 mol N≡N键放出能量分别为436 kJ、391 kJ、946 kJ。则:
(1)若1 mol N2完全反应生成NH3可________(填“吸收”或“放出”)热量________kJ。
(2)如果将1 mol N2和3 mol H2混合,使其充分反应,放出的热量总小于上述数值,其原因是________________________。
(3)实验室模拟工业合成氨时,在容积为2 L的密闭容器内,反应经过10 min后,生成10 mol NH3,则用N2表示的化学反应速率为________mol·L-1·min-1。
(4)一定条件下,当合成氨的反应达到化学平衡时,下列说法正确的是________。
a.正反应速率和逆反应速率相等
b.正反应速率最大,逆反应速率为0
c.N2的转化率达到最大值
d.N2和H2的浓度相等
e.N2、H2和NH3的体积分数相等
f.反应达到最大限度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某稀溶液中含有0.2 mol HNO3和x mol H2SO4,向其中加入25.6 g铜粉,充分反应后产生的气体在标准状况下的体积为4.48 L,则x值至少为( )
A.0.6B.0.4C.0.3D.0.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1.52 g铜镁合金完全溶解于50 mL 14 mol/L的浓硝酸中,得到NO2和N2O4的混合气体1120 mL(标准状况),向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是( )
A.该合金中铜与镁的物质的量之比是2:1
B.得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL
C.NO2和N2O4的混合气体中,NO2的体积分数是80%
D.与铜镁合金反应的HNO3的物质的量为0.12 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有以下物质相互转化,试回答:

(1)写出B的化学式_______________,D的化学式_______________________。
(2)写出由B转变成E的化学方程式_____________________________。
(3)写出用KSCN鉴别G溶液的离子方程式______________;向G溶液加入A的有关离子反应方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】木炭跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图所示装置)。下列有关说法不正确的是( )

A.洗气瓶中产生的沉淀是碳酸钡B.在Z导管出来的气体中有二氧化碳
C.洗气瓶中产生的沉淀是硫酸钡D.在Z导管口有红棕色气体出现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氯酸钾熔化,粒子间克服了________的作用力;二氧化硅熔化,粒子间克服了________的作用力;碘的升华,粒子间克服了________的作用力。三种晶体的熔点由高到低的顺序是______(填化学式)。
(2)下列六种晶体:①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,它们的熔点从低到高的顺序为________(填序号)。
(3)在H2、(NH4)2SO4、SiC、CO2、HF中,由极性键形成的非极性分子是________,由非极性键形成的非极性分子是________,能形成分子晶体的物质是________,含有氢键的晶体的化学式是__________,属于离子晶体的是_________,属于原子晶体的是_______,五种物质的熔点由高到低的顺序是__________。
(4)A、B、C、D为四种晶体,性质如下:
A 固态时能导电,能溶于盐酸
B 能溶于CS2,不溶于水
C 固态时不导电,液态时能导电,可溶于水
D 固态、液态时均不导电,熔点为3 500℃
试推断它们的晶体类型:
A.______;B.______;C.________;D._____。
(5)相同压强下,部分元素氟化物的熔点见下表:
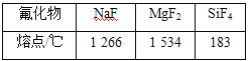
试解释上表中氟化物熔点差异的原因:__________
(6)镍粉在CO中低温加热,生成无色挥发性液态Ni(CO)4,呈四面体构型。150 ℃时,Ni(CO)4分解为Ni和CO。Ni(CO)是________晶体,Ni(CO)4易溶于下列________(填序号)
a 水 b 四氯化碳 c 苯 d 硫酸镍溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 反应A(g)+3B(g)![]() 2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率
2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率
分别如下,其中反应速率最大的是( )
A.v(C)=0.04 mol/(L·s)
B.v(B)=0.06 mol/(L·min)
C.v(A)=0.15 mol/(L·min)
D.v(D)=0.01 mol/(L·s)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com