
【题目】研究表明:丰富的CO2可以作为新碳源,解决当前应用最广泛的碳源(石油和天然气)枯竭危机,同时又可缓解由CO2累积所产生的温室效应,实现CO2的良性循环。
(1)目前工业上有一种方法是用CO2加氢合成低碳烯烃。现以合成乙烯(C2H4)为例、该过程分两步进行:
第一步:CO2(g)+H2(g)![]() CO(g)+H2O(g) △H =+41.3kJ·mol-1
CO(g)+H2O(g) △H =+41.3kJ·mol-1
第二步:2CO(g)+4H2(g)![]() C2H4(g)+2H2O(g) △H =-210.5kJ·mol-1
C2H4(g)+2H2O(g) △H =-210.5kJ·mol-1
①CO2加氢合成乙烯的热化学方程式为_____________________________。
②一定条件下的密闭容器中,上述反应达到平衡后,要加快反应速率并提高CO2的转化率,可以采取的措施是______(填字母)。
A.减小压强 B.增大H2浓度 C.加入适当催化剂 D.分离出水蒸气
(2)另一种方法是将CO2和H2在230℃催化剂条件下生成甲醇蒸气和水蒸气。现在10L恒容密闭容器中投入1molCO2和2.75molH2,发生反应:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)。在不同条件下测得平衡时甲醇的物质的量随温度、压强的变化如图所示:
CH3OH(g)+H2O(g)。在不同条件下测得平衡时甲醇的物质的量随温度、压强的变化如图所示:

①能判断该反应达到化学平衡状态的是_______(填字母)。
a.c(H2):c(CH3OH)=3:1 b.容器内氢气的体积分数不再改变
C.容器内气体的密度不再改变 d.容器内压强不再改变
②上述反应的△H______0(填“>”或“<”),图中压强p1____p2(填“>”或“<”)。
③经测定知Q点时容器的压强是反应前压强的9/10,则Q点H2的转化率为____________。
④N点时,该反应的平衡常数K=______(计算结果保留两位小数)。
(3)用生石灰吸收CO2可生成难溶电解质CaCO3,其溶度积常数Ksp=2.8×10-9。现有一物质的量浓度为2×10-4mol/L纯碱溶液,将其与等体积的CaCl2溶液混合,则生成沉淀所需CaCl2溶液的最小浓度为___mol/L。
【答案】2CO2+6H2(g) ![]() C2H4(g)+4H2O(g) △H= -127.9 kJ/mol B bd < > 20.5% 1.04 5.6×10-5
C2H4(g)+4H2O(g) △H= -127.9 kJ/mol B bd < > 20.5% 1.04 5.6×10-5
【解析】
(1)①根据两个反应方程式,消去CO,整理并计算反应的△H,正确答案:
2CO2+6H2(g) ![]() C2H4(g)+4H2O(g) △H= -127.9 kJ/mol。
C2H4(g)+4H2O(g) △H= -127.9 kJ/mol。
②减小压强,各物质的浓度减少,平衡左移,CO2的转化率降低,反应速率减慢,A错误;增大H2浓度,平衡右移,浓度增大,速率加快,CO2的转化率增大,B正确;加入适当催化剂,能够加快反应速率,但是平衡不动,CO2的转化率不变,C错误;分离出水蒸气,减少生成物浓度,速率减慢,但是平衡右移,CO2的转化率增大,D错误;正确选项B。
(2)①c(H2):c(CH3OH)=3:1 这仅仅是是反应的过程中一种情况,无法判定反应是否达平衡状态,a错误;容器内氢气的体积分数不再改变,可以判断反应达平衡状态,b正确;反应前后气体的总质量不变,容器的体积恒定,容器内气体的密度恒为定值,无法判定反应达到化学平衡状态,C错误;该反应为气体的总量减少的反应,当容器气体的总量不再发生变化,容器内的压强也不再改变,可以判定反应达到化学平衡状态,d正确;正确选项:bd。
②从图像看出,温度升高,n(CH3OH)减少,平衡左移,该反应正反应为放热反应,△H<0;当温度不发生改变,压强由p2→p1,增大压强平衡右移,n(CH3OH)增大,所以压强p1>p2,正确答案:< ; >。
③设二氧化碳的消耗量为xmol,根据方程式进行计算如下:
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。
起始量 1 2.75 0 0
变化量 x 3x x x
平衡量 1- x 2.75-3x x x
反应后气体总量为1-x+2.75-3x+x+x=(3.75-2x)mol,反应前气体总量为1+2.75=3.75 mol,根据压强比等于物质的量之比:(3.75-2x)/3.75=9/10, x=0.1875 mol, Q点H2的转化率为3×0.1875÷2.75×100%= 20.5%,正确答案:20.5%。
④ 10L恒容密闭容器中投入1molCO2和2.75mol,反应进行到506℃,达平衡状态,对应M点时,甲醇的量为0.25mol,进行如下计算:
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。
起始量 1 2.75 0 0
变化量 0.25 0.75 0.25 0.25
平衡量 0.75 2 0.25 0.25
各物质浓度分别为c(CO2)= 0.075 mol/L, c(H2)= 0.2 mol/L , c(CH3OH)= c(H2O)= 0.025 mol/L, 该反应的平衡常数K=(0.025)2/(0.23×0.075)= 1.04 ;由于N 和M处于同一温度下的不同曲线上两点,所以平衡常数相同,正确答案:1.04。
(3)设CaCl2溶液的最小浓度为为cmol/L,两溶液等体混合,溶液的浓度均减半,带入溶度积常数Ksp的计算公式:Ksp= c(Ca2+)c(CO32-)=(c÷2)×(2×10-4÷2)= 2.8×10-9,解之,c=5.6×10-5 mol/L;正确答案:5.6×10-5。


 应用题作业本系列答案
应用题作业本系列答案 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
【题目】以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图所示。下列说法正确的是
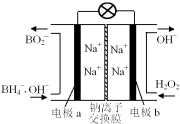
A.电池放电时Na+从b极区移向a极区
B.该电池的负极反应为:BH4-+8OH--8e-===BO2-+6H2O
C.电极a采用MnO2,MnO2既作电极材料又有催化作用
D.每消耗3 mol H2O2,转移的电子为3 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量变化示意图,下列说法不正确的是

A. 该反应的热化学方程式为N2(g)+3H2(g)![]() 2NH3(g) △H =-92kJ·mol-1
2NH3(g) △H =-92kJ·mol-1
B. 若在反应体系中加入高效催化剂,E1、E2和△H均减小
C. 若已知H-H的键能和N-H的键能,可求得N![]() N的键能
N的键能
D. 反应2NH3(g)![]() N2(g)+3H2(g)的△S>0
N2(g)+3H2(g)的△S>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别取50mL 0.5mol/L的盐酸溶液与50mL 0.55mol/L的氢氧化钠溶液进行中和热测定实验。下列操作和说法不正确的是

A. 稍过量的氢氧化钠是确保盐酸完全反应
B. 向盛装盐酸的烧杯中小心缓慢地加入氢氧化钠溶液
C. 仪器A的名称是环形玻璃搅拌棒
D. 在实验过程中,把温度计上的酸用水冲洗干净后再测量氢氧化钠溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用Na2CO3·10H2O晶体配制0.20 mol/L Na2CO3溶液480 mL。
(1)实验时要用到的玻璃仪器有:除托盘天平、量筒、烧杯、玻璃棒、胶头滴管外,至少还必须用到的一种玻璃仪器是___________________,在使用该仪器前必须进行的操作是_______________________。
(2)应用托盘天平称取Na2CO3·10H2O晶体的质量为___________g。
(3)配制溶液时有以下几个操作:

简述定容的过程:_______________________________。
(4)配制过程中,下列操作对所配溶液的浓度有什么影响,完成填空。
a.Na2CO3·10H2O晶体不纯,混有NaCl
b.用“左码右物”的称量方法称量晶体
c.容量瓶中洗净后未干燥,残留少量水
d.未冷却至室温就转移定容
e.加蒸馏水时不慎超过了刻度线,立即用胶头滴管将多余的水吸出
f.定容时,俯视刻度线
会引起所配溶液的浓度偏大的有________,无影响的有________。(填序号)
(5)如果直接使用浓度为2.00mol/L的Na2CO3溶液来配制100mL 1.00mol/L的Na2CO3溶液,需要量取2.00mol/L的Na2CO3溶液的体积为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质的叙述错误的是
A. 将过量氨气通入CuSO4溶液中可得深蓝色溶液
B. 蛋白质溶于水所得分散系可产生丁达尔效应
C. 硅酸钠溶液与稀盐酸反应可生成硅酸胶体
D. 过量铁粉在氯气中燃烧可生成氯化亚铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表所示:
电解质 | 醋酸 | 碳酸 | 亚硫酸 |
电离常数 | K=1.75×10-5 | K1=4.30×10-7 K2=5.61×10-11 | K1=1.00×10-2 K2=1.02×10-7 |
(1)写出亚硫酸的第一级电离平衡常数表达式:K1=_____________________。
(2)已知NaHSO3溶液显酸性,写出溶液中离子浓度大小_____________________。
(3)Na2CO3溶液去油污的原因: _____________________。(用化学用语表示)
(4)在相同条件下,试比较①CH3COONa ②NaHCO3 ③Na2SO3水溶液的碱性强弱:(填序号)_____________________。
(5)若保持温度不变,在醋酸溶液中加入少量醋酸钠,下列量会变小的是_________。(填序号)
A.c(CH3COO-) B.c(H+) C.醋酸电离平衡常数 D.醋酸的电离程度
(6)NaHSO3水解反应的平衡常数Kb=_______________ molL-1。
(7)H2SO3溶液和NaHCO3溶液反应的主要离子方程式为_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com