
【题目】【化学—选修3物质结构与性质】
Ⅰ.已知砷化镓的晶胞结构如图所示。请回答下列问题:

(1)下列说法正确的是__________(填序号)。
A.砷化镓晶胞结构与NaCl相同
B.第一电离能As>Ga
C.电负性As>Ga
D.原子半径As>Ga
(2)砷化镓可由(CH3)3Ga和AsH3在700℃下反应制得,反应的方程式为:__________________________。
(3)AsH3空间形状为___________;已知(CH3)3Ga为非极性分子,则其中镓原子的杂化方式为____________。
Ⅱ.金属铜的导电性仅次于银,居金属中的第二位,大量用于电气工业。
(4)请解释金属铜能导电的原因___________________,Cu2+的核外电子排布式为________________。
(5)在硫酸铜溶液中通入过量的氨气,小心蒸发,最终得到深蓝色的[Cu(NH3)4]SO4晶体,晶体中含有的化学键除普通共价键外,还有_________和_________。
【答案】 BC (CH3)3Ga+AsH3![]() GaAs+3CH4 三角锥 sp2 铜是金属晶体,由金属阳离子和自由电子构成,自由电子在外加电场的作用下可发生定向移动 [Ar]3d9或1s22s22p63s23p63d9 离子键 配位键
GaAs+3CH4 三角锥 sp2 铜是金属晶体,由金属阳离子和自由电子构成,自由电子在外加电场的作用下可发生定向移动 [Ar]3d9或1s22s22p63s23p63d9 离子键 配位键
【解析】(1)A项,GaAs晶体中As分布于晶胞体心,Ga分布于顶点和面心,而如图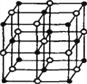 NaCl中阴阳离子分别位于晶胞的顶点、面心以及棱和体心,二者结构不同,故A错误;B项,同周期元素从左到右第一电离能逐渐增大,所以第一电离能:As>Ga,故B正确;C项,同周期元素从左到右电负性逐渐增大,所以电负性:As>Ga,故C正确;D项,同周期从左到右原子半径减小,所以原子半径As<Ga,故D错误。综上,选BC。
NaCl中阴阳离子分别位于晶胞的顶点、面心以及棱和体心,二者结构不同,故A错误;B项,同周期元素从左到右第一电离能逐渐增大,所以第一电离能:As>Ga,故B正确;C项,同周期元素从左到右电负性逐渐增大,所以电负性:As>Ga,故C正确;D项,同周期从左到右原子半径减小,所以原子半径As<Ga,故D错误。综上,选BC。
(2)由已知,反应物为(CH3)3Ga和AsH3,一种生成物为GaAs,根据原子守恒还应有CH4,反应在700℃下进行,化学方程式为:(CH3)3Ga+AsH3![]() GaAs+3CH4。
GaAs+3CH4。
(3)As原子最外层5个电子,AsH3中含有3个δ键和1个孤电子对,为三角锥形,Ga最外层3个电子,(CH3)3Ga中Ga形成3个δ键,没有孤电子对,为sp2杂化。
(4)金属铜能导电是因为铜是金属晶体,由金属阳离子和自由电子构成,自由电子在外加电场的作用下可发生定向移动,从而导电;Cu是29号,故Cu2+的核外电子排布式为[Ar]3d9或1s22s22p63s23p63d9。
(5)[Cu(NH3)4]SO4晶体属于配合物,配离子与硫酸根之间形成离子键、铜离子与氨分子之间形成配位键。


科目:高中化学 来源: 题型:
【题目】下表所列物质晶体的类型全部正确的一组是( )
原子晶体 | 离子晶体 | 分子晶体 | |
A | 石墨 | 磷酸 | 单质硫 |
B | 单晶硅 | 硫 | 白磷 |
C | 金刚石 | 纯碱 | 冰 |
D | 铁 | 过氧化钠 | 冰醋酸 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下有关物质结构的描述正确的是
A. 甲苯分子中的所有原子可能共平面
B. 乙烷分子中的所有原子可能共平面
C. CH2=CH—C6H5分子中的所有原子可能共平面
D. 二氯甲烷分子为正四面体结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 分子数为NA的CO和C2H4混合气体的体积约为22.4 L
B. 标准状况下,4.48 L重水(D2O)中含有的中子数为2NA
C. 用MnO2与浓盐酸制取Cl2时,每生成0.5mol Cl2则转移电子数为NA
D. 0.1 L 3.0 mol·L-1的NH4NO3溶液中含有NH![]() 的数目为0.3NA
的数目为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于过氧化钠的说法正确的是( )
A. 过氧化钠在常温下的颜色为白色 B. 阴阳离子之比为1:1
C. 与水反应过氧化钠作氧化剂,水作还原剂 D. 1mol与足量的二氧化碳反应转移的电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 分子数为NA的CO和C2H4混合气体的体积约为22.4 L
B. 标准状况下,4.48 L重水(D2O)中含有的中子数为2NA
C. 用MnO2与浓盐酸制取Cl2时,每生成0.5mol Cl2则转移电子数为NA
D. 0.1 L 3.0 mol·L-1的NH4NO3溶液中含有NH![]() 的数目为0.3NA
的数目为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关离子方程式书写正确的是
A. Na2CO3溶液除去锅炉中水垢(CaSO4): Ca2++CO32-═CaCO3↓
B. 用惰性电极电解饱和硫酸铜溶液:2Cu2++2H2O![]() 2Cu+O2↑+4H+
2Cu+O2↑+4H+
C. 铝溶于氢氧化钠溶液:Al+2OH-+H2O=AlO2-+2H2↑
D. 用H2O2从酸化的海带灰浸出液中提取碘:2I-+H2O2=I2+2OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com