
【题目】糖类、油脂、蛋白质是人体重要的能源物质,请根据它们的性质回答以下问题:
(1)油脂在酸性和碱性条件下水解的共同产物是____________(写名称)。
(2)蛋白质的水解产物具有的官能团是____________和____________(写结构简式)。
(3)葡萄糖是一种重要的单糖,其分子结构中除含有五个羟基外还含有的官能团是____________(写结构简式)
【答案】甘油或丙三醇 —NH2 —COOH —CHO
【解析】
(1)油脂在酸性条件下的水解产物为高级脂肪酸和甘油,在碱性条件下的水解产物为高级脂肪酸钠和甘油;
(2)蛋白质的水解产物是氨基酸;
(5)葡萄糖是一种单糖,是一种多羟基的醛;
(1)油脂在酸性条件下的水解产物为高级脂肪酸和甘油(或丙三醇),在碱性条件下的水解产物为高级脂肪酸钠和甘油(或丙三醇),故油脂在酸性和碱性条件下水解的共同产物是甘油(或丙三醇);
(2)蛋白质的水解产物是氨基酸,氨基酸分子中含有的官能团为氨基(![]() )和羧基(
)和羧基(![]() );
);
(3)葡萄糖的分子式为C6H12O6,其结构简式为HOCH2(CHOH)4CHO,故葡萄糖分子中除含有五个羟基外还含有的官能团是醛基(![]() )。
)。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】现有一瓶A和B的混合液,已知A和B的某些性质如下:
物质 | 分子式 | 熔点℃ | 沸点℃ | 密度 | 水溶性 |
A | C2H6O2 | -98 | 57.5 | 0.93 | 可溶 |
B | C4H8O2 | -84 | 77 | 0.90 | 可溶 |
由此,分离A和B的最佳方法是( )
A.分馏B.升华C.萃取D.分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,2.24L![]() 中含有的极性键数目为0.2
中含有的极性键数目为0.2![]()
B. 13.8g![]() 和
和![]() 的混合气体与足量水反应,转移的电子数为0.2
的混合气体与足量水反应,转移的电子数为0.2![]()
C. 足量铜与含0.2mol![]() 的浓硫酸反应,生成
的浓硫酸反应,生成![]() 分子数为0.1
分子数为0.1![]()
D. 常温下,pH均为4的![]() 溶液和
溶液和![]() 溶液各1L,水电离出的
溶液各1L,水电离出的![]() 数目均为
数目均为![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜、锌及其化合物用途广泛。回答下列问题:
(1)Zn2+的价层电子轨道表达式为__。
(2)元素第二电离能(I2):Zn_Cu(填“>”“<”或“=”)。
(3)卤化锌的熔点如表所示:
ZnF2 | ZnCl2 | ZnBr2 | ZnI2 | |
溶点/℃ | 872 | 275 | 394 | 446 |
①ZnCl2、ZnBr2、ZnI2的熔点呈表中变化规律的原因___。
②ZnF2的熔点远高于其它三种卤化锌,其原因为___。
(4)邻氨基吡啶(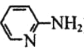 )的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。
)的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。
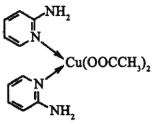
①邻氨基吡啶的铜配合物中,C原子杂化类型为__。
②1mol![]() 中σ键和π键的数目之比为__。
中σ键和π键的数目之比为__。
(5)铜的晶胞为面心立方(如图所示),已知晶胞参数为a,则该晶胞的空间利用率为__。(圆周率为π)。
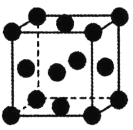
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究小组探究外界条件对化学反应mA(g)+nB(g)![]() pC(g)的速率和平衡的影响,图像如下,下列判断正确的是( )
pC(g)的速率和平衡的影响,图像如下,下列判断正确的是( )
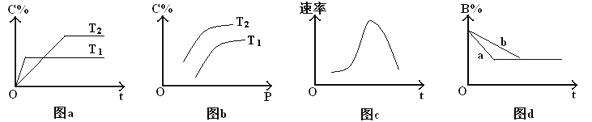
A. 由图a可知,T1>T2,该反应的逆反应为吸热反应
B. 由图b可知,该反应m+n<p
C. 图c是绝热条件下速率和时间的图像,由此说明该反应吸热
D. 图d中,若m+n=p,则曲线a一定增大了压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25gL-1。某兴趣小组用图1装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定。
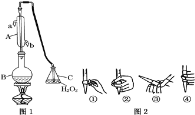
(1)仪器A的名称是 ______,水通入A的进口为 ______。
(2)B中加入300.00mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,其化学方程式为 ______
(3)除去C中过量的H2O2,然后用0.090 0molL-1NaOH标准溶液进行滴定,滴定前排气泡时,应选择图2中的 ______ ;若滴定终点时溶液的pH=8.8,则选择的指示剂为 ______ ;若用50mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积(填序号) ______ (①=10mL;②=40mL;③<10mL;④>40mL)
(4)滴定至终点时,消耗NaOH溶液25.00mL,该葡萄酒中SO2含量为:______ gL-1。
(5)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施:______。
(6)常温下,用一定量的NaOH溶液吸收逸出的SO2气体,吸收后的吸收液恰好呈中性,下列关于吸收液的说法正确的是______
A. ![]()
B. ![]()
C. ![]()
D. ![]()
E. 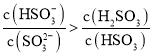
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
A.在干冰晶体中,每一个二氧化碳分子周围有12个二氧化碳分子紧密相邻
B.金刚石网状结构中,由共价键构成的碳原子环中,最小的环上有4个碳原子
C.熔点由高到低的顺序是:金刚石>碳化硅>晶体硅
D.在12g金刚石晶体中,含共价键为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 合成氨反应放热,采用低温可以提高氨的生成速率
B. 常温下,将pH=4的醋酸溶液加水稀释,溶液中所有离子的浓度均降低
C. 反应4Fe(OH)2(s)+2H2O(l)+O2(g)===4Fe(OH)3(s)常温下能自发进行,该反应的ΔH<0
D. 在一容积可变的密闭容器中反应2SO2(g)+O2(g)![]() 2SO3(g)达平衡后,保持温度不变,缩小体积,平衡正向移动,
2SO3(g)达平衡后,保持温度不变,缩小体积,平衡正向移动,![]() 的值增大
的值增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“侯氏制碱法”是我国化工专家候德榜为世界制碱工业作出的突出贡献。某实验小组模拟“侯氏制碱法”的工艺流程及实验装置(部分夹持装置省略)如下:

下列叙述错误的是
A. 实验时先点燃装置①的酒精灯,过一段时间后再打开装置③中分液漏斗的旋塞
B. 装置②的干燥管中可盛放蘸稀硫酸的脱脂棉,作用是吸收多余的NH3
C. 向步骤Ⅰ所得滤液中通入氨气,加入细小的食盐颗粒并降温,可析出NH4Cl
D. 用装置④加热碳酸氢钠可实现步骤Ⅱ的转化,所得CO2可循环使用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com