
【题目】医生建议患甲状腺肿大的病人多吃海带,这是由于海带中含较丰富的( )
A.碘元素
B.铁元素
C.钾元素
D.锌元素
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在25℃时,密闭容器中X,Y,Z三种气体的起始浓度和平衡浓度如表,下列说法错误的是( )
物质 | X | Y | Z |
初始浓度/molL﹣1 | 0.1 | 0.2 | 0 |
平衡浓度/molL﹣1 | 0.05 | 0.05 | 0.1 |
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y2Z,平衡常数为1600
C.其他条件不变时,增大压强可使平衡常数增大
D.改变温度可以改变该反应的平衡常数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、F是家庭中常见的有机物,A可以用来除去暖瓶或水壶中的水垢;E是石油化工发展水平的标志,F是一种常见的高分子材料。根据下面转化关系回答下列问题:
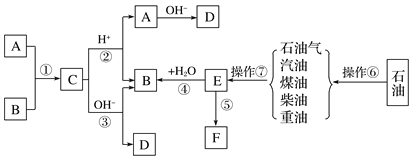
(1)操作⑥、操作⑦的名称分别为________________、________________。
(2)E的结构简式为_________。
(3)B的官能团名称为________,对B的描述正确的是________。
①有毒 ②无色无味 ③密度比水小 ④与酸性高锰酸钾溶液反应使其褪色
⑤在海带提碘实验中作萃取剂从碘水中提取碘单质
⑥在热Cu丝作用下生成相对分子质量比它小2的有机物
A.①③⑤ B.②③④ C.③④⑥ D.④⑤⑥
(4)写出下列反应的化学方程式:
①写出不含18O的A与用18O标记的B在一定条件下发生反应的化学方程式(注明条件和18O的位置):
_______________________________________________________________________,
④E和水反应生成B的方程式(注明条件):
_______________________________________________________________________,
⑤作为家庭中常见的物质,高分子化合物F给我们带来了极大的方便,同时也造成了环境污染,反应⑤的方程式为:___________________________________________________________,
写出有机物B遇到红热的铜丝在空气中反应的化学方程式:
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的反应方程式正确的是( )
A.亚硫酸钠水溶液显碱性:SO32﹣+2H2O?H2SO3+2OH﹣
B.SO2的水溶液显酸性:SO2+H2O?H2SO3?2H++SO32﹣
C.燃煤时加入石灰石减少SO2排放:2CaCO3+2SO2+O2 ![]() 2CaSO4+2CO2
2CaSO4+2CO2
D.浓NaOH溶液处理少量二氧化硫:SO2+OH﹣═HSO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有25℃时pH=12的NaOH溶液100mL.,欲用以下几种方法将其pH调整到11,回答下列问题(已知混合后溶液的总体积等于混合前两稀溶液的体积之和):
(1)25℃时,pH=12的NaOH溶液中由水电离产生的c(OH﹣)=
(2)加水稀释,需加水的体积为mL.
(3)加入pH=2的盐酸,需加盐酸的体积为mL.(精确到0.1)
(4)加入pH=10的NaOH溶液,需加NaOH溶液的体积为mL.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质分类正确的是( )
①混合物:盐酸、王水、水玻璃、水银
②化合物:CaCl2、烧碱、聚苯乙烯、O3
③电解质:H2SO4、胆矾、冰醋酸、硫酸钡
④同素异形体:C60、C70、金刚石、石墨
A. ①③ B. ②④ C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[选修3:物质结构与性质]
(1)19-Ⅰ 下列叙述正确的有( )
A.某元素原子核外电子总数是最外层学@科网电子数的5倍,则其最高正价为+7
B.钠元素的第一、第二电离能分别小于镁元素的第一、第二电离能
C.高氯酸的酸性与氧化性均大于次氯酸的酸性和氧化性
D.邻羟基苯甲醛的熔点低于对羟基苯甲醛的熔点
(2)19-Ⅱ ⅣA族元素及其化合物在材料等方面有重要用途。回答下列问题:
1)碳的一种单质的结构如图(a)所示。该单质的晶体类型为 , 原子间存在的共价键类型有 , 碳原子的杂化轨道类型为。


2)SiCl4分子的中心原子的价层电子对数为 , 分子的立体构型为 , 属于分子(填“极性”或“非极性”)。
3)四卤化硅SiX4的沸点和二卤化铅PbX2的熔点如图(b)所示。
①SiX4的沸点依F、Cl、Br、I次序升高的原因是。
②结合SiX4的沸点和PbX2的熔点的变化规律,可推断:依F、Cl、Br、I次序,PbX2中的化学键的离子性、共价性。(填“增强”“不变”或“减弱”)
4)碳的另一种单质C60可以与钾形成低温超导化合物,晶体结构如图(c)所示。K位于立方体的棱上和立方体的内部,此化合物的化学式为;其晶胞参数为1.4 nm,晶体密度为
g·cm-3。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com