
【题目】POCl3广泛用于染料等工业。某化学学习小组借助拉瓦锡研究空气成分的曲颈甑(装置甲)合成PC13,并采取PCl3氧化法制备POCl3。
已知:(1)PCl3的熔点为-112℃,沸点为75.5℃,遇水生成H3PO3和HCl;
(2)2PCl3+O2==2POCl3。
【实验Ⅰ】制备PCl3
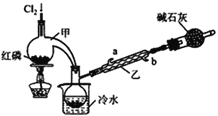
(1)实验室制备Cl2的原理是________________________。
(2)碱石灰的作用除了处理尾气外还有________________________。
(3)装置乙中冷凝水从_____(选填a或b)进入。
【实验Ⅱ】制备POCl3
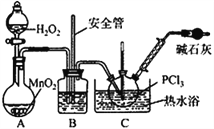
(4)实验室常用有微孔的试剂瓶保存H2O2,“微孔”与上述装置中的___________(仪器名称)目的是一致的。
(5)C中反应温度控制在60~65℃,其原因是________________________。
【实验Ⅲ】测定POCl3含量
①准确称取30.70gPOC13产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解;
②将水解液配成100.00mL溶液,取10.00mL溶液于锥形瓶中;
③加入10.00mL3.200mol/LAgNO3标准溶液,并加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖;
④以Fe3+ 为指示剂,用0.2000mol/LKSCN 溶液滴定过量的AgNO3溶液,达到滴定终点时共用去10.00 mL KSCN 溶液。
已知:Ag++SCN-==AgSCN↓ Ksp(AgCl)>Ksp(AgSCN )。
(6)POC13水解的化学反应方程式为________________________。
(7)滴定终点的现象为____________,用硝基苯覆盖沉淀的目的是________________________。
(8)反应中POC13的百分含量为________________。
【答案】 MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O 防止空气中的水蒸气进入烧瓶,提高产品纯度 a 安全管 一是温度过高,PCl3会大量挥发,从而导致产量降低;二是温度过低,反应速率会变慢 POCl3+3H2O=H3PO4+3HCl 当最后一滴标准KSCN溶液滴入时,溶液变为红色,且半分钟不褪去 使生成的沉淀与溶液隔离,避免滴定过程中SCN-与AgCl反应 50%
MnCl2+Cl2↑+2H2O 防止空气中的水蒸气进入烧瓶,提高产品纯度 a 安全管 一是温度过高,PCl3会大量挥发,从而导致产量降低;二是温度过低,反应速率会变慢 POCl3+3H2O=H3PO4+3HCl 当最后一滴标准KSCN溶液滴入时,溶液变为红色,且半分钟不褪去 使生成的沉淀与溶液隔离,避免滴定过程中SCN-与AgCl反应 50%
【解析】(1)实验室常用浓盐酸与二氧化锰加热制备Cl2,反应的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)根据装置图,PCl3遇水容易发生水解反应生成H3PO3和HCl;碱石灰的作用除了处理尾气外,还可以防止空气中的水蒸气进入烧瓶,提高产品纯度,故答案为:防止空气中的水蒸气进入烧瓶,提高产品纯度;
(3)装置乙中冷凝水应该遵循下进上出,从a口进,b口出,故答案为:a;
(4)双氧水容易分解,实验室常用有微孔的试剂瓶保存H2O2,可以起到平衡气压的作用,“微孔”与上述装置中的安全管的目的是一致的,故答案为:安全管;
(5)根据题意,PCl3的熔点为-112℃,沸点为75.5℃,C中反应温度控制在60~65℃,如果温度过高,PCl3会大量挥发,从而导致产量降低;如果温度过低,反应速率会变慢,故答案为:一是温度过高,PCl3会大量挥发,从而导致产量降低;二是温度过低,反应速率会变慢;
(6)PCl3遇水容易发生水解反应生成H3PO3和HCl,水解的化学反应方程式为POCl3+3H2O=H3PO4+3HCl,故答案为:POCl3+3H2O=H3PO4+3HCl;
(7)以硫酸铁溶液为指示剂,用KSCN溶液滴定过量的AgNO3溶液达到终点时的现象是溶液变红色,用硝基苯覆盖沉淀可以使生成的沉淀与溶液隔离,避免滴定过程中SCN-与AgCl反应,影响测定结果,故答案为:当最后一滴标准KSCN溶液滴入时,溶液变为红色,且半分钟不褪去;使生成的沉淀与溶液隔离,避免滴定过程中SCN-与AgCl反应;
(8)KSCN的物质的量为0.2mol/L×0.01L=0.002mol,根据反应Ag++SCN-=AgSCN↓,可知溶液中剩余的银离子的物质的量为0.002mol,POCl3与水反应生成氯化氢的物质的量为3.2mol/L×0.01L-0.002mol=0.030mol,根据POCl3+3H2O=H3PO4+3HCl,POCl3的物质的量为![]() =0.010mol,30.70gPOCl3产品中POCl3的物质的量为0.1mol,所以产品中POC13的百分含量为
=0.010mol,30.70gPOCl3产品中POCl3的物质的量为0.1mol,所以产品中POC13的百分含量为![]() ×100%=50%,故答案为:50%。
×100%=50%,故答案为:50%。


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】阿塞那平用于治疗精神分裂症,可通过以下方法合成(部分反应条件略去);

(1)阿塞那平中的含氧官能团为_______(填官能团的名称)。由F→阿塞那平的反应类型为______________。
(2)化合物X的分子式为C4H9NO2,则由B→C反应的另一产物的化学式_______________________。
(3)由D生成E的过程中先后发生加成反应和消去反应,则加成反应后中间体的结构简式为____________。
(4)写出同时满足下列条件的B的一种同分异构体的结构简式:________。
I.属于芳香化合物,分子中含有5种不同化学环境的氢;
II.能发生银镜反应和水解反应,水解产物能与FeCl3溶液发生显色反应。
(5)已知: ![]() ,卤代烃碱性条件下不与醇反应。请写出以CH3Cl、CH3NH2和
,卤代烃碱性条件下不与醇反应。请写出以CH3Cl、CH3NH2和![]() 为原料制备
为原料制备 的合成路线流程图(无机试剂任用)。_____________
的合成路线流程图(无机试剂任用)。_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时在10mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/LHCl溶液,溶液中含碳微粒的物质的量分数随溶液pH的变化如下图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法正确的是
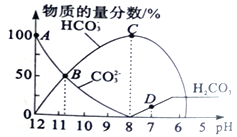
A. A点时,溶液中c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-)
B. B点时,溶液中c(Na+)>c(CO32-)=c(HCO3-)>(H+)>c(OH-)
C. C点时,溶液中浓度最大的离子是 Na+
D. D点时,溶液的pH为7,溶液的总体积为20mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列递变关系错误的是
A.原子半径:Si>P>S>ClB.最高化合价:C<N<O<F
C.碱性:NaOH>Mg(OH)2>Al(OH)3D.得电子能力:P<S<Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用锌片和稀硫酸反应制取氢气时,为加快生成氢气的速率,下列措施不适宜的是
A. 对该反应体系加热 B. 加入硝酸铜固体
C. 改用粗锌 D. 不用锌片,改用锌粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在溶液中能大量共存的是( )
A.K+、H+、Cl﹣、OH﹣
B.K+、H+、HCO3﹣、Cl﹣
C.Fe2+、H+、Br﹣、OH﹣
D.K+、NH4+、SO42﹣、Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分析正确的是
A. 异丁烷的二氯代物有4种
B. 区别蛋白质和淀粉可用浓硝酸做颜色反应
C. 石蜡油分解产物均能使酸性KMnO4溶液褪色
D. 甲苯的硝化反应方程式为: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】洗发剂除了能去除头发上的油污外,一般还有护发、养发、使头发柔顺易梳理的功能,这是因为其中加入了添加剂,下列不属于洗发剂的添加剂的是( )
A. 调理剂 B. 止屑止痒剂
C. 螯合剂 D. 表面活性剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.1 mol·L-1 NaOH溶液450 mL和 0.5 mol·L-1硫酸溶液450 mL。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是________(填字母)。仪器C的名称是________,本实验所需玻璃仪器E规格和名称是___________________。

(2)下列操作中,容量瓶所不具备的功能有__________(填字母)。
A.配制一定体积准确浓度的标准溶液
B.长期贮存溶液
C.用来加热溶解固体溶质
D.量取220 mL体积的液体
(3)在配制NaOH溶液实验中,其他操作均正确,若定容时仰视刻度线,则所配制溶液浓度________(填“大于”“等于”或“小于”,下同)0.1 mol·L-1。若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度______0.1 mol·L-1。
(4)根据计算得知:所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为________ mL(计算结果保留一位小数)。如果实验室有10 mL、25 mL、50 mL量筒,应选用________ mL规格的量筒最好。
(5)如果定容时不小心超过刻度线,应如何操作:______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com