
【题目】已知化学反应:C(s)+![]() O2(g)=CO(g) ΔH1<0 CO(g)+
O2(g)=CO(g) ΔH1<0 CO(g)+![]() O2(g)=CO2(g) ΔH2<0 C(s)+O2(g)=CO2(g) ΔH3<0。相同条件下,下列说法正确的是( )
O2(g)=CO2(g) ΔH2<0 C(s)+O2(g)=CO2(g) ΔH3<0。相同条件下,下列说法正确的是( )
A.56 g CO和32 g O2所具有的总能量小于88 g CO2所具有的总能量
B.碳的燃烧热是|ΔH3|
C.ΔH1<ΔH3
D.28 g CO的总能量比44 g CO2的总能量高
 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
【题目】如图所示的原电池装置,X、Y为两个电极,电解质溶液为稀硫酸,外电路中的电子流向如图所示,对此装置的下列叙述正确的是
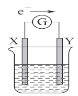
A.外电路中的电流方向为:X→外电路→Y
B.若两个电极分别为Zn和碳棒,则X为碳棒,Y为Zn
C.若两个电极都是金属,则它们的活动性为X>Y
D.X极上发生的是还原反应,Y极上发生的是氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固态或气态碘分别与氢气反应的热化学方程式如下:
①H2(g)+I2(?)2HI(g)△H=-9.48kJmol-1
②H2(g)+I2(?)2HI(g)△H=+26.48kJmol-1
下列判断不正确的是( )
A.![]() 中的I2为气态,
中的I2为气态,![]() 中的I2为固态
中的I2为固态
B.![]() 的反应物总能量比
的反应物总能量比![]() 的反应总能量低
的反应总能量低
C.1mol固态碘升华时将吸热35.96kJ
D.反应![]() 的产物比反应
的产物比反应![]() 的产物热稳定性更好
的产物热稳定性更好
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容容器中,当下列哪些物理量不再发生变化时,表明反应A(g)+2B(g)![]() C(g)+D(g)己达到平衡状态的是( )
C(g)+D(g)己达到平衡状态的是( )
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度
④混合气体的总物质的量 ⑤混合气体的平均相对分子质量 ⑥v(C)与v(D)的比值
⑦混合气体的总质量 ⑧混合气体的总体积 ⑨C、D的分子数之比为1 : 1
A. ①③④⑤ B. ①③④⑤⑧⑨ C. ①②③④⑤⑦ D. ①②③④⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,Fe2O3和H2反应可转化为Fe3O4,方程式为3Fe2O3+H2![]() 2Fe3O4+H2O。下列说法正确的是( )
2Fe3O4+H2O。下列说法正确的是( )
A.Fe2O3俗名磁性氧化铁
B.该反应条件下H2的还原性强于Fe3O4的还原性
C.每消耗160 g Fe2O3,反应中转移2×6.02×1023个电子
D.Fe3O4可由Fe与H2O在常温下反应制得
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①H2(g)+ ![]() O2(g)=H2O(g);ΔH1= akJ·mol-1
O2(g)=H2O(g);ΔH1= akJ·mol-1
②2H2(g)+O2(g) = 2H2O(g);ΔH2= b kJ·mol-1 ③ H2(g)+ ![]() O2(g)=H2O(l);ΔH3= c kJ·mol-1
O2(g)=H2O(l);ΔH3= c kJ·mol-1
④2H2(g)+O2(g) = 2H2O(l);ΔH4= d kJ·mol-1,下列关系式中正确的是( )
A.2a=b<0B.b>d>0C.a<c<0D.2c=d>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积固定的密闭容器中存在如下反应:N2(g)+3H2![]() 2NH3(g) △H<0。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出如下关系图,分析正确的是
2NH3(g) △H<0。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出如下关系图,分析正确的是
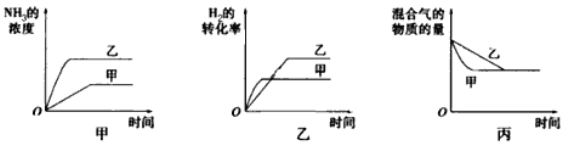
A. 图甲研究的是温度对反应的影响,且甲的温度比乙高
B. 图乙研究的是压强对反应的影响,且甲的压强比乙大
C. 图乙研究的是温度对反应的影响,且甲的温度比乙高
D. 图丙研究的是不同催化剂对反应的影响,且乙使用的催化剂效率比甲高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O,下列说法不正确的是( )
A.该反应中的H2SO4只体现酸性,不体现氧化性
B.1molKClO3参加反应时有5mol电子转移
C.发生氧化反应与还原反应的氯元素的质量比为5:1
D.生成标准状况下22.4LCl2,则有![]() molKClO3被还原
molKClO3被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:
CO(g)+H2S(g)![]() COS(g)+H2(g) K=0.1
COS(g)+H2(g) K=0.1
反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是
A. 升高温度,H2S浓度增加,表明该反应是吸热反应
B. 通入CO后,正反应速率逐渐增大
C. 反应前H2S物质的量为7mol
D. CO的平衡转化率为80%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com