
【题目】乙二醛(OHC-CHO)是一种重要的精细化工产品。长郡中学高三化学兴趣小组利用乙醛液相硝酸氧化法制备乙二醛并测定乙二醛纯度,装置如图所示。
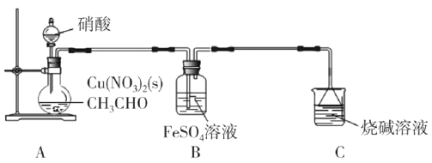
已知:①NO+FeSO4=FeSO4·NO(棕色)。
②几种有机物的部分性质如表所示:

实验步骤:
①取20mL的乙醛装于烧瓶,加入2gCu(NO3)2粉末作催化剂,向烧瓶中缓慢滴加2mol·L-1硝酸至乙醛完全反应为止;
②提纯产品,最终得到10.0mL产品。
请回答下列问题:
(1)盛装硝酸的仪器名称是__。
(2)实验中,观察到装置B中溶液变为棕色,制备乙二醛的化学方程式为__。
(3)向烧瓶中滴加硝酸要“缓慢”,其目的是__;判断烧瓶中制备乙二醛的反应已完成的标志是__。
(4)分离提纯产品,宜选择下列装置__(填字母)。
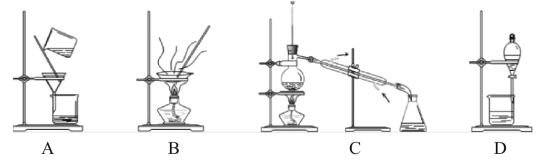
(5)根据上述实验数据,该实验中乙二醛的产率约为__(填字母)。
a.56.5% b.61.8% c.67.9% d.72.6%
(6)实验室可用酸性KMnO4溶液测定乙二醛的纯度,发生反应的离子方程式为:18H++6MnO4-+5C2H2O2→10CO2↑+6Mn2++14H2O。实验步骤如下:取VmL产品,加蒸馏水稀释至250mL,量取25.00mL稀释后的溶液于锥形瓶,滴加5.00mL稀硫酸,用cmol·L-1KMnO4溶液,三次平行实验消耗KMnO4溶液体积如下:
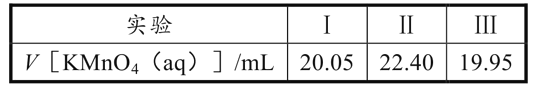
滴定终点的标志是__;该产品纯度为___g·mL-1(用含V和c的代数式表示)。
【答案】分液漏斗 3CH3CHO+4HNO3![]() 3OHC-CHO+4NO
3OHC-CHO+4NO![]() +5H2O 防止乙二醛被氧化 当A中烧瓶不再产生气泡 C b 当滴入最后一滴KMnO4溶液,溶液由无色变为紫红色且半分钟不褪色
+5H2O 防止乙二醛被氧化 当A中烧瓶不再产生气泡 C b 当滴入最后一滴KMnO4溶液,溶液由无色变为紫红色且半分钟不褪色 ![]()
【解析】
该实验的目的是制备乙二醛并测定乙二醛纯度,制备乙二醛的原理是用硝酸氧化乙醛,用FeSO4检验生成的气体NO,烧碱溶液进行尾气处理;在分离提纯产物时,根据表格中的乙二醛与其他几种有机物的物理性质差异,只能用蒸馏法分离;在计算产率时,先计算理论产量,再计算实际产量,产率=![]() ;在用酸性KMnO4溶液测定乙二醛的纯度时,因为酸性KMnO4溶液本身有颜色,故不需要其他的指示剂,在计算时先根据化学方程式计算出乙二醛的量,再计算纯度。
;在用酸性KMnO4溶液测定乙二醛的纯度时,因为酸性KMnO4溶液本身有颜色,故不需要其他的指示剂,在计算时先根据化学方程式计算出乙二醛的量,再计算纯度。
(1)实验装置图中盛装硝酸的仪器是分液漏斗,故答案为:分液漏斗;
(2)观察到装置B中溶液变为棕色,说明硝酸的还原产物为NO,化学方程式为:3CH3CHO+4HNO3![]() 3OHC-CHO+4NO
3OHC-CHO+4NO![]() +5H2O,故答案为:3CH3CHO+4HNO3
+5H2O,故答案为:3CH3CHO+4HNO3![]() 3OHC-CHO+4NO
3OHC-CHO+4NO![]() +5H2O;
+5H2O;
(3)要缓慢加入硝酸的原因是防止乙二醛被氧化,当A中烧瓶不再产生气泡时,说明反应已经完成,故答案为:防止乙二醛被氧化;当A中烧瓶不再产生气泡;
(4)根据表格中的乙二醛与其他几种有机物的物理性质差异,只能用蒸馏法分离,故答案为:C;
(5)n(乙醛)=![]() =0.355mol,由方程式可知n(乙二醛)= n(乙醛)=0.354mol,理论上生成的m(乙二醛)=0.354mol
=0.355mol,由方程式可知n(乙二醛)= n(乙醛)=0.354mol,理论上生成的m(乙二醛)=0.354mol![]() 58g/mol=20.53g,乙二醛的实际产量=10.0mL
58g/mol=20.53g,乙二醛的实际产量=10.0mL![]() 1.27g/mL=12.7g,产率=
1.27g/mL=12.7g,产率=![]() =
=![]()
![]() 61.8%,答案为:b;
61.8%,答案为:b;
(6)用酸性KMnO4溶液测定乙二醛的纯度,即用酸性KMnO4溶液滴定乙二醛溶液,由于酸性KMnO4溶液本身有颜色,故不需要其他的指示剂,当滴入最后一滴KMnO4溶液,溶液由无色变为紫红色且半分钟不褪色,说明到达滴定终点;根据方程式找到关系式:6MnO4-![]() 5C2H2O2,表4的数据中,第II次数据偏差较大,应该舍去,故用去的KMnO4溶液的体积平均值为20.00mL,计算出n(MnO4-)=0.02c mol,则n(C2H2O2)=
5C2H2O2,表4的数据中,第II次数据偏差较大,应该舍去,故用去的KMnO4溶液的体积平均值为20.00mL,计算出n(MnO4-)=0.02c mol,则n(C2H2O2)=![]()
![]() 0.02c mol,原VmL的产品中含有的n(C2H2O2)=
0.02c mol,原VmL的产品中含有的n(C2H2O2)=![]()
![]() 0.02c
0.02c![]() 10 mol=
10 mol=![]() mol,算出产品的纯度为=
mol,算出产品的纯度为=![]() =
=![]() g·mL-1,故答案为:当滴入最后一滴KMnO4溶液,溶液由无色变为紫红色且半分钟不褪色;
g·mL-1,故答案为:当滴入最后一滴KMnO4溶液,溶液由无色变为紫红色且半分钟不褪色;![]() 。
。


 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案科目:高中化学 来源: 题型:
【题目】下列表述正确的是( )
A.“青矾(绿矾)厂气熏人,衣服当之易烂,栽木不盛”。青矾厂气是![]() 和
和![]()
B.杜康用高粱酿酒的原理是通过蒸馏法将高粱中的乙醇分离出来
C.“信州铅山县有苦泉,流以为涧。挹其水熬之,则成胆矾”,其中涉及的操作有结晶
D.推广使用煤液化技术可以减少温室气体二氧化碳的排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列我国科研成果所涉及材料中,主要成分为同主族元素形成的无机非金属材料的是
|
|
|
|
A.4.03米大口径碳化硅反射镜 | B.2022年冬奥会聚氨酯速滑服 | C.能屏蔽电磁波的碳包覆银纳米线 | D.“玉兔二号”钛合金筛网轮 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. ![]() C和
C和![]() C是碳元素的2种核素,它们互为同位素
C是碳元素的2种核素,它们互为同位素
B. 化学研究者开发出被称为第五形态的固体碳,这种新的碳结构称作“纳米泡沫”,它外形类似海绵,比重极小,并具有磁性。纳米泡沫碳与C60互称同素异形体
C.  与
与 互为同分异构体
互为同分异构体
D. 硝基苯可看成是由![]() 和—NO2两种基团组成
和—NO2两种基团组成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于合成材料的说法中,错误的是
A.聚氯乙烯可制成薄膜、软管等,其单体是CH2=CHCl
B.锦纶![]() 的单体是H2N(CH2)6NH2和HOOC(CH2)4COOH
的单体是H2N(CH2)6NH2和HOOC(CH2)4COOH
C.合成酚醛树脂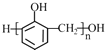 的单体是苯酚和甲醇
的单体是苯酚和甲醇
D.合成顺丁橡胶![]() 的单体是CH2=CH﹣CH=CH2
的单体是CH2=CH﹣CH=CH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】材料是经济和生态文明建设的重要物质基础。
①生产硅酸盐水泥和普通玻璃都需用到的共同原料是___。
②橡胶是制造轮胎的重要原料,橡胶属于___(填字母)。
A.金属材料 B.无机非金属材料 C.有机高分子材料
③钢铁制品在潮湿的空气中能发生__腐蚀.发生该腐蚀时的负极反应式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备硝基苯的实验装置如图所示(夹持装置已略去)。下列说法不正确的是( )

A.水浴加热的优点为使反应物受热均匀、容易控制温度
B.浓硫酸、浓硝酸和苯混合时,应向浓硝酸中加入浓硫酸,待冷却至室温后,再将所得混合物加入苯中
C.仪器a的作用是冷凝回流,提高原料的利用率
D.反应完全后,可用仪器a、b蒸馏得到产品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸俗称草酸,为二元酸(结构简式为HOOC-COOH,可简写为H2C2O4)。25℃时,草酸的电离平衡常数K1=5.0×10-2,K2=5.4×10-5;碳酸的电离平衡常数K1=4.5×10-7,K2=4.7×10-11。草酸钙的Ksp=4.0×10-8,碳酸钙的Ksp=2.5×10-9。回答下列问题:
(1)写出水溶液中草酸的电离方程式:________________________________。
(2)25℃,物质的量浓度都为0.1 mol/L的Na2C2O4溶液的pH比Na2CO3溶液pH______________________(填“大”“小”或“相等”)。
(3)常温下将0.2 mol/L的KOH溶液10 mL与0.2 mol/L的草酸溶液10 mL混合,若混合溶液显酸性,则该溶液中所有离子浓度由大到小的顺序:____________________。
(4)25℃时向20 mL碳酸钙的饱和溶液中逐滴加入1.0×10-3mol/L的草酸钾溶液20 mL,能否产生沉淀?________________(填“能”或“否”)。
(5)除去锅炉水垢中的CaSO4可先用碳酸钠溶液处理,而后用盐酸溶解,其反应的离子方程式:______________________________;________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com