
| 甲 | 乙 | 丙 | 丁 | 戊 | |
| 0.1mol/L 的 Ba(OH)2溶液的体积/mL | 10 | 10 | 10 | 10 | 10 |
| 0.1mol/L 的E溶液的体积/mL | 5 | 10 | 15 | 20 | 25 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、称取氢氧化钠20.0 g |
| B、定容时俯视观察刻度线 |
| C、移液时,对用于溶解氢氧化钠的烧杯没有进行冲洗 |
| D、移液用玻璃棒引流时,玻璃棒下端靠在容量瓶刻度线上方 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 L 0.3 mol?L-1 CH3COOH和3 L 0.1 mol?L-1 CH3COOH中的H+数目 |
| B、1 L 0.3 mol?L-1 CH3COOH和3 L 0.1 mol?L-1 CH3COOH的电离常数 |
| C、在4NH3+6NO═5N2+6H2O反应中,被氧化和被还原的N原子数 |
| D、纯水在25℃和80℃时的pH |
查看答案和解析>>
科目:高中化学 来源: 题型:
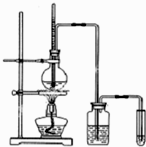 下面是实验室制乙烯并检验其性质的装置图,请回答:
下面是实验室制乙烯并检验其性质的装置图,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯分子中碳、氢原子个数比为1:2,证明乙烯分子里含有一个碳碳双键 |
B、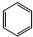 表示苯分子的结构,因此能解释邻二甲苯有 表示苯分子的结构,因此能解释邻二甲苯有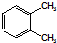 和 和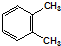 两种结构 两种结构 |
C、因为甲烷是一种正四面体结构,所以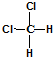 和 和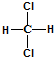 属于同一种物质 属于同一种物质 |
| D、苯的分子式是C6H6,分子式中碳原子远没有饱和,因此苯能使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
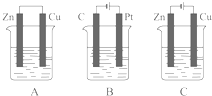 如图所示,A、B、C三个装置的烧杯中分别盛有足量的CuCl2溶液.
如图所示,A、B、C三个装置的烧杯中分别盛有足量的CuCl2溶液.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、PCl3和SO2都是极性分子 |
| B、H2O是一种非常稳定的化合物,这是由于氢键所致 |
| C、BF3、NCl3分子中所有原子的最外层电子都满足8电子稳定结构 |
| D、凡是中心原子采取sp3杂化轨道形成的分子其几何构型都是正四面体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com