
| 时间/浓度 | C(NH3)(mol/L) | C(O2)(mol/L) | C(NO)(mol/L) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | A | 0.2 |
| 第4min | 0.3 | 0.975 | 0.5 |
| 第6min | 0.3 | 0.975 | 0.5 |
| 第8min | 0.3 | 1.6 | 0.5 |
| 1025kJ |
| 5 |
| 0.3mol/L |
| 2min |
| 5 |
| 4 |
| 5 |
| 4 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
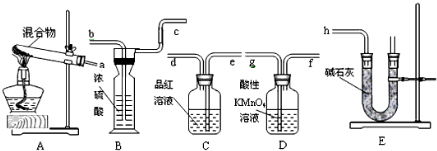
| A、b、a、e、d、c |
| B、e、d、a、b、c |
| C、a、b、d、c、e |
| D、c、d、e、a、b |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不含NO3-,可能含Fe3+ |
| B、含有NO3-、I-、Cl- |
| C、含I-,但不能确定是否含Cl- |
| D、不含有NO3-和Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
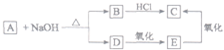 已知有机物A的分子式为C4H8O2,它能在NaOH溶液中发生水解.根据下图所示的各物质相互转变关系,分别写出下列有机物的结构简式.
已知有机物A的分子式为C4H8O2,它能在NaOH溶液中发生水解.根据下图所示的各物质相互转变关系,分别写出下列有机物的结构简式.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com