
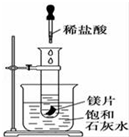
 ��ͼ��ʾ�����Թܷ���ʢ��25�汥�ͳ���ʯ��ˮ���ձ��У��Թ��п�ʼ���뼸С��þƬ�����õιܵ���10mL�������Թ��У��Իش��������⣺
��ͼ��ʾ�����Թܷ���ʢ��25�汥�ͳ���ʯ��ˮ���ձ��У��Թ��п�ʼ���뼸С��þƬ�����õιܵ���10mL�������Թ��У��Իش��������⣺���� ��ͼ��ʾ��ʵ���У����Թ��ڵ���ϡ���ᣬ������þ���ҷ�Ӧ�ų�������ͬʱ��Ӧ�ų�������ʹ����ʯ��ˮ��Һ�¶����ߣ��¶��������������ܽ�ȼ�С��������Һ���������������ƶ�ʹ��Һ����ȥ����ǣ�
��� �⣺��1��þ��������ҷ�Ӧ���ɹ۲쵽�����������壬��Ӧ�ų�����ʹ������Һ�¶����ߣ������������ʣ��۲쵽��Һ����ǣ�
�ʴ�Ϊ��þƬ���д������ݣ�þƬ���ܽ⣬�ձ�����Һ����ǣ�
��2��þ�����ᷢ���û���Ӧ�������Ȼ�þ����������Ӧ�Ļ�ѧ����ʽΪMg+2HCl�TMgCl2+H2������Ӧ����1molMgCl2��ת��2mol���ӣ�ת��0.04mol����ʱ�����ɵ�MgCl2���ʵ���Ϊ0.02mol��MgCl2���ʵ���Ũ��Ϊ$\frac{0.02mol}{0.01L}$=2mol/L��
�ʴ�Ϊ��2mol/L��
��3������Ӧ����������������������ʱ����Ӧ�Ƿ��ȷ�Ӧ����MgCl2��Һ��H2��������С��þƬ����������������ʴ�Ϊ�����ڣ����ȷ�Ӧ��
���� ���⿼���˻�ѧ��Ӧ����������仯������Ϊ��Ƶ���㣬���ؿ���ѧ���ķ���������ע�����ͨ����ѧ�仯���ȶ�ʹ������Һ�¶����ߣ��������Ƶı�����Һ�У����������ܽ�����¶����߶���С�ģ��ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cu+2Ag+�TCu2++2Ag Cu+2AgCl�TCuCl2+2 Ag | |
| B�� | CO32-+2 H+�TCO2��+H2O BaCO3+2HCl�TBaCl2+CO2��+H2O | |
| C�� | Al3++3OH-�TAl��OH��3�� Al�� NO3��3+3NH3•H2O�TAl��OH��3��+3NH4NO3 | |
| D�� | H++OH-�TH2O Ba��OH��2+2HNO3�TBa��NO3��2+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 Ag+��aq��+Cl-��aq�����������백ˮ��ϣ���������Һ�������ӵ�Ũ�ȣ�ʹ����ƽ�������ƶ�����ʹAgCl�ܽ⣮
Ag+��aq��+Cl-��aq�����������백ˮ��ϣ���������Һ�������ӵ�Ũ�ȣ�ʹ����ƽ�������ƶ�����ʹAgCl�ܽ⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
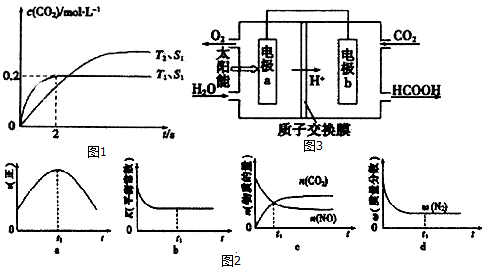
| A�� | ͨ�뺤��ʹ�ܱ�������ѹǿ����ƽ��������Ӧ�����ƶ� | |
| B�� | ����X�����ʵ��������������ܶȼ�С | |
| C�� | X������Ӧ������Y���淴Ӧ���ʵ�$\frac{m}{n}$�� | |
| D�� | �����¶ȣ���������ƽ����Է����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��HCl��Һ��������ˮϴ��AgCl�����Լ��ٳ�����ʧ | |
| B�� | ��BaSO4������뵽����Na2CO3��Һ�У���ַ�Ӧ����ˡ�ϴ�ӣ��������еμ�ϡ���ᣬ�������������֤����������Ksp��BaSO4����Ksp��BaCO3�� | |
| C�� | ��ˮ�м���NaHCO3��NaHSO4�����ˮ�ĵ���̶Ⱦ����� | |
| D�� | ��������������ˮ�ⷴӦ������ϡ�������߷�Ӧ���ʺ�����������ת���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Al65Cu23Fe12��Ӳ�ȱȽ���Al��Cu��Fe��Ӳ�ȴ� | |
| B�� | Al65Cu23Fe12�����ֽ����Ļ��ϼ۾��������� | |
| C�� | Al65Cu23Fe12�����������ڽ����ں�ˮ�еIJ��� | |
| D�� | 1mol Al65Cu23Fe12���ڹ���������ʱ��ʧȥ265 mol���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
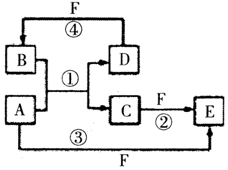 A��B��C��D��E��F�������ʵ�ת����ϵ��ͼ��ʾ����Ӧ�����Ͳ��ֲ���δ���������ش��������⣺
A��B��C��D��E��F�������ʵ�ת����ϵ��ͼ��ʾ����Ӧ�����Ͳ��ֲ���δ���������ش��������⣺ ����Ӧ�ܵĻ�ѧ����ʽΪC+4HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2+4NO2��+2H2O��
����Ӧ�ܵĻ�ѧ����ʽΪC+4HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2+4NO2��+2H2O���鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com