
【题目】下列有关物质的分类正确的是( )
A.混合物:空气、矿泉水、水银
B.酸性氧化物:、CO2、SO2、CO
C.盐:醋酸钠、氯化铵、纯碱
D.弱电解质:CH3COOH,H2O,NH3
科目:高中化学 来源: 题型:
【题目】铁触媒是重要的催化剂,CO易与铁触媒作用导致其失去催化活性:Fe+5CO=Fe(CO)5;除去CO的化学反应方程式为:[Cu(NH3)2]OOCCH3+CO+NH3=[Cu(NH3)3(CO)]OOCCH3。
请回答下列问题:
(1)基态Fe原子的价电子排布图为 。
(2)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则Fe(CO)5的晶体类型是 ,与CO互为等电子体的分子的分子式为 。
(3)配合物[Cu(NH3)2]OOCCH3中碳原子的杂化类型是 ,配体中提供孤对电子的原子是 。
(4)用[Cu(NH3)2]OOCCH3除去CO的反应中,肯定有 形成。
a.离子键 b.配位键 c.非极性键 d.σ键
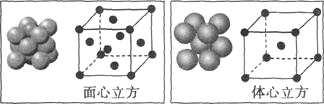
(5)单质铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示,面心立方晶胞和体心立方晶胞中实际含有的铁原子个数之比为 ,面心立方堆积与体心立方堆积的两种铁晶体的晶胞单位分别为a pm和b pm,则![]() = 。
= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】200 ℃时,11.6 g CO2和水蒸气的混合气体与足量的Na2O2充分反应后,固体质量增加了3.6 g。则原混合气体中CO2和H2O的物质的量之比是( )
A.1:4 B.3:11 C.1:11 D.21:22
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前工业上可用CO2来生产燃料甲醇,有关反应为:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=—49.0 kJ·mol-1。现向体积为1L的密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
CH3OH(g)+H2O(g) ΔH=—49.0 kJ·mol-1。现向体积为1L的密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
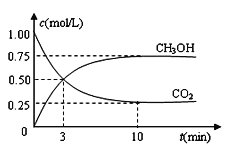
(1)从反应开始到平衡,氢气的平衡浓度为C(H2)=_____________;
(2)若改变条件使平衡向正反应方向移动,则平衡常数______________(填序号)
a.可能不变 b.可能减小 c.可能增大 d.不变、减小、增大皆有可能
(3)能够说明该反应已达到平衡的是__________(填字母序号,下同)。
A.恒温、恒容时,容器内的压强不再变化
B.恒温、恒容时,容器内混合气体的密度不再变化
C.一定条件下,CO2、H2和CH3OH的浓度保持不变
D.一定条件下,单位时间内消耗3molH2的同时生成1mol CH3OH
(4)在其他条件不变的情况下,将体系体积压缩到原来的二分之一,下列有关该体系的说法正确的是________。
a.氢气的浓度减小 b.正反应速率增大,逆反应速率也增大
c.甲醇的物质的量增加 d.重新平衡时n(H2)/n(CH3OH)增大
(5)求此温度(T)下该反应的平衡常数K= ________。若开始时向该1L密闭容器中充入1mol CO2,2mol H2,1.5mol CH3OH和1mol H2O(g),则反应向________(填“正”或“逆”)反应方向进行。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.化学反应中,物质变化的同时不一定发生能量变化
B.反应焓变(△H)的大小与方程式中各物质的化学计量系数无关
C.反应产物的总焓大于反应物的总焓时,反应吸热,△H>0
D.吸热反应中,形成化学键释放的能量大于断裂化学键吸收的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在原子的第n层电子层中,当它为最外电子层时,最多容纳的电子数与(n-1)层相同,当它为次外层时,最多容纳的电子数比(n+1)层多容纳10个电子,则此电子层为( )
A. K层 B. L层 C. M层 D. N层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对外加电流的金属保护中,被保护的金属( )
A. 与电源的正极相连 B. 表面上发生氧化反应
C. 与电源的负极相连 D. 与另一种活泼性较差的金属相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于分液漏斗的使用,下列说法正确的是( )
A. 可在分液漏斗内用四氯化碳萃取碘酒中的碘单质
B. 分液漏斗在使用前只需检查旋塞芯处是否漏水即可
C. 在分液漏斗中加入萃取剂后应上下颠倒摇匀使萃取剂与溶质充分接触
D. 放出下层液体时,应打开上方的玻璃塞,并使下端管口紧贴烧杯内壁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与科学、技术、社会、环境关系密切,下列说法正确的是
A. 明矾既能沉降水中的悬浮物,又能杀菌消毒
B. NH4Cl溶液可用作焊接时的除锈剂
C. 轮船船底四周镶嵌铜块以保护船体
D. 电解熔融氯化铝可以得到铝
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com