
| A、HClO、浓硫酸、HNO3均具有氧化性,都是氧化性酸 |
| B、H2O、HCOOH、Cu2(OH)2CO3均含有氧元素,都是氧化物 |
| C、HF、CH3COOH、CH3CH2OH都易溶于水,都是电解质 |
| D、HCOOH、H2CO3、H2SO4分子中均含有两个氢原子,都是二元酸 |


科目:高中化学 来源: 题型:

| A、常压下五种元素的单质中Z单质的沸点最高 |
| B、Y、Z的阴离子电子层结构都与R原子的相同 |
| C、W的氢化物还原性小于Y的氢化物 |
| D、Y元素的非金属性比W元素的非金属性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
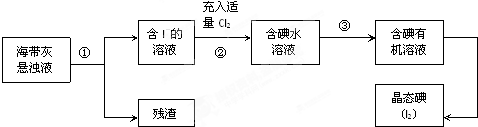
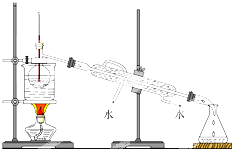
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 I2(g)+H2(g)?2HI(g) |
B、 CH3COOH?H++CH3COO-(忽略溶液体积变化) |
C、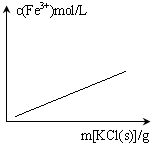 FeCl3+3KSCN?Fe(SCN)3+3KCl(忽略液体体积变化) |
D、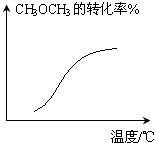 CH3OCH3(g)+3H2O(g)?6H2(g)+2CO(g)-Q(恒压) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
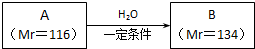
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | W | X | Y | Z |
| A | CH3COOC2H5 | CH3COOH | Na2CO3溶液 | 分液 |
| B | CO2 | SO2 | 饱和Na2CO3溶液 | 洗气 |
| C | NaCl固体 | I2 | CCl4 | 分液 |
| D | Na2CO3溶液 | NaHCO3溶液 | Ca(OH)2溶液 | 过滤 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、从1 L 1 mol/L的NaCl溶液中取出10 mL,其浓度仍是1 mol/L |
| B、制成0.5 L 10 mol/L的盐酸,需要氯化氢气体112 L(标准状况) |
| C、0.5 L 2 mol/L BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023 |
| D、10 g 98%的硫酸(密度为1.84 g/cm3)与10 mL 18.4 mol/L硫酸的浓度是不同的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com