
| 选项 | W | X | Y | Z |
| A | CH3COOC2H5 | CH3COOH | Na2CO3溶液 | 分液 |
| B | CO2 | SO2 | 饱和Na2CO3溶液 | 洗气 |
| C | NaCl固体 | I2 | CCl4 | 分液 |
| D | Na2CO3溶液 | NaHCO3溶液 | Ca(OH)2溶液 | 过滤 |
| A、A | B、B | C、C | D、D |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HClO、浓硫酸、HNO3均具有氧化性,都是氧化性酸 |
| B、H2O、HCOOH、Cu2(OH)2CO3均含有氧元素,都是氧化物 |
| C、HF、CH3COOH、CH3CH2OH都易溶于水,都是电解质 |
| D、HCOOH、H2CO3、H2SO4分子中均含有两个氢原子,都是二元酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
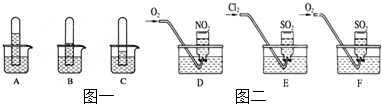
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知A为中学化学中的一种深蓝色盐,B、C为日常生活中常见的金属单质,D、G为无色无味气体,各物质之间的转化关系如下图(电解采用惰性电极,部分反应产物已略去).请回答下列问题:
已知A为中学化学中的一种深蓝色盐,B、C为日常生活中常见的金属单质,D、G为无色无味气体,各物质之间的转化关系如下图(电解采用惰性电极,部分反应产物已略去).请回答下列问题:| Ⅰ | Ⅱ | Ⅲ | Ⅳ | |
| H溶液的体积(mL) | 100 | 100 | 100 | 100 |
| 加入B、C合金的质量(g) | 3 | 6.6 | 9 | 12 |
| 剩余固体的质量(g) | 0 | 0.64 | 3.2 | 6.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1L0.1mol?L-1的氨水含有0.1NA个NH4+ |
| B、84gNaHCO3晶体中含有 NA个 HCO3- |
| C、1molFe在氧气中充分燃烧失去的电子数为3NA |
| D、64g铜片与足量稀HNO3反应生成NA个NO分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学反应中的能量变化,表现形式除热量外还可以是光能和电能等 |
| B、化学反应中的能量变化不一定服从能量守恒定律 |
| C、在一个确定的化学反应关系中,反应物的总能量与生成物的总能量可能相同 |
| D、在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com