解答:
解:(1)前3 min,v(C)=
=
=0.4 mol?L
-1?min
-1,故答案为:0.4 mol?L
-1?min
-1;
(2)根据图中数据知道,A、B、C、D四种物质的物质的量的变化量之比是0.4:0.2:0.6:0.2=2:1:3:1,等于方程式的系数之比,方程式表示为:2A(g)+B(g)?3C(g)+D(s),
A.反应前后气体的体积不变,所以混合气体的压强不变化,不一定平衡,故A错误;
B.混合气体的密度等于质量和体积的比值,质量变化,体积不变,所以当密度不变了,达到了平衡,故B正确;
C.混合气体的平均相对分子质量是质量和物质的量的比值,质量变化,物质的量不变,所以当混合气体的平均相对分子质量不变了,达到了平衡,故C正确;
D.B的物质的量不变化,是平衡状态的特征,达到了平衡,故D正确;
E.混合气体的总的物质的量始终是不变化的,故E错误.
故答案为:BCD.
(3)当达到平衡时,平衡常数K=
=
=1.69,故答案为:1.69;
(4)反应2A(g)+B(g)?3C(g)+D(s),达到平衡后,
A.保持体积不变,通入2mol A和1mol B,会使得A的转化率减小,故A错误;
B.D是固体,移走一部分D,平衡不移动,A的转化率不变,故B正确;
C.把容器的体积缩小一倍,即加压,平衡不移动,A的转化率不变,故C正确;
D.升高温度,平衡逆向移动,A的转化率减小,故D错误.
故答案为:BC.
(5)T℃时,容积为1 L的密闭容器中,起始充入0.2mol A、0.4 mol B、0.3 mol C、0.5mol D,此时Qc=
=
=1.69=K,仍然是平衡状态,故正逆反应速率相等,故答案为:=;浓度商与平衡常数相等或Q
c=K.

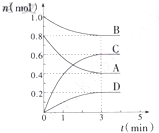 在T℃时,在容积为0.5L的密闭容器中发生如下反应:mA(g)+nB(g)?pC(g)+qD(s),△H<0(m、n、p、q为最简整数比).A、B、C、D物质的量的变化如图所示:
在T℃时,在容积为0.5L的密闭容器中发生如下反应:mA(g)+nB(g)?pC(g)+qD(s),△H<0(m、n、p、q为最简整数比).A、B、C、D物质的量的变化如图所示: