
�������ڶ��ڿθ��½̲ģ�B��������һ�ڿθĽ̲ġ�
��A���ҹ���ѧ�Һ�°�����ͼ���ĸ����Ĵ����������գ��������̿ɼ�Ҫ��ʾ���£�
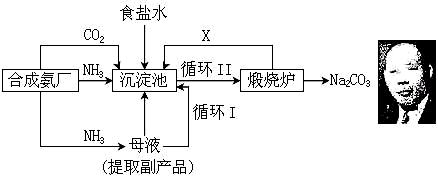
(1) ������������ķ����� ������Ʒ��һ����;Ϊ ��
(2) �������з����Ļ�ѧ��Ӧ����ʽ�� ��
(3) д������������X���ʵķ���ʽ ��
(4) ʹԭ���Ȼ��Ƶ������ʴ�70%��ߵ�90%���ϣ���Ҫ������� �������������еı�ţ���ѭ�����ӳ�������ȡ�������IJ����� ��
(5)Ϊ�����Ʒ̼�������Ƿ����Ȼ��ƣ���ȡ������������ˮ���ٵμ� ��
(6) ��ĸҺ��ͨ����������ϸСʳ�ο�������ȴ��������Ʒ��ͨ������������ ��
(a) ����NH4+��Ũ�ȣ�ʹNH4Cl���������
(b) ʹNaHCO3���������
(c) ʹNaHCO3ת��ΪNa2CO3�����������NH4Cl����
��B��ij��ѧ����С������ͼװ����ȡ�屽��
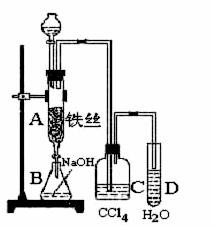
�����Һ©���м��뱽��Һ�� ���ٽ����Һ�������뷴Ӧ��A��A�¶˻������С�
(1)д��A�з�Ӧ�Ļ�ѧ����ʽ
(2)�۲쵽A�е������� ��
(3)ʵ�����ʱ����A�¶˵Ļ������÷�ӦҺ����B�У������Ŀ���� ��д���йصĻ�ѧ����ʽ ��
(4)C��ʢ��CCl4�������� ��
(5)��֤������Һ�巢������ȡ����Ӧ�������Ǽӳɷ�Ӧ�������Թ�D�м���AgNO3��Һ������������ɫ����������֤������һ����֤�ķ��������Թ�D�м��� �������� ��
���𰸡�
��A��
(1)�����Ƽ���°��Ƽ ���ʻ���Һ��ҩ�ȣ����������𰸾��ɣ�
(2)NH3 + CO2 + H2O + NaCl �� NH4Cl + NaHCO3��
��NH3+CO2+H2O��NH4HCO3 NH4HCO3+NaCl��NaHCO3��+NH4Cl
(3)CO2
(4)I ����
(5)ϡ�������������Һ
(6)a��c
��������������Ҫ�����°��Ƽ������ԭ�����������ա�Cl���ļ���ȣ����������Ƽ������ԭ������֪��ʳ��ˮ��ͨ�백����Ϊ�˵õ�������Һ�������ո����CO2����CO2����ʱ������Ӧ��NH3+H2O+CO2==NH4HCO3��NH4HCO3+NaCl==NaHCO3��+NH4Cl����NaHCO3������¯������ʱ�ֽ⣺2NaHCO3 Na2CO3+CO2��+H2O����XΪCO2��Ҫ���NaCl�������ʱ��뽫���˳�NaHCO3��ĸҺѭ�����á�Ҫ����Na2CO3���Ƿ����NaCl��ֻ��������Һ�м��������ữ��AgNO3��Һ���Ƿ��а�ɫ�������ɡ�����ĸҺ��ͨ��NH3ʱ������ӦHCO4-+NH3==NH4++CO32-��c��NH4+������NaHCO3ת��ΪNa2CO3��
Na2CO3+CO2��+H2O����XΪCO2��Ҫ���NaCl�������ʱ��뽫���˳�NaHCO3��ĸҺѭ�����á�Ҫ����Na2CO3���Ƿ����NaCl��ֻ��������Һ�м��������ữ��AgNO3��Һ���Ƿ��а�ɫ�������ɡ�����ĸҺ��ͨ��NH3ʱ������ӦHCO4-+NH3==NH4++CO32-��c��NH4+������NaHCO3ת��ΪNa2CO3��
��B��
(1)C6H6 + Br2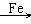 C6H5Br + HBr��
C6H5Br + HBr��
(2)��ӦҺ�� �к���ɫ�������A����
(3)��ȥ�����屽�е���
Br2 + 2NaOH �� NaBr + NaBrO + H2O
�� 3Br2 + 6NaOH �� 5NaBr + NaBrO3 + 3H2O
(4)��ȥ�廯�������е�������
(5)ʯ����Һ����Һ���ɫ �����������𰸾��ɣ�
��������������Ҫ�����屽�Ʊ������е�ϸ�����⡣
���ڱ���Һ��ķе�ϵͣ��ҷ�Ӧ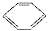 +Br2
+Br2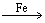
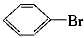 +HBr��Ϊ���ȷ�Ӧ����A�й۲쵽������Ϊ����ӦҺ�У��к���ɫ�������A������HBr�л��е�Br2�ھ���CCl4 ʱ�����գ����Ʊ����屽�г�����Br2��һ�����NaOH��Һ�У�������ӦBr2+2NaOH====NaBr+NaBrO+H2O����ȥ�����÷�ӦΪȡ����Ӧ�����HBr���ɣ���Ϊ�ӳɷ�Ӧ��û��HBr���ɣ���ֻ����D���Ǻ��д���H+��Br�����ɡ�
+HBr��Ϊ���ȷ�Ӧ����A�й۲쵽������Ϊ����ӦҺ�У��к���ɫ�������A������HBr�л��е�Br2�ھ���CCl4 ʱ�����գ����Ʊ����屽�г�����Br2��һ�����NaOH��Һ�У�������ӦBr2+2NaOH====NaBr+NaBrO+H2O����ȥ�����÷�ӦΪȡ����Ӧ�����HBr���ɣ���Ϊ�ӳɷ�Ӧ��û��HBr���ɣ���ֻ����D���Ǻ��д���H+��Br�����ɡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��T��ʱ����ag NH3��ȫ����ˮ���õ�V mL��Һ���������Һ���ܶ�Ϊ�� g/cm3�����ʵ���������ΪW�����к�NH4+�����ʵ���Ϊbmol��������������ȷ���� ( )
A�����ʵ���������Ϊ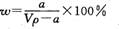
B��������Һ���ټ���V mLˮ��������Һ���ʵ�������������O��5w
C����Һ��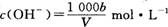
D�����ʵ����ʵ���Ũ��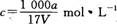
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1����֪����Fe(s)��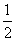 O2(g)��FeO(s) ��H1����272.0 kJ��mol��1��
O2(g)��FeO(s) ��H1����272.0 kJ��mol��1��
��2Al(s)��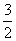 O2(g)===Al2O3(s) ��H2����1675.7 kJ��mol��1��
O2(g)===Al2O3(s) ��H2����1675.7 kJ��mol��1��
Al��FeO�������ȷ�Ӧ���Ȼ�ѧ����ʽ�� ��
ijͬѧ��Ϊ�����ȷ�Ӧ�����ڹ�ҵ����������ж��� ����ܡ����ܡ�����
��������� ��
��2����Ӧ�����������Ϊ��̬��ij���淴Ӧ�ڲ�ͬ�����µķ�Ӧ���̷ֱ�ΪA��B��
��ͼ��ʾ��
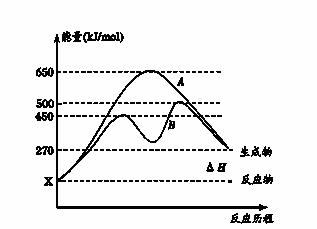
�پ�ͼ�жϸ÷�Ӧ��___��������š����ȷ�Ӧ������Ӧ�ﵽƽ�������
�������䣬�����¶ȣ��淴Ӧ���ʽ�____�����������С�����䡱����
������B���̱����˷�Ӧ���õ�����Ϊ________������ĸ����
A�������¶ȡ��� B������Ӧ���Ũ��
C�������¶� D��ʹ�ô���
��3����֪�Ȼ�ѧ����ʽ��H2(g)��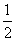 O2(g)��H2O(g)����H����241.8 kJ��mol��1
O2(g)��H2O(g)����H����241.8 kJ��mol��1
�÷�Ӧ�Ļ��Ϊ167.2 kJ��mol��1�������淴Ӧ�Ļ��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��40 g�ܶ�Ϊ�� g•cm��3���������Һ�ﺬ1 g Ca2������NO3�������ʵ���Ũ���ǣ� ����
A����/400 mol•L��1 B��20��mol•L��1
C��2.5�� mol•L��1 D��1.25�� mol•L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��CO2��H2��ɵĻ������ͬ�¡�ͬѹ���뵪�����ܶ���ͬ����û��������CO2��H2����������Ϊ�� ����
A��29��8 B��22��1 C��13��8 D��8��13
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�о���ѧϰС�����SO2���Ʊ�������̽��ʵ�顣
�� ���ݷ�ӦNa2SO3(��) + H2SO4��Ũ�� == Na2SO4 + SO2��+H2O���Ʊ�SO2���塣
�����м�ͼ���ڴ���ķ����л����Ʊ����ռ�SO2��ʵ��װ�ã����Լ���ʾ��ͼ��
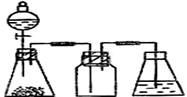
�� ʵ������У�ʹ�÷�Һ©���μ�Ũ����IJ�����__________________________��
�� ��SO2����ֱ�ͨ��������Һ�У�
�� Ʒ����Һ��������__________________________________________________��
�� ��ˮ��Һ��������_________________________________________________��
�� ������Һ��������________________________________________________��
�� ��һС����ʵ���з��֣�SO2�����������������º���ʵ������ܲ����ԣ����ֲ��������������⡣�����Ʋ���ܵ�ԭ��˵����Ӧ����֤���������Բ�������
�� ԭ��_______________________����֤����________________________________��
�� ԭ��_______________________����֤����________________________________��
�� ԭ��_______________________����֤����________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
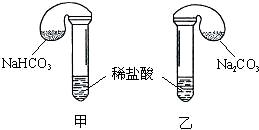
��ѧ����ϣ�����ѧ���ֱ���ͼʾ�ס�����װ�ã�̽����NaHCO3��Na2CO3��ϡ����ķ�Ӧ���������е��Լ�����������ͬ�����£������������еĹ����ĩͬʱ�����Թ��У�װ�õ��������Ѽ�飩��
��ش�
��1�����鷴Ӧ��ʼʱ��________װ���е���������ȱ��װ���з�Ӧ�����ӷ���ʽ��___________________________��
��2�����Թ��в�������������ʱ������ʵ����ֲ�ͬ������д�±��Ŀո�
| �Լ����� | ʵ������ ����������仯�� | ����ԭ�� | |
| �� �� �� | 0.42 g NaHCO3 0.53 g Na2CO3 3 mL 4 mol/L���� | ������������������������� | �ס������������ n��NaHCO3��=n��Na2CO3�� V����CO2��=V����CO2�� |
| �� �� �� | 0.3 g NaHCO3 0.3 g Na2CO3 3 mL 4 mol/L���� | ����������������������� | |
| �� �� �� | 0.6 g NaHCO3 0.6 g Na2CO3 3 mL 2 mol/L���� | ����������������������� | |
| Ƭ�̺�������������С���������������������� | �������ӷ���ʽ��ʾ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
298Kʱ����FeCl��������Һ�м�����п����Fe3+ ��������ԭ��Fe2+���ݴ�ijѧϰС�������ͼ��ʾ��ԭ���װ�á������й�˵����ȷ����
��A��������ӦΪZn�C2e��=Zn2+ ��
B�����ձ�����Һ�ĺ�ɫ��dz
��C��Pt�缫�������ݳ��� ��
 D���õ���ܷ�ӦΪ3Zn + 2Fe3+ = 2Fe + 3Zn2+
D���õ���ܷ�ӦΪ3Zn + 2Fe3+ = 2Fe + 3Zn2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������Ҷ�ͪ������ҽҩ�м��弰�����߹̻��������ɶ���������ͪ�����Ƶã���Ӧ�Ļ�ѧ����ʽ��װ��ͼ(����װ��ʡ��)���£�
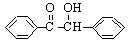 ��2FeCl3
��2FeCl3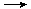
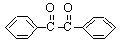 ��2FeCl2��2HCl
��2FeCl2��2HCl
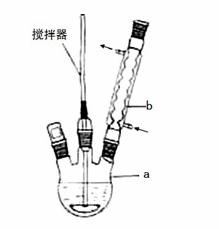
�ڷ�Ӧװ���У�����ԭ�ϼ��ܼ��������¼��Ȼ�������Ӧ�����������У���ȴ���ж������Ҷ�ͪ�ֲ�Ʒ��������70���Ҵ�ˮ��Һ�ؽᾧ�ᴿ���ؽᾧ���̣�
�����ܽ������̿��ɫ�����ȹ��ˡ���ȴ�ᾧ�����ˡ�ϴ�ӡ�����
��ش��������⣺
��1��д��װ��ͼ�в������������ƣ�a___________��b____________��
��2�����ȹ��˺���Һ��ȴ�ᾧ��һ������£�������Щ���������ڵõ��ϴ�ľ��壺____��
A��������ȴ��Һ B����ҺŨ�Ƚϸ�
C�������ܽ�Ƚ�С D�����������ܼ�
�����Һ�з������������ɲ���__________�ȷ����ٽ�����������
��3���������õ���ֽӦ��_______������ڡ���С�ڡ�������©���ھ�����ȫ��С��ס���ձ��еĶ������Ҷ�ͪ����ת�벼��©��ʱ��������������ճ���������壬��ѡ��Һ�彫�����ϵľ����ϴ������ת�벼��©��������Һ������ʵ���________��
A����ˮ�Ҵ� B������NaCl��Һ C��70���Ҵ�ˮ��Һ D����Һ
��4�������ؽᾧ�����е���һ��������ȥ�˲��������ʣ�___________��
��5��ijͬѧ���ñ���ɫ��(ԭ���Ͳ�����ֽ������ͬ)���ٷ�Ӧ���̣��ֱ��ڷ�Ӧ��ʼ������15min��30min��45min��60minʱ����ëϸ��ȡ��������������ɫ��չ����İߵ���ͼ��ʾ����ʵ�������±ȽϺ��ʵĻ���ʱ����________��
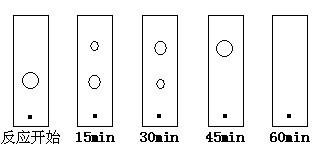
A��15min B��30min C��45min D��60min
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com