
【题目】O3是一种常见的绿色氧化剂,可由臭氧发生器(原理如图)电解稀硫酸制得。下列说法错误的是( )
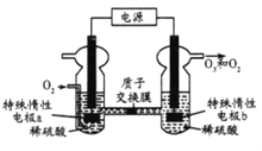
A.电极a为阴极
B.a极的电极反应为O2+4H++4e-═2H2O
C.电解一段时间后b极周围的pH上升
D.标准状况下,当有5.6LO2反应时,收集到O2和O3混合气体4.48L,O3的体积分数为80%
【答案】CD
【解析】
根据装置图,电极b中得到O2和O3,该电极中O的化合价升高,根据电解原理,电极b为阳极,则a为阴极,据此分析;
A. 根据装置图,电极b中得到O2和O3,该电极中O的化合价升高,根据电解原理,电极b为阳极,则a为阴极,故A说法正确;
B. 电极a为阴极,电解质为稀硫酸,其电极反应式为O2+4H++4e-=2H2O,故B说法正确;
C. 电极b产生O2和O3,电极反应式为2H2O-4e-=4H++O2、3H2O-6e-=6H++O3,一段时间后电极b周围c(H+)增大,pH下降,故C说法错误;
D. 根据电荷守恒,令SO3的物质的量为amol,根据电荷守恒,![]() ,解得a=0.1mol,混合气体物质的量为0.2mol,即O3的体积分数为
,解得a=0.1mol,混合气体物质的量为0.2mol,即O3的体积分数为![]() ×100%=50%,故D说法错误;
×100%=50%,故D说法错误;
答案:CD。


科目:高中化学 来源: 题型:
【题目】(1)一杯咖啡中含有0.194g咖啡因(分子式C8H10N4O2,M=194g/mol),你知道其中有_______个咖啡因分子;这些咖啡因分子中的N原子的物质的量为_________.
(2)经检测一瓶泉水样品,1.0L样品中含4.8×10﹣2g Mg2+,那么该泉水中Mg2+的物质的量浓度为____________.含1.0mol Mg的这种泉水的体积是_________L.
(3)0.2mol H2S,在标准状况下的体积约为_______L;相同质量的CH4和H2S中分子个数比为____________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下述转化关系,回答问题:

已知:①+CH3Br![]() CH3+HBr;
CH3+HBr;
②C物质苯环上一卤代物只有两种。
(1)写出B物质的名称__________;D物质的结构简式________。
(2)写出反应②的类型________;反应⑤的条件________。
(3)写出反应⑥的化学方程式:________________________________。
(4)写出D+E反应的化学方程式:_______________。
(5)反应②还有可能生成一种C16H18的有机物,其苯环上一卤代物也只有两种,写出它的结构简式:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学科学对提高人类生活质量和促进社会发展具有重要作用。下列说法正确的是( )
A.某些金属元素的焰色反应、海水提溴、煤的气化、石油的裂化都是化学变化的过程
B.氮氧化物的大量排放,会导致光化学烟雾、酸雨和温室效应等环境问题
C.油脂的主要成分是高级脂肪酸甘油酯,长时间放置的油脂会因水解而变质
D.白葡萄酒含维生素C等多种维生素,通常添加微量![]() 的目的是防止营养成分被氧化
的目的是防止营养成分被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃是由C、H元素组成的有机物、不同有机物的结构不同。试回答下列问题:
(1)分子式为C6H12的某烯烃的所有的碳原子都在同一个平面上,则该烯烃的结构式___,系统命名为___。
(2)组成符合CnH2n-2的某种烃,分子结构中没有支链或侧链,它完全燃烧时所消耗的氧气的体积是相同状态下该烃蒸气体积的8.5倍。
(a)若该烃为链状烯烃,并且与等物质的量的Br2加成只能得到某单一产物,则该烃的结构简式为___。
(b)若该烃只能与含等物质的量的Br2四氯化碳溶液发生反应,则其结构简式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
A.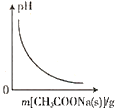 图表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化
图表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化
B.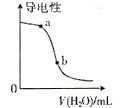 图表示向醋酸溶液中加水时其导电性变化,则CH3COOH溶液的pH:a点>b点
图表示向醋酸溶液中加水时其导电性变化,则CH3COOH溶液的pH:a点>b点
C.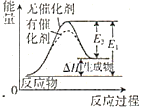 图表示催化剂能改变化学反应的焓变
图表示催化剂能改变化学反应的焓变
D. 图表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
图表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作能达到相应实验目的的是
选项 | 实验操作 | 实验目的 |
A | 室温下,用pH试纸分别测定浓度均为0.1mol/L HClO溶液和CH3COOH溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
B | 向10mL浓度均为0.1mol/L的BaCl2和CaCl2混合溶液中加入10mL 0.1mol/L Na2SO4溶液,出现白色沉淀 | 证明Ksp(BaSO4)<Ksp(CaSO4) |
C | 向含有酚酞试液的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
D | 室温下,等体积、pH=2的HA和HB两种酸分别与足量Zn反应,HB放出的H2多 | 证明HB是强酸 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组用浓度为0.20 mol·L-1的盐酸标准液滴定含有一定量杂质的烧碱样品(杂质与酸不反应)溶于水形成的溶液。
(1)准确量取一定体积的待测液需要使用的仪器是________________。
(2)若滴定开始和结束时,滴定管中的液面如图所示,则消耗盐酸标准液的体积为______mL。
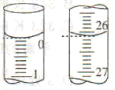
(3)用盐酸标准液滴定待测烧碱样品的溶液时,________(填“左手”或“右手”,下同)握酸式滴定管的活塞,________摇动锥形瓶,眼睛始终注视________________。
(4)滴定时,若以酚酞为指示剂,滴定达到终点的标志是__________。
(5)将准确称取的5.0g烧碱样品配制成250mL待测液,并用盐酸标准液滴定。滴定前读数及滴定后读数如表所示。
滴定次数 | 待测液体积(mL) | 0.20mol/L的盐酸体积(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 10.00 | 0.70 | 20.60 |
第二次 | 10.00 | 4.00 | 24.10 |
第三次 | 10.00 | 1.10 | 21.10 |
由实验数据可知,烧碱的纯度为________。
(6)下列操作会导致测得的待测液的浓度偏大的是________(填标号)。
a.部分标准液滴出锥形瓶外
b.用待测溶液润洗锥形瓶
c.锥形瓶洗净后还留有蒸馏水
d.放出碱液的滴定管开始有气泡,放出液体后气泡消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25°C 时,向 10 mL 0.10 mol·L-1 的 HA (Ka =1.0×10-4)中逐滴加入 0.10 mol·L-1NaOH 溶液,溶液 pH 随滴入的 V[(NaOH)aq]变化如下图所示。下列说法正确的是
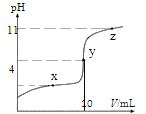
A.x 点,c(HA)> c(A-)
B.y 点,c(HA)+c(A-)=c(Na+) =0.10 mol·L-1
C.z 点,c(Na+) = c(A-) + c(OH-)
D.水的电离程度,x 点小于 y 点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com