
选考〔化学—物质结构与性质](13分)
钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,
反应原理为: 2Mn2++5S2O82-+8H2O 2MnO4-+10SO42-+16H+
2MnO4-+10SO42-+16H+
(1)基态锰原子的核外电子排布式为 _
(2)上述反应涉及的元素属于同主族元素,其第一电离能由大到小的顺序为 (填元素符号)。
(3)已知H2.S2O8的结构如图。

①H2.S2O8硫原子的轨道杂化方式为 。
②上述反应中被还原的元素为 。
③上述反应每生成1 mol MnO4 -,S2O82- 断裂的共价键类型及其数目为 。
(4)一定条件下,水分子间可通过O一H...O氢键将从H2O分子结合成三维骨架结构,其中的多面体孔穴中可包容气体小分子,形成笼形水合包合物晶体
①下图是一种由水分子构成的正十二面体骨架(“o”表示水分子),其包含的氢键数为 ;

②实验测得冰中氢键的作用能为18.8目kJ·mol-1,而冰的熔化热为5.0kJ·mol-1,其原因可能是 。
(1)1s22s22p63s23p63d54s2 (2)O>S
(3)①sp3 ② S ③非极性键 2.5NA
(4)①30 ②液态水中仍然存在大量氢键
【解析】
试题分析:(1)锰是25号元素,基态锰原子的核外电子排布式为1s22s22p63s23p63d54s2
(2)上述反应涉及的元素属于同主族元素是O和S,根据同主族元素,第一电离能从上到下依次减小,则其第一电离能由大到小的顺序为O>S,
(3)①H2.S2O8硫原子与氧原子形成4个键,所以其轨道杂化方式为sp3杂化,②上述反应中锰元素的化合价由+2价升高到+7价,是失电子被氧化,硫元素的化合价由+7价降低到+6价,得电子,被还原,所以被还原的元素为S ,③根据上述反应2Mn2++5S2O82-+8H2O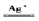 2MnO4-+10SO42-+16H+,转移10e-,可知每生成1 mol MnO4 -,S2O82- 断裂的共价键类型为非极性键及其数目为2.5NA。
2MnO4-+10SO42-+16H+,转移10e-,可知每生成1 mol MnO4 -,S2O82- 断裂的共价键类型为非极性键及其数目为2.5NA。
(4)①由水分子构成的正十二面体骨架,水分子数共为5/3×12=20个,每个水分子有一个氧原子,两个氢原子,水分子间可通过O一H...O氢键将从H2O分子结合成三维骨架结构,所以其包含的氢键数为20×1.5=30;②液态水中仍然存在大量氢键,所以实验测得冰中氢键的作用能为18.8目kJ·mol-1,而冰的熔化热为5.0kJ·mol-1。
考点:考查基态原子的核外电子排布式,第一电离能的判断,杂化轨道,非极性键等知识。


科目:高中化学 来源:2014-2015江苏省高二上学期期末考试化学试卷(解析版) 题型:选择题
已知C3N4晶体的硬度很可能比金刚石还大,且原子间均以单键结合,下列关于C3N4的说法正确的是

A.C3N4可能是分子晶体
B.C3N4晶体中C—N键的键长比金刚石的C—C键的键长要长
C.C3N4晶体是每个C原子连接4个N原子,每个N原子连接3个C原子
D.该晶体与金刚石相似,都是原子间以非极性键形成空间的网状结构
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省大冶市高三上学期期末联考理综化学试卷(解析版) 题型:选择题
利用如图所示装置进行下列实验,能得出相应实验结论的是
选项 | ① | ② | ③ | 实验结论 |
|
A. | 稀盐酸 | Na2S | 漂粉精溶液 | 酸性:盐酸>氢硫酸>次氯酸 | |
B. | 浓盐酸 | KMnO4 | Na2S溶液 | 氧化性:KMnO4> Cl2>S | |
C. | 浓氨水 | NaOH | 酚酞 | 碱性:NaOH >NH3·H2O | |
D. | 浓硫酸 | Na2SO3 | BaCl2溶液 | SO2与可溶性钡盐均不反应 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省兰州市高三下学期诊断考试理综化学试卷(解析版) 题型:实验题
[选修2—化学与技术](15分)金属钒被誉为“合金的维生素”,钒及其化合物在工业生产中有着广泛的应用。从废钒催化剂(主要成分有V2O5,VOSO4,K2SO4,SiO2等)中回收V2O5的生产流程图如下:

请回答:
(1)进行步骤①前,将废钒催化剂粉碎的目的是 。写出步骤①中发生氧化还原反应的离子方程式 。
(2)实验室中进行萃取分液操作时,用到的玻璃仪器有 。②③变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂)R2(SO4)n(水层)+2n HA(有机层) 2RAn(有机层) + n H2SO4(水层),为提高②中萃取百分率,应采取的措施是____ ;
2RAn(有机层) + n H2SO4(水层),为提高②中萃取百分率,应采取的措施是____ ;
(3)25°C时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
通过上表数据分析,在实际生产中,⑤中加入氨水,调节溶液的最佳pH为______;
(4)在焙烧NH4VO3的过程中,固体质量的减少值(纵坐标)随温度变化的曲线如下图所示,则NH4VO3在分解过程中 。

A.先分解失去H2O,再分解失去NH3
B.先分解失去NH3,再分解失去H2O
C.同时分解失去H2O和NH3
D.同时分解失去H2、N2和H2O
(5)全钒液储能电池的电解质溶液为VOSO4溶液,电池的工作原理为VO2++V2++2H+ VO2++H2O+V3+,电池放电时正极的电极反应式为 。
VO2++H2O+V3+,电池放电时正极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省兰州市高三下学期诊断考试理综化学试卷(解析版) 题型:选择题
科学家设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如下图所示,下列说法不正确的是

A.通入N2的电极发生的电极反应式为:N2 + 6e- + 8H+== 2NH4+
B.反应过程中溶液的pH会变大,故需要加入盐酸
C.该电池外电路电流从通入H2的电极流向通入N2的电极
D.通入H2的电极为负极,A为NH4Cl
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省厦门市高三质量检查理综化学试卷(解析版) 题型:选择题
工业上,在强碱性条件下用电解法除去废水中的CN-,装置如图所示,依次发生的反应有:
①CN- —2e- +2OH- ═CNO- +H2O
②2Cl- 一2e══Cl2 ↑
③3Cl2 +2CNO- +8OH-═N2 +6Cl-十2CO32-+4H2O
下列说法正确的是

A.铁电极上发生的反应为Fe一2e一═Fe2+
B.通电过程中溶液pH不断增大
C.为了使电解池连续工作,需要不断补充NaCl
D.除去1 mol CN-,外电路至少需转移5 mol电子
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省泉州市高三3月教学质量检查理综化学试卷(解析版) 题型:填空题
(13分)利用铜萃取剂M,通过如下反应实现铜离子的富集:

(1)X难溶于水、易溶于有机溶剂,其晶体类型为 。
(2)M所含元素的电负性由大到小顺序为 ,N原子以 轨道与O原子形成σ键。
(3)上述反应中断裂和生成的化学键有 (填序号)。
a.离子键
b.配位键
c.金属键
d.范德华力
e.共价键
(4)M与W(分子结构如图)相比,M的水溶性小,更利于Cu2+的萃取。M水溶性小的主要原因是 。

(5)基态Cu2+的外围电子排布式为 ,Cu2+等过渡元素水合离子是否有颜色与原子结构有关,且存在一定的规律。判断Sc3+、Zn2+的水合离子为无色的依据是 。
离子 | Sc3+ | Ti3+ | Fe2+ | Cu2+ | Zn2+ |
颜色 | 无色 | 紫红色 | 浅绿色 | 蓝色 | 无色 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省龙岩市高三教学质量检查理综化学试卷 (解析版) 题型:选择题
甲、乙是由同主族元素R、Z组成的两种单质,常温下能进行如下反应:甲 + 乙 + H2O —— HRO3 + HZ(未配平)。下列说法正确的是
A.R原子最外层电子数为5 B.单质的氧化性:甲>乙
C.原子半径:R>Z D.HRO3与HZ之计量数比为5:1
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省汕头市等三校高二上学期期末化学试卷(解析版) 题型:选择题
一定条件下,在某密闭容器中进行如下反应:mA(g)+nB(g) pC(g)+qD(g),若增大压强或升高温度,重新达到平衡,反应速率随时间的变化过程如图所示,则对该反应的叙述正确的是
pC(g)+qD(g),若增大压强或升高温度,重新达到平衡,反应速率随时间的变化过程如图所示,则对该反应的叙述正确的是

A.正反应是吸热反应 B.逆反应是放热反应
C.m+n<p+q D.m+n>p+q
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com