
【题目】25 ℃时,将浓度均为0.1 mol·L-1,体积分别为Va和Vb的HA溶液与BOH溶液按不同体积比混合,保持Va + Vb=100 mL,Va、Vb与混合液pH的关系如图所示,下列说法正确的是
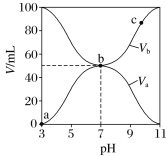
A. Ka(HA)=1×10-6
B. b点c(B+)=c(A-)=c(OH-)=c(H+)
C. a→c过程中水的电离程度始终增大
D. c点时,![]() 随温度升高而减小
随温度升高而减小
【答案】D
【解析】
根据图知,酸溶液的pH=3,则c(H+)<0.1mol/L,说明HA是弱酸;碱溶液的pH=11,c(OH-)<0.1mol/L,则BOH是弱碱。
A、由图可知 0.1molL-1HA 溶液PH=3,由 HAH++A-可知:Ka=![]() =10-5 molL-1,选项A错误;B、b点是两者等体积混合溶液呈中性,所以离子浓度的大小为:c(B+)=c(A-)>c(H+)=c(OH-),选项B错误;C、a→b是酸过量和b→c 是碱过量两过程中水的电离程受抑制,b点是弱酸弱碱盐水解对水的电离起促进作用,所以a→c 过程中水的电离程度先增大后减小,选项C错误;D、c 点时,
=10-5 molL-1,选项A错误;B、b点是两者等体积混合溶液呈中性,所以离子浓度的大小为:c(B+)=c(A-)>c(H+)=c(OH-),选项B错误;C、a→b是酸过量和b→c 是碱过量两过程中水的电离程受抑制,b点是弱酸弱碱盐水解对水的电离起促进作用,所以a→c 过程中水的电离程度先增大后减小,选项C错误;D、c 点时,![]() 在分子和分母同乘以氢离子的浓度,得到:
在分子和分母同乘以氢离子的浓度,得到:![]() =
=![]() ,而Ka=
,而Ka=![]() =10-5 molL-1,温度越高Kw越大,所以
=10-5 molL-1,温度越高Kw越大,所以![]() 越小,选项D正确;答案选D。
越小,选项D正确;答案选D。


科目:高中化学 来源: 题型:
【题目】(1)在一定条件下N2与H2反应生成NH3,请回答:
①若反应物的总能量为E1,生成物的总能量为E2,且E1>E2,则该反应为________(填“吸热”或“放热”)反应。
②已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为________________。
(2) N2H4和H2O2混合可作火箭推进剂,已知:16 g液态N2H4和足量氧气反应生成N2(g)和H2O(l),放出310.6 kJ的热量;2H2O2(l)===O2(g)+2H2O(l) ΔH=-196.4 kJ·mol-1。反应N2H4(g)+O2(g)===N2(g)+2H2O(l)的ΔH=____________kJ·mol-1。N2H4和H2O2反应生成N2(g)和H2O(l)的热化学方程式为_______________________________________。
(3)实验室用50 mL 0.50 mol·L-1盐酸与50 mL某浓度的NaOH溶液在如图所示装置中反应,通过测定反应过程中所放出的热量可计算中和热。该装置有两处明显的错误,其中一处是缺少一种玻璃仪器,该仪器的名称为____________;实验室提供了0.50 mol·L-1和0.55 mol·L-1两种浓度的NaOH溶液,应选择_____________mol·L-1的NaOH溶液进行实验。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中说明氨气具有还原性和碱性的是( )
A. 2NH3+3CuO=3Cu+N2+3H2O
B. 8NH3+3Cl3=6NH4Cl+N2
C. 4NH3+6NO![]() 5N2+6H2O
5N2+6H2O
D. NH3+HCl=NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为有效提升空气质量,国家强制各燃煤企业要对燃煤烟气进行脱硫、脱硝处理后排放。回答下列问题:
(1)燃煤烟气“脱硝”中涉及到的部分反应如下:
a.4NH3(g)+6NO(g) ![]() 5N2(g)+6H2O(g) △H 1
5N2(g)+6H2O(g) △H 1
b.4NH3(g)+5O2(g) ![]() 4NO(g)+6 H2O(g)△H2 =-925kJ·mol-1
4NO(g)+6 H2O(g)△H2 =-925kJ·mol-1
c.N2(g)+O2(g) ![]() 2NO(g)△H 3=+175kJ·mol-1
2NO(g)△H 3=+175kJ·mol-1
则△H 1=_____kJ/mol。
(2)向某恒容密闭容器中加入2molNH3、3molNO,在适当条件下发生(1)中反应a,反应过程中NO的平衡转化率随温度T、压强p的变化曲线如图所示:
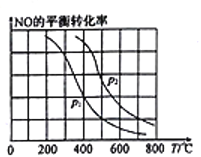
①p1________p2(填“>”“<”或“=”)。
②若在压强为加p2、温度为600℃时,达到平衡时反应体系内化学能降低了300kJ,则NO的转化率为_______________________。
③600℃时,下列各项数据中能表明该反应已达到化学平衡状态的是______。
a.水与NO的生成速率相等 b.混合气体的密度保持不变
c. NH3、NO生成速率比为5:4 d.容器的总压强保持不变
(3)将2molN2、3molH2O、0.5molNO的混合气体置于x、y、z三个容积相同的恒容密闭容器中,控制适当的条件发生反应,反应过程中c(NO)随时间的变化如图所示。
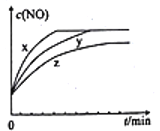
①在建立平衡的过程中,三个容器中反应速率的相对大小为______________。
②与y容器中反应相比,z容器中反应改变的条件及判断依据分别是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他利用NaHCO3、NaCl、NH4C1等物质溶解度的差异,以食盐、氨气、二氧化碳等为原料制得NaHCO3,进而生产出纯碱。以下A、B、 C、 D四个装置可组装成实验室模拟“侯氏制碱法”制取NaHCO3的实验装置。装置中分别盛有以下试剂:B:稀硫酸;C:盐酸、碳酸钙;D:含氨的饱和食盐水、水。

四种盐在不同温度下的溶解度(g/100 g水)表(说明:①>35 ℃ NH4HCO3会有分解)

请回答以下问题:
(1)装置的连接顺序应是__________(填字母)。
(2)A装置中盛放的试剂是__________,其作用是___________________。
(3)在实验过程中,需要控制D温度在30℃~35℃,原因是_________________。
(4)反应结束后,将锥形瓶浸在冷水中,析出NaHCO3晶体。用蒸馏水洗涤NaHCO3晶体的目的是除去____(杂质以化学式表示)。
(5)将锥形瓶中的产物过滤后,所得的母液中含有___________(以化学式表示),加入氯化氢,并进行_________操作,使NaCl溶液循环使用,同时可回收NH4Cl。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向四只盛有不同溶液的烧杯中逐滴加入稀盐酸至过量,并将溶液加热,产生的CO2气体与HCl物质的量的关系如图(忽略CO2的溶解和HCl的挥发):
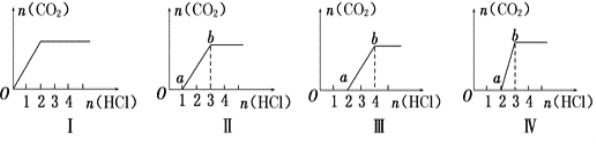
则下列分析都正确的组合是( )
①I图对应溶液中的溶质为NaHCO3
②II图对应溶液中的溶质为Na2CO3和NaHCO3,且二者的物质的量之比为1:1
③III图对应溶液中的溶质为NaOH和Na2CO3,且二者的物质的量之比为1:1
④IV图对应溶液中的溶质为Na2CO3
A.①② B.①③ C.②④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H是一种新型香料的主要成分之一,其合成路线如下(部分产物和部分反应条件略去):

已知:①RCH=CH2+CH2==CHR′![]() CH2=CH2+RCH=CHR′;
CH2=CH2+RCH=CHR′;
②B中核磁共振氢谱图显示分子中有6种不同环境的氢原子。
请回答下列问题:
(1)(CH3)2C=CH2的同分异构体中存在顺反异构的有机物的名称为________。
(2)A的核磁共振氢谱除苯环上的H外,还显示________组峰,峰面积比为________。
(3)D分子中含有的含氧官能团名称是________,E的结构简式为__________________。
(4) 发生加聚反应的化学方程式为____________________________;D和G反应生成H的化学方程式为_________________________________________。
发生加聚反应的化学方程式为____________________________;D和G反应生成H的化学方程式为_________________________________________。
(5)G的同分异构体中,同时满足下列条件的有________种(不包括立体异构)。
①苯的二取代物 ②与FeCl3溶液发生显色反应 ③含“-COO-”结构
(6)参照上述合成路线,以丙烯为原料(无机试剂任选),设计制备2,3-丁二醇的合成路线_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢。则A的结构简式是_____________。
(2)吗啡和海洛因都是严格查禁的毒品。吗啡分子中C、H、N、O的质量分数分别为71.58%、6.67%、4.91%和16.84%,已知其相对分子质量在200~300之间。吗啡的相对分子质量为_____________;吗啡的化学式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH4++6HCHO=3H++6H2O+(CH2)6N4H+ ,然后用NaOH标准溶液滴定反应生成的酸,某兴趣小组用甲醛法进行了如下实验:
步骤I 称取样品1.500g。
步骤II 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤Ⅲ 移取25.00mL样品溶液于250mL锥形瓶中,加入10mL20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:
①到达滴定终点时,俯视碱式滴定管读数,则测得样品中氮的质量分数________(填“偏高”、“偏低”或“无影响”)。
②达到滴定终点时,发现碱式滴定管的尖端有气泡,则滴定时用去NaOH标准溶液的体积__________ (填“偏大”、“偏小”或“无影响”)
③滴定时边滴边摇动锥形瓶,眼睛应观察___________
④滴定达到终点判断:__________________________________________
(2)滴定结果如下表所示:
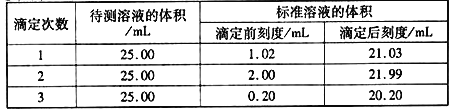
若NaOH标准溶液的浓度为0.1010mol·L-1则该样品中氮的质量分数为______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com