
【题目】用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
(1)准确称量8.2 g含有少量中性易溶杂质的样品,配成500 mL待测溶液。称量时,样品可放在________(填字母)称量。
A.小烧杯中 B.洁净纸片上 C.托盘上
(2)滴定过程中,眼睛应注视________________。滴定时,用0.2000molL-的盐酸来滴定待测液,不可选用______(填编号字母)作指示剂。
A.甲基橙 B.石蕊 C.酚酞
(3)滴定时,用0.200 0 mol·L-1的盐酸来滴定待测溶液,根据下表数据,计算被测烧碱溶液的物质的量浓度是________ mol·L-1,烧碱样品的纯度是________。
滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
第一次 | 10.00 | 0.40 | 20.50 |
第二次 | 10.00 | 4.10 | 24.00 |
(4)下列实验操作会对滴定结果产生什么后果?(填“偏高”、“偏低”或“无影响”)
①若将锥形瓶用待测液润洗,然后加入10.00mL待测液,则滴定结果______
②若锥形瓶未干燥就加入10.00mL待测液,则滴定结果______。
【答案】A 锥形瓶内溶液颜色的变化 B 0.4000 97.56% 偏高 无影响
【解析】
(1)易潮解的药品,必须放在玻璃器皿上(如小烧杯、表面皿)里称量;
(2)酸碱中和滴定时,可用酚酞或甲基橙做指示剂,石蕊变色范围宽且现象不明显,故一般不用石蕊作指示剂;
(3)根据c(待测)=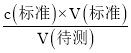 ,V(标准)用两次的平均值;根据m=cVM计算500mL溶液中氢氧化钠的质量,再根据质量分数公式计算氢氧化钠的质量分数;
,V(标准)用两次的平均值;根据m=cVM计算500mL溶液中氢氧化钠的质量,再根据质量分数公式计算氢氧化钠的质量分数;
(4)根据c(待测)=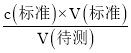 分析不当操作对V(标准)的影响,以此判断浓度的误差。
分析不当操作对V(标准)的影响,以此判断浓度的误差。
(1)烧碱易潮解,必须放在玻璃器皿上(如小烧杯、表面皿)里称量,故答案为A;
(2)滴定过程中,眼睛应注视锥形瓶内溶液颜色的变化;酸碱中和滴定时,可用酚酞或甲基橙做指示剂,石蕊变色范围宽且现象不明显,故一般不用石蕊作指示剂,故答案为B;
(3)第一次消耗的标准液的体积为:(20.50-0.40)mL=20.10mL,第二次消耗的标准液体积为:24.00mL-4.10mL=19.90mL,两次滴定数据都是有效的,所以消耗标准液平均体积为20.00mL,根据c(待测)=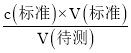 =
=![]() =0.4000molL-1,样品中含有烧碱的质量为:m(烧碱)=cVM=0.4000molL-1×0.5L×40g/mol=8.0g,烧碱的质量分数为:ω=
=0.4000molL-1,样品中含有烧碱的质量为:m(烧碱)=cVM=0.4000molL-1×0.5L×40g/mol=8.0g,烧碱的质量分数为:ω=![]() ×100%=97.56%;
×100%=97.56%;
(4)①若将锥形瓶用待测液润洗,然后加入10.00mL待测液,待测液的物质的量偏大,造成V(标准)偏高,根据c(待测)=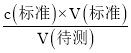 分析,可知c(待测)偏高;
分析,可知c(待测)偏高;
②若锥形瓶未干燥就加入10.00mL待测液,V(标准)无影响,根据c(待测)=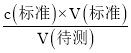 分析,可知c(待测)无影响。
分析,可知c(待测)无影响。


科目:高中化学 来源: 题型:
【题目】某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如图的实验装置。
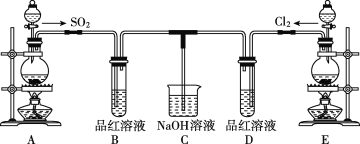
(1)实验室用装置E制备Cl2,其反应的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。若有6mol的HCl参加反应,则转移的电子总数为____。
MnCl2+Cl2↑+2H2O。若有6mol的HCl参加反应,则转移的电子总数为____。
(2)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:B____,D____。
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为:B____,D____。
(3)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1∶1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示):____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业合成氨反应在催化剂表面的反应历程及能量变化如图所示,下列说法正确的是
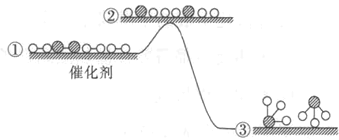
A.增大压强,①→②之间的能量差值会增大
B.合成氨的正逆反应的焓变相同
C.合成氨的过程是吸热反应
D.若使用催化剂,生成等量的NH3需要的时间更短
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的工业硫酸盐废水中含有大量的Fe2+、Fe3+、较多的Cu2+和少量的Na+。工厂计划从该废水中回收硫酸亚铁和金属铜,设计如下流程图。

回答下列问题;
(1)A的化学式为_________,D的化学式为_______。
(2)在工业废水中加入过量A时,发应的离子方程式有:___________、__________。
(3)得到FeSO47H2O晶体的操作Ⅲ为:加热浓缩、冷却结晶、______、______、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一个电化学过程的示意图如图所示。

请回答下列问题:
(l)通入CH3CH2OH一极的电极反应式为__________________________。
(2)乙池是铜的精炼池,则A电极的材料是_____________;反应一段时间后,乙池溶液中c(Cu2+)__________(填“增大”“变小”或“不变”)。
(3)丙池含有0.01 mol KCl的溶液100mL,假如电路中转移了0.03 mol e-,则阳极产生的气体在标准状况下的体积是________。
(4)丙池中滴有酚酞,实验开始后观察到的现象是_______________________________,写出丙池的总反应方程式:________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国药学家屠呦呦因发现植物黄花蒿叶中含有抗疟疾的物质—青蒿素而荣获2015年诺贝尔奖。科学家对青蒿素的结构进行进一步改良,合成药效更佳的双氢青蒿素、蒿甲醚。下列说法正确的是
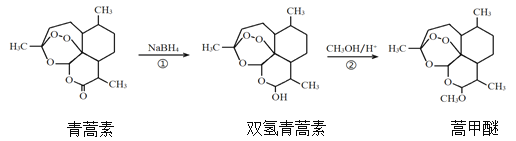
A.利用黄花蒿叶研究青蒿素结构的基本步骤为:元素分析确定实验式→测定相对分子质量确定分子式→波谱分析确定结构式
B.①、②的反应类型分别为还原反应、酯化反应
C.双氢青蒿素在水中的溶解性大于青蒿素
D.双氢青蒿素与蒿甲醚组成上相差-CH2-,二者互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2010年,中国首次应用六炔基苯在铜片表面合成了石墨炔薄膜(其合成示意图如右图所示),其特殊的电子结构将有望广泛应用于电子材料领域。下列说法不正确的是( )
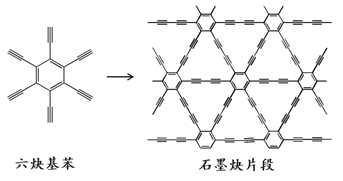
A.六炔基苯的化学式为C18H6
B.六炔基苯和石墨炔都具有平面型结构
C.六炔基苯和石墨炔都可发生加成反应
D.六炔基苯合成石墨炔属于加聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的量的计算是中学化学的重要部分,请回答下列有关物质的量的计算问题。
(1)在标准状况下,67.2 L CO2是__________mol,质量为_______g,含有__________个CO2分子,其中含有__________mol氧原子。
(2)在标准状况下,1.7 g氨气所占的体积约为_________L,它与同条件下_____mol H2S含有相同的氢原子数。
(3)某气态氧化物化学式为RO2,在标准状况下,1.28 g该氧化物的体积是448 mL,则氧化物的摩尔质量为_______,R的相对原子质量为__________。
(4)实验室常用浓硫酸的质量分数为98%,密度为1.80 g·mL1,其物质的量浓度是_______。
(5)标准状况下,将V L A气体(摩尔质量为M g/mol)完全溶于0.1 L水(密度1 g/cm3)中,所得溶液的密度为d g/mL,则此溶液的物质的量浓度为_______mol/L。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2O、NO和NO2等氮氧化物是空气污染物含有氮氧化物的尾气需处理后才能排放。
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为___。
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收。
①下列措施不能提高尾气中NO和NO2去除率的有___(填字母代号)
A.采用气、液逆流的方式吸收尾气
B.加快通入尾气的速率
C.吸收尾气过程中定补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是__(填化学式),吸收后排放的尾气中含量较高的氮氧化物是__(填化学式)。
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
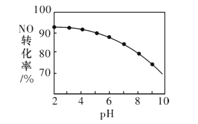
①在酸性NaClO溶液中,HC1O氧化NO生成Cl和NO3-,其离子方程式为__。
②NaClO溶液的初始pH越小,NO转化率越高,其原因是__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com